2.1. Состояние данной массы идеального газа описывается уравнением Менделеева - Клапейрона:
 ,
,
где P,T - давление и температура газа; V - объем, занимаемый данной массой газа (объем сосуда);  - число молей, содержащихся в данной массе газа; R - универсальная газовая постоянная, R = 8,31Дж/(моль·K ).
- число молей, содержащихся в данной массе газа; R - универсальная газовая постоянная, R = 8,31Дж/(моль·K ).
2.2. Исходя из уравнения состояния, можно определить плотность идеального газа:
 .
.
Между температурой t (по шкале Цельсия) и температурой T (по шкале Кельвина) существует следующая связь:
T =(t + 273,15)К  (t +273) К.
(t +273) К.
2.3. Вводя постоянную Больцмана  Дж/К уравнение состояния (2.1) примет вид:
Дж/К уравнение состояния (2.1) примет вид:
р = nkT,
где n – концентрация молекул.
2.4. Закон Дальтона для смеси газа.
Если в сосуде V при температуре T содержится смесь газов, то необходимо считать, что каждый из компонентов этой смеси распространяется по всему объему сосуда. Парциальное давление pi, создаваемое отдельным i -м компонентом смеси, определяется из уравнения Менделеева - Клапейрона:
 ,
,
где mi- масса данного компонента в смеси; 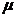 i - масса одного моля этого компонента.
i - масса одного моля этого компонента.
Давление смеси газов равно сумме парциальных давлений, входящих в нее газов:

или
 .
.
В равновесном состоянии плотность смеси ρ см равна сумме плотностей компонентов смеси:
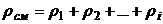 .
.
Пример 1. Смесь азота и гелия при температуре 270С находится под давлением Р = 1,3·102Па. Масса азота составляет 70% от общей массы смеси. Найти концентрацию молекул каждого из газов.
Дано: Р =1,3·102Па; m1 =0,7 m; m1 =28г/моль = 28·10-3кг/моль;  4г/моль=4·10-3 кг/моль; Т = 27+ 273 = 300К.
4г/моль=4·10-3 кг/моль; Т = 27+ 273 = 300К.
Найти: n 1 и n 2.
Решение. Давление смеси выразим по закону Дальтона:
 .
.
где Р 1 – парциальное давление азота в смеси; Р 2 – парциальное давление гелия.
Выразим Р 1и Р 2 из уравнения Менделеева - Клапейрона:
 ;
;  .
.
Найдем соотношение между Р 1 и Р 2:
 т. е. Р 2 = 3 Р 1.
т. е. Р 2 = 3 Р 1.
Так как
Рсм = Р1 + Р2 = Р1 + 3Р1 = 4Р1,
Следовательно,
 ,
,  .
.
С другой стороны, давление любого газа можно легко выразить через концентрацию его молекул (n) и температуру:
 ;
;  .
.
Отсюда
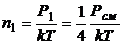 ;
; 
 .
.
Проверим размерность:

 .
.
Произведем вычисления:
 ;
;
n 2 = 3 n 1 = 2,4 ·1022 м-3.
Ответ: n 1 = 0,8·1022 м-3; n 2 = 2,4·1022м-3.
 2017-11-30
2017-11-30 797
797








