Установки УЗО предназначены для ультразвуковой предстерилизационной очистки в моющем или моюще-дезинфицирующем растворе ультразвуковым воздействием медицинских инструментов.
Цель:
- Удаление водорастворимых, частичнорастворимых органических соедине-
ний: кровь, белок, остатки микробов, лекарственных средств, твердых, жидких пленок из масел и жиров растительного (на новых инструментах) про исхождения;
- твердых частиц: костной ткани, пыли, продуктов коррозии.
Показания:
- Изделия медицинского назначения (ИМН), мелкие сложной конфигурации, проникающие в стерильные ткани тела или сосудистую стенку (после дезинфекции).
- кран
- устройство для дозированной подачи жидкого мыла
- разовое полотенце или сухое индивидуальное
- воздушный стерилизатор
- защитная одежда: шапочка, маска, очки, перчатки из плотной резины, специальная обувь.
- вентилируемое помещение
- емкость с моющим раствором
- инструкция по техники безопасности
- руководство по эксплуатации, утвержденное СЭС
- установки УЗО
- УЗО – 10-01 контейнер ЕДПО –10-01 с рабочим объемом 10 литров.
- методические указания по применению моющих средств для предстерилизационной очистки, утвержденных МЗ РФ.
- реактивы для проведения пробы на кровь и моющее средство
- журнал учета качества предстерилизационной очистки
| Процесс | Обоснование | |
| I. Подготовка к процедуре | ||
| Вымыть руки стандартным способом | Обеспечение инфекционной безопасности. Профилактика ВБИ. | |
| Осушить руки сухим, чистым, индивидуальным полотенцем | Обеспечение инфекционной безопасности. | |
| Надеть чистые печатки | Создание барьера инфицированию кожи медицинской сестры | |
| II Выполнение процедуры | ||
| Инструмент, прошедший цикл дезинфекции в емкости ЕДПО с заранее уложенной на дно поддона пластиной, отражателем, промыть в поддоне, залить 1% моющим раствором Бланизола. (рис. 1) | Обеспечение необходимого контакта инструмента с моющим раствором. (Концентрация раствора важна для качества предстерилизационной очистки). | |
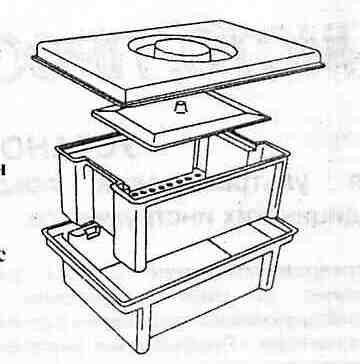 Рис. 5 ЕДПО (контейнер) Рис. 5 ЕДПО (контейнер) | ||
| Закрыть крышкой (которая совмещена с излучателем ультразвука). (рис.5, 6) | Предотвращение испарения растворов. Наличие контакта излучающей пластины с раствором повышают эффективность очистки. | |
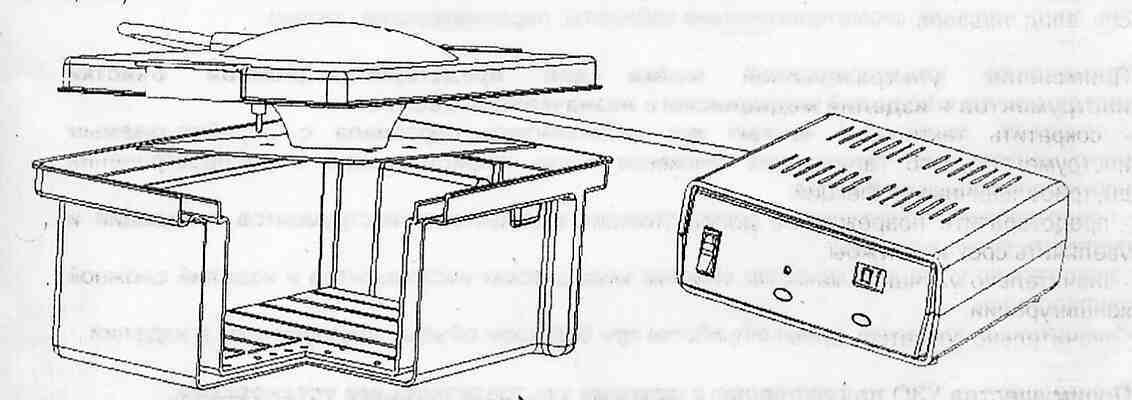 Рис. 6 Установка УЗО Рис. 6 Установка УЗО | ||
| Включить в сеть. Нажать на таймер. Задать требуемое время для очистки – 30 минут. | Установленное и текущее время фиксируется на цифровом табло, щадящий режим, высокое качество предстерилизационной очистки. | |
| Происходит удаление загрязнений в раствор. | Ультразвуковой излучатель образует колебания, которые вызывают возникновение в жидкой среде упругих волн и невидимых глазом пульсирующих воздушных пузырьков. Это порождает гидродинамическое воздействие на обрабатываемые поверхности. | |
| После проведения ультразвуковой очистки инструмент вновь промыть в поддоне проточной водой. | Удаление токсических веществ с поверхности обрабатываемых изделий значительно. Значительно сокращается время обработки при большом объеме инструментов. | |
| Залить дистиллированную воду. Повторить №2,3,4. | Обессоливание поверхности изделий предупреждает повреждение тканей. Качество очистки соответствует требованиям стандарта. | |
| Выключить из сети. Извлечь инструменты, поместить на металлические сетки. | Соблюдение техники безопасности. | |
| Подсушить в воздушном стерилизаторе при температуре 80-850 С. | Условия для проведения стерилизации. | |
| Сделать пробы (на скрытую кровь и остатки моющего средства). | Оценивание качества механической очистки. | |
| Результаты пробы записать в журнал учета качества предстерилизационной очистки. | Осуществление контроля, учета и преемственности. | |
| III Завершение процедуры | ||
| Снять перчатки стандартным способом и подвергнуть их дезинфекции в соответствии действующих СанПиНов. | Недопущение загрязнения рук при снятии перчаток. | |
| Вымыть руки с мылом под проточной водой стандартным способом. | Обеспечение инфекционной безопасности. | |
| Осушить руки сухим, индивидуальным полотенцем. | Обеспечение инфекционной безопасности. | |
| Контроль качества: - по пунктам |
«Азопирамовая проба».
Цель: Контроль качества предстерилизационной очистки (на наличие скрытой крови)
Проводится:
- в централизованной стерилизационной ежедневно
- самоконтроль в отделении мед.сестрой ежедневно
- старшей мед сестрой – 1 раз в неделю
- Устройство для дозированной подачи жидкого мыла
- Разовое полотенце или сухое индивидуальное
- Кран
- 1% изделий одного наименования, но не менее 3ед. прошедшие предстерилизационную очистку
- исходный раствор азопирама, приготовленный аптекой,
- 3% перекись водорода
- марлевая салфетка
- стекла с мазками крови
- журнал учета результатов контроля предстерилизационной очистки
| Процесс | Обоснование | |
| I. Подготовка к процедуре | ||
| Вымыть руки стандартным способом | Механическое удаление грязи, продуктов жизнедеятельности кожи, временных и некоторых резидентных микроорганизмов. | |
| Осушить руки сухим, чистым, индивидуальным полотенцем | Обеспечение инфекционной безопасности. | |
| Надеть защитную одежду (маска, косынка, перчатки) | Создание барьера инфицированию кожи медицинской сестры | |
| Приготовить рабочий раствор азопирама смешивая равные объемы (1:1) исходного раствора азопирама и 3% перекиси водорода, рабочий раствор пригоден к употреблению только в течение 1-2 часов. | Выявление наличия гемоглобина (скрытой крови) на изделиях медицинского назначения. | |
| II Выполнение процедуры | ||
| Проверить активность рабочего раствора, капнув несколько капель на стекло с мазком крови | Определение пригодности и активности рабочего раствора (реактив меняет цвет на фиолетовый сразу же или не позже 1-2 минут). |
| Холодные изделий (То не выше 25оС) проверить тампоном, смоченным реактивом или нанести 3-4 капли рабочего раствора пипеткой на инструмент. | Повышение температуры исследуемых изделий способствует разрушению реактива или его спонтанному окрашиванию. | |
| Экспозиция 0,5-1 минута. | Соблюдение технологии. | |
| Проверку качества очистки катетеров или других полых изделий оценивают путем введения реактива внутрь изделий с помощью чистого одноразового шприца или пипеткой. | Обеспечение проникновения рабочего раствора в места соединения. | |
| Инструмент держать над марлевой салфеткой и наблюдать за изменением цвета стекающего раствора. | Оценивание результата. | |
| Чтение пробы: - фиолетовое окрашивание переходящее в розово-сиреневое появляется при наличии на изделии гемоглобина сразу же или не позже 1-2 минут. -Буроватое окрашивание – при наличии окислителей, хлорамина, хлорной извести, стирального порошка, отбеливателей, ржавчины. | Изменение цвета позже, чем через одну минуту, не засчитывается | |
| Независимо от результата пробы изделие промыть проточной водой | Удаление токсичных веществ. | |
| При положительной пробе вся партия изделий подлежит повторной очистке. | Обеспечение качества очистки ИМН. | |
| III Завершение процедуры | ||
| Снять перчатки стандартным способом и подвергнуть их дезинфекции в соответствии действующих СанПиНов. | Недопущения загрязнения рук при снятии перчаток. | |
| Вымыть руки стандартным способом. | Обеспечение инфекционной безопасности. | |
| Осушить руки сухим, индивидуальным полотенцем. | Обеспечение инфекционной безопасности | |
| Результаты пробы записать в журнал учета. | Осуществление контроля, учета и преемственности. | |
| Контроль качества: - по пунктам |
Цель: Контроль качества предстерилизационной очистки (на скрытую кровь)
Проводится:
- в централизованной стерилизационной ежедневно
- самоконтроль в отделении мед.сестрой ежедневно
- старшей мед сестрой – 1 раз в неделю
- Устройство для дозированной подачи жидкого мыла
- Разовое полотенце или сухое индивидуальное
- Кран
- 1% изделий одного наименования, но не менее 3ед. прошедшие предстерилизационную очистку
- 5% спиртовой раствор амидопирина, приготовленный аптекой
- 3% раствор перекиси водорода
- 30% раствор уксусной кислоты
- марлевая салфетка
- стекла с мазками крови
- журнал учета результатов контроля предстерилизационной очистки
| Процесс | Обоснование | |
| I. Подготовка к процедуре | ||
| Вымыть руки стандартным способом | Механическое удаление грязи, продуктов жизнедеятельности кожи, временных и некоторых резидентных микроорганизмов. | |
| Осушить руки сухим, чистым, индивидуальным полотенцем | Обеспечение инфекционной безопасности. | |
| Надеть защитную одежду (маска, косынка, перчатки) | Создание барьера инфицированию кожи медицинской сестры | |
| Приготовить реактив, смешав в равных количествах 5% спиртовый р-р амидопирина, 3% р-р перекиси водорода, 30% раствор уксусной кислоты разными промаркированными пипетками. Рабочий раствор пригоден к употреблению только в течение 1-2 часов. | Выявление наличия гемоглобина (крови) на изделиях медицинского назначения. | |
| II Выполнение процедуры | ||
| Проверить активность рабочего раствора, капнув несколько капель на стекло с мазком крови. | Определение пригодности и активности рабочего раствора (реактив меняет цвет на сине-фиолетовый сразу же или не позже 1-2 минут). | |
| Холодные изделий (То не выше 25оС) проверить тампоном, смоченным реактивом или нанести 3-4 капли рабочего раствора пипеткой на инструмент. | Необходимые условия для проведения пробы. | |
| Экспозиция 0,5-1 минута. | Соблюдение технологии. | |
| При проверке качества очистки катетеров или других полых изделий оценивают путем введения реактива внутрь изделий с помощью чистого одноразового шприца. | Обеспечение проникновения рабочего раствора в места соединения. | |
| Инструмент держать над марлевой салфеткой и наблюдать за изменением цвета стекающего раствора. | Оценивание результата. | |
| Чтение пробы: - сине-фиолетовое окрашивание появляется при наличии на изделии скрытой крови сразу же или не позже 1-2 минут. | Изменение цвета позже, чем через одну минуту, проба не засчитывается | |
| Независимо от результата пробы изделие промыть проточной водой | Удаление токсичных веществ. | |
| При положительной пробе вся партия изделий подлежит повторной очистке. | Обеспечение качества очистки ИМН. | |
| III Завершение процедуры | ||
| Снять перчатки стандартным способом и подвергнуть их дезинфекции в соответствии действующих СанПиНов. | Недопущение загрязнения рук при снятии перчаток. | |
| Вымыть руки стандартным способом и осушить сухим, индивидуальным полотенцем. | Обеспечение инфекционной безопасности. | |
| Результаты пробы записать в журнал учета. | Осуществление контроля, учета и преемственности. | |
| Контроль качества: - по пунктам |
Цель: Контроль на наличие остатков моющего средства:
- в централизованной стерилизационной ежедневно
- самоконтроль в отделении мед.сестрой ежедневно
- старшей мед сестрой -1 раз в неделю
- 1% изделий одного наименования, но не менее 3ед. одного наименования
- 1 % спиртовый раствор фенолфталеина, приготовленный в аптеке
- Вата
- Устройство для дозированной подачи жидкого мыла
- Изделия медицинского назначения прошедшие предстерилизационную очистку
- Разовое полотенце
- Емкость с дистиллированной водой
- Защитная одежда: халат, шапочка, очки, маска, перчатки, спец. обувь.
- Журнал учета качества результатов контроля предстерилизационной очистки
| Процесс | Обоснование | |
| I. Подготовка к процедуре | ||
| Вымыть руки стандартным способом | Обеспечение инфекционной безопасности. | |
| Осушить руки сухим, чистым, индивидуальным полотенцем | Обеспечение инфекционной безопасности. | |
| Надеть защитную одежду (халат, маска, косынка, перчатки) | Предупреждение инфицирования кожи медицинской сестры | |
| Приготовить 1% спиртовый раствор фенолфталеина | Определение наличия остатков моющих средств(поверхностно – активных веществ). | |
| II Выполнение процедуры | ||
| 2-3 капли 1% спиртового раствора фенолфталеина нанести на инструмент (на места соединения подвижных частей инструмента) | Обеспечение проникновения рабочего раствора | |
| Экспозиция 0,5 –1 минута | Соблюдение технологии. | |
| Проверку качества промывания катетеров или других полых изделий оценивают путем введения реактива внутрь изделий с помощью чистого одноразового шприца или пипетки. | Обеспечение проникновения рабочего раствора. | |
| Инструмент держать над марлевой салфеткой и наблюдать за изменением цвета стекающего раствора. | Оценивание результата. | |
| Экспозиция 0,5-1 минута | Соблюдение технологии. | |
| 6. | Появление розового окрашивания (экспозиция 0,5-1 минута) свидетельствует о неполном отмывании щелочных добавок моющего раствора | Изменение цвета позже, чем через одну минуту не считается положительной (в соответствии с технологией). |
| 7. | При наличии «+» пробы, всю партию изделий промывают повторно проточной водой, затем дистиллированной и выкладывают на решетку для сушки в воздушном стерилизаторе при Т 85°С до полного исчезновения влаги. | Удаление токсических веществ с поверхности обрабатываемых изделий Стерилизуемые ИМН должны быть сухими. |
| III Завершение процедуры | ||
| Снять перчатки стандартным способом и подвергнуть их утилизации в соответствии действующими СанПиНами. | Недопущение загрязнения рук при снятии перчаток. | |
| Вымыть руки стандартным способом. | Обеспечение инфекционной безопасности. | |
| Осушить руки сухим, индивидуальным полотенцем. | Обеспечение инфекционной безопасности. | |
| Результаты пробы записать в журнал учета. | Осуществление контроля, учета и преемственности. | |
| Контроль качества:- по пунктам |
Тест – эталонный контроль по теме:
«Предстерилизационная обработка».
1. Проба на наличие скрытой крови:
а) фенолфталеиновая
б) с Суданом-3
в) амидопириновая
2. Контроль предстерилизационной очистки проводится СЭС:
а) 1 раз в неделю
б) 1 раз в месяц
в) 1 раз в квартал
г) 1 раз в год
3. Для дезинфекции шприцы и иглы погружают в 3% р-р хлорамина на:
а) 15мин. б) 60мин.
в) 45мин. г) 120мин.
4. Температура моющего раствора при предстерилизационной очистке ме-
дицинского инструментария (в градусах):
а) 55-650 б) 45-500
б) 25-350 г) 18-200
5. При попадании крови на слизистую ротоглотки необходимо:
а) прополоскать рот и горло 3% раствором перекиси водорода
б) прополоскать рот и горло 0.5% раствором хлорамина
в) прополоскать рот и горло 700 этиловым спиртом
6. Приготовление 1 литра моющего раствора для предстерилизационной
обработки инструментария:
а) 5 гр. Любого порошка, 200 мл 3% перекиси водорода довести до
литра водой
б) 5 гр. Порошка "Лотос", 160 мл 3% перекиси водорода довести до
литра водой
в) 5 гр. Порошка "Лотос" развести в 1 литре воды
г) 10 гр. порошка развести в 990 мл воды
7. При загрязнении кровью подушечки для рук, жгута для в/в инъекций, их
дезинфицируют:
а) в 15% растворе хлорамина - 2 часа
б) в 0.5% растворе хлорной извести - 3 часа
в) в 3% растворе хлорамина - 1 час
8. Раствор хлорамина, применяемый для дезинфекции мединструментов
после больных с вирусным гепатитом:
а) 10% б) 6% в) 5% г) 3%
9. Экспозиция при замачивании мединструментов в моющем растворе при
предстерилизационной очистке (в минутах):
а) 45мин б) 30ми в) 15мин г) 10мин
10. Номер приказа МЗ СССР, регламентирующий санитарно-противо -
эпидемиологический режим ЛПУ по профилактике гепатита:
а) №720 б) №770 в) №408 г) №288
11. Количество перекиси водорода в моющем растворе:
а) 6% раствор перекиси водорода 180 мл
б) 3% раствор перекиси водорода 160 мл
в) 3% раствор перекиси водорода 360 мл
12. Проба на наличие остаточного количества моющего средства:
а) фенолфталеиновая
б) с Суданом-3
в) азопирамовая
г) амидопириновая
13. Контролю предстерилизационной очистке подвергают:
а) 3% от одновременно обработанных изделий
б) 1% от одновременно обработанных изделий, но не менее 3-5 единиц
изделий одного наименования
в) все обработанные изделия
14. Для приготовления 3% раствора хлорамина необходимо взять:
а) 3 гр. сухого хлорамина и воды 1 литр
б) 30 гр. сухого хлорамина и воды 10 литров
в) 300 гр. сухого хлорамина и воды 10 литров
г) 300 гр. сухого хлорамина и воды 1 литр
15. Для приготовления 1 литра моющего раствора при предстерилизационной обработке инструментов необходимо взять пергидроля 27,5% (в мл):
а) 33 б) 30 в) 17 г) 14
16. Положительная азопирамовая проба на скрытую кровь дает окрашивание:
а) зеленое в) красное
б) розовое г) фиолетовое
17.Срок использования маски в процедурной, перевязочной (в часах):
а) 6 б) 4 в) 3 г)2
18. Для приготовления 1 литра 1% раствора Виркона нужно взять сухого
порошка (в граммах):
а) 100 б) 20 в) 30 г)10
19. Для приготовления 1 литра 3% раствора пероксимеда необходимо взять
30% средства (в мл):
а) 100 б) 10 в) 33 г) 200
20. Для приготовления 1 литра 2% раствора лизоформина 3000 необходимо взять средства (в мл):
а) 10 б) 20 в) 30 г) 200
Эталон ответов к тесту по теме:
«Предстерилизационная обработка».
| 1 - в |
| 2 - в |
| 3 - б |
| 4 - б |
| 5 - в |
| 6 - б |
| 7 - в |
| 8 - г |
| 9 - в |
| 10 –в |
| 11 –б |
| 12 – а |
| 13 -б |
| 14 -в |
| 15 -в |
| 16 -г |
| 17 -г |
| 18 -г |
| 19 -а |
| 20 -б |
| Критерий выставления оценки: "5" - 20-19 "4" - 18-17 "3" - 16-15 "2" - 14 и меньше |
Используемая литература:
1. Обуховец Т.П. «Основы сестринского дела. Практикум», Ростов-на-Дону, 2005 (2011).
2. Мухина С.А. Тарновская И.И. Теоретические основы сестринского дела: Учебник. – 2-е изд., испр. и доп. – Москва Издательская группа Гэотар-Медиа, 2008 (2010).
3. Мухина С. А., Тарновская И. И. «Практическое руководство к предмету «Основы сестринского дела» Москва Издательская группа Гэотар-Медиа, 2008 (2010).
Дополнительные источники:
· СанПиН 2.1.7.2790-10 «Санитарно-эпидемиологические требования к обращению с медицинскими отходами». УТВЕРЖДЕНЫ постановлением Главного государственного санитарного врача Российской Федерацииот 09.12. 2010г. № 163
· СанПиН 2.1.3. 2630-10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность». Утвержден постановлением Главного санитарного врача РФ от 18 мая 2010 года № 58
· Инструкция по применению индикаторов стерилизации одноразового
применения ИС-120, ИС-132, ИС-160, ИС-180 (МЗ РФ №154, 004. 98 ИП от 18.02.98 г.)
· Приказ №720 от 31.07.1978 г. город Москва «Об улучшении медицинской помощи больным с гнойными хирургическими заболеваниями и усиление мероприятий по борьбе с внутрибольничной инфекцией».
· Приказ №254 МЗ РФ от 03.09.91 г. «Развитие дезинфекционного дела в стране».
· Приказ МЗ СССР №770 от 10.06.85г «О введении в действие отраслевого стандарта ОСТ 42-21-2-85 «Стерилизация и дезинфекция изделий медицинского назначения. Методы, средства и режимы»
 2017-12-14
2017-12-14 1997
1997







