Якщо в колоїдний розчин додати електроліт, то це приведе до того, що іони дифузійного шару перейдуть в адсорбційний шар. Гранула стане електронейтральною. Таку зміну викликає коагуляційний іон (іон, заряджений протилежно гранулі).
Чим вище валентність коагуаляційного іону, тим швидше гранула стане електронейтральною.
Такий стан розчину, коли усі гранули електронейтральні називають ізоелектричним. В ізоелектричному стані колоїдні розчини втрачають свою стійкість, втрачають відштовхуючі сили і починають діяти сили тяжіння. Частинки зліплюються, розчин коагулює.
Коагуляція - процес злипання колоїдних частинок, утворення більш крупних агрегатів з наступною втратою колоїдною системою седиментаційної стійкості.
Коагуляцію можна викликати нагріванням, замерзанням, перемішуванням, центрифугуванням, додаванням різних електролітів.
Найбільш легко досягається коагуляція золей під дією електролітів. Додаванням електролітів до іоностабілізованого колоїдного розчину призводить до зниження електрокінетичного потенціалу, тобто до зменшення сил відштовхування.
Відрізняють 3 види коагуляції:
1) Взаємна коагуляція. Проходить при зливанні двох різнойменно заряджених розчинів. Має велике практичне значення. У виробництві барвників, порошку тощо.
2) Нейтралізаційна коагуляція. Викликається стабілізатором - електролітом, якщо він адсорбує не вибірково, а еквівалентно.
3) Концентраційна коагуляція. Визначається електролітом заданої концентрації.
Поріг коагуляції - це та найменша кількість електроліту, яку необхідно витратити для видимої коагуляції колоїдного розчину.
Коагуляція - процес зворотній. Зворотній процес пептизація, яка викликається спеціальною речовиною - пептизатором. Пептизатор: вода, електроліти.
Правило Шульце - Гарді: коагулюючу дію виявляють лише ті іони доданого електроліту, який має знак заряду, протилежний гранулі, дія іонів - коагуляторів у декілька разів збільшується з підвищенням їх валентності.
Запитання до семінару.
1. Яку будову має подвійний електричний шар?
2. Яка будова міцели і яка її частина рухається до електроду при електрофорезі?
3. Яка основна причина агрегативної стійкості гідрофобних золей?
4. Що таке коагуляція?
5. Які фактори визивають коагуляцію?
6. Який іон електроліту володіє коагулюючою дією?
7. Що таке поріг коагуляції?
8. Який стан золю називають ізоелектричним?
9. Яке практичне значення коагуляцій них процесів?
10. При яких умовах можливо утворення коагуляційної структури?
11. Які причини можуть визвати утворення гелю?
12. Чим пояснюється синерезис гелів?
13. Що називають тиксотропією?
14. Що таке пептизація?
15. В якому випадку вважається, що рідина підпорядковується закону Ньютона?
16. При якій умові рівняння Шведова-Бінгама перетворюється в рівняння Ньютона?
17. На які групи розподіляють ПАР?
18. Як залежить поверхневий натяг розчину колоїдних ПАР від концентрації?
19. Чи можливо змінити концентрацію в розчинах колоїдних ПАР?
20. Що називають критичною концентрацією міцелеутворення?
21. Напишіть формулу міцели золю бромистого срібла, одержаного при взаємодії розбавленого бромистого калію з надлишком азотнокислого срібла.
22. У три колби налито по 100 см3 золю Fe(ОН)3. Щоб викликати коагуляцію золя, знадобилося добавити у першу колбу 10,5 см3 1 н КСІ, у другу – 62,5 см3 0,01 н
Na2SO4, у третю – 37,0 см3 0,001 н Na3PO4. Розрахуйте пороги коагуляції і визначте знак частинки золю.
23. Напишіть формулу міцели золю берлінської лазурі, одержаного при взаємодії K4[Fe(CN)6] з надлишком хлористого заліза.
24. Написати формулу золя золота, стабілізованого KAuO2. У якого із електролітів: NaCI, BaCI2, FeCI3 поріг коагуляції буде мати найменшу величину?
25. Пороги коагуляції електролітів (ммолль/л) для хлориду срібла:
C 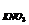 = 50,0 C
= 50,0 C 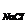 = 51,0 C
= 51,0 C 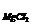 = 0,717 C
= 0,717 C 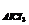 = 0,093
= 0,093
Визначити знак заряду частинок золю.
26. До 100 см3 0.03% розчину хлориду натрію добавлено 250 см3 0,01 н AgNO3. Щоб викликати коагуляцію, до одержаного золю хлориду срібла добавили такі електроліти: KBr, MgSO4, AICI3, K2CrO4. Який із добавлених електролітів має найменший поріг коагуляції, найменшу коагулюючу здатність?
27. Золь йодиду срібла одержали змішуванням рівних об’ємів розчинів йодиду калію і нітрату срібла. Пороги коагуляції для різних електролітів і даного золя мають значення (ммоль/л):
C 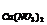 = 315 C
= 315 C 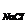 = 300 C
= 300 C 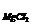 = 320 C
= 320 C 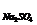
 = 20
= 20
У якого із електролітів: КСІ чи AgNO3 концентрація більша? Дайте обґрунтовану відповідь.
Семінар № 8
Тема: Колоїдні ПАР, грубодисперсні системи.
Мета: Вивчити властивості мікрогетерогенних та грубодисперсних систем, знати засоби отримання, стабілізації та руйнування суспензій та емульсій.
Вивчити грубодисперсні системи: піни, аерозолі, порошки. Навчитися проводити стабілізацію та коагуляцію цих дисперсних систем. Використовувати методи добування та руйнування цих систем. Знати і вміти відрізняти пасти від інших дисперсних систем, класифікацію паст, які використовуються в харчовій промисловості. Знати основні типи високомолекулярних сполук, властивості їх розчинів, вміти порівнювати розчини ВМС з дисперсними системами та істинними розчинами, розраховувати ступінь набрякання.
Методичні вказівки.
До мікрогетерогенних та грубодисперсних систем відносяться суспензії, емульсії, аерозолі, порошки. У порівнянні з колоїдними частинками в цих системах частинки дисперсної фази мають значно більші розміри. Як і колоїдні системи, мікрогетерогенні і грубодисперсні системи термодинамічне неврівноважені і мають тенденцію до самовільного зменшення дисперсності шляхом агрегації частинок дисперсної фази.
Суспензії - дисперсні системи з твердою дисперсною фазою і рідким дисперсним середовищем.
Суспензії - дуже розповсюджені дисперсні системи. До них відносяться глинисті, цементні та вапняні "розчини". Шоколадна маса при температурі вище 35°С представляє собою суспензію частинок какао і кристалів цукру у рідині какао -олії.
Суспензія карбонату кальцію утворюється при очищенні соку цукрового буряка (дифузійного соку) шляхом послідовної обробки його розчином Са(ОН)2і диоксидом вуглецю.
 2018-01-08
2018-01-08 1659
1659








