Электронное облако:
· Это область атомного пространства, в которой вероятность обнаружения электрона максимальна;
· Это траектория движение электрона
· Это атомная электронная орбиталь
Квантовые числа электронов в атоме:
1) Главное квантовое число n. Характеризует энергию электрона на уровне. Принимает значение на уровне 1,2,3,4…. Значение главного квантового числа – номер уровня.
Чем больше значение n, тем больше энергия электрона на уровне, тем дальше от ядра может находиться электрон.
n характеризует размеры электронного облака.
2) Побочное квантовое число l. Характеризует энергию электрона на подуровне.
Принимает значения: 1,2,3..
l max= n-1
| n | |||
| l | 0, 1 | 0, 1, 2 |
Значение l – номер подуровня. Чаще всего подуровни обозначаются буквами:
| s | p | d | f |
Побочное квантовое число характеризует форму орбитали:

Полная энергия электрона в атоме:
n+l
Т.е. энергия электрона в атоме зависит от размеров атомной электронной орбитали и ее формы.
3) Магнитное квантовое число m(me). Характеризует ориентацию электронного облака в атомном пространстве.
Количество значений m определяется по формуле:
2 l +1
| n | ||||
| l | 0,1 | 0,1,2 | ||
| m | -1,0,1 | -2,-1,0,1,2 | -3,-2,-1,0,1,2,3 | |
| Кол-во значений m | 1 значение | 3 значения | 5 значений | 7 значений |
Значения m, n, l характеризуют полностью атомную орбиталь. Атомная орбиталь – состояние электронов, которое характеризуется определенными значениями m, n, l.
4) Спиновое квантовое число s (ms). Характеризует движение электрона вокруг собственной оси (не вокруг ядра).
 - электрон вращается вокруг своей оси по часовой стрелке
- электрон вращается вокруг своей оси по часовой стрелке
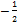 - электрон вращается вокруг своей оси против часовой стрелки
- электрон вращается вокруг своей оси против часовой стрелки
 2018-01-21
2018-01-21 1373
1373
