Хим в-ва и эл. взаимодействуют в соотношениях, пропорциональных их химическим эквивалентам (хим.вещество + хим. вещество или хим. элемент + хим. элемент).
Химический эквивалент элемента (в-ва) –такое его кол-во, которое без остатка взаимодействует с одной весовой частью Н или с 8-мью весовыми частями О.
Масса одного эквивалента вещества – эквивалентная масса [mэ].
Эквивалентная масса химического элемента:
 ,
,
где В – валентность.
Например, эквивалентная масса азота:
| Соединение | N2O | NO | N2O3 | NO2 | N2O5 |
| mэ | 14/1 | 14/2 | 14/3 | 14/4 | 14/5 |
mэ(H)=1г/экв mэ(О)=8г/экв
Эквивалентная масса вещества:
· для кислоты:
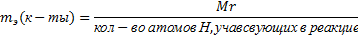
| Реакция | mэ(H3PO4) |
| H3PO4 + 3KOH = K3PO4 +3HOH | 98/3 |
| H3PO4 + 2KOH = K2HPO4 +2HOH | 98/2 |
| H3PO4 + KOH = KH2PO4 +HOH | 98/1 |
· для основания

| Реакция | mэ(Al(OH)3) |
| Al(OH)3 + 3HCl = AlCl3 + 3HOH | 78/3 |
| Al(OH)3 + 2HCl = AlOHCl2 + 2HOH | 78/2 |
| Al(OH)3 + HCl = AL(OH)2Cl + HOH | 78/1 |
· 
· 
Математическая формулировка закона:

m1 и m2 могут быть в г, кг, весовых частях, %
Для газов:

Эквивалентный объем Vэ – это объем одного эквивалента газа при нормальных условиях.
Vэ(H2) =22,4/2 = 11,2 л/экв

|

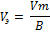
Закон кратных отношений открытый Дальтоном (1803г), гласит:
Если два эл. образуют между собой несколько соединений, то массы атомов одного эл., приходящиеся на одну и ту же массу атомов другого эл., соотносятся между собой как небольшие целые числа
Пример:
Сера образует два оксида - SO2 и SO3. ОАМ серы и кислорода равна 32 и 16. Массовое отношение серы и кислорода в SO2 равно 32: (2·16) = 32: 32, в SO3 32: (3·16) = 32: 48. Отсюда следует, что на каждые 32 массовые части серы в этих соединениях приходится 32 и 48 массовых частей кислорода соответственно, т.е. а после сокращения в соответствии с математическими законами, соотношение массовых частей кислорода 32: 48 = 2: 3, что и является отношением небольших кратных чисел.
Закон кратных отношений является фактическим объединением закона сохранения массы и закона постоянства состава на базе атомной гипотезы строения вещества.
 2018-01-21
2018-01-21 943
943








