Растворение труднорастворимого электролита (ТРЭ) в количестве растворителя происходит до состояния насыщения.В насыщенном растворе электролит находится в динамическом равновесии с твердой фазой. Растворимость электролита определяет концентрацию ионов в насыщенном растворе электролита, значит его электропроводность. Чем меньше растворимость ТРЭ, тем он слабее.
При растворении электролита, например, соли, в раствор переходят не молекулы, а ионы. В этом случае в насыщенном растворе равновесие устанавливается между ионами соли в кристаллической фазе и ионами, перешедшими в раствор: СаСО3 кр ↔ Ca2+р-р + СО32-р-р.
Константа равновесия этого процесса:
Крав. = [Ca2+] • [СО32-]
[СаСО3кр]
 | Поскольку абсолютно нерастворимых веществ нет, какая - то часть AgCl перейдёт в раствор. Поскольку AgCl - сильный электролит, все молекулы, перешедшие в раствор, диссоциируют на ионы, и в растворе будут находится ионы. |
Любой раствор может быть насыщенным, ненасыщенным и перенасыщенным.
Ненасыщенным называют раствор, в котором при данной температуре можно растворить ещё какое - то количество данного вещества.
Насыщенным называют раствор, в котором скорость реакции растворения равна скорости реакции осаждения.
Концентрация насыщенного раствора для данного вещества при данной температуре есть величина постоянная, следовательно, в насыщенном растворе концентрации ионов данного электролита являются константами.
Перенасыщенными называют растворы, которые содержат осадок.
Насыщенные растворы трудно растворимых электролитов характеризуется величиной, называемой произведением растворимости.
AB - трудно растворимый электролит
AB=A++B-
ПРАВ = [A+]*[B-] - насыщенный раствор,
ПРАВ > [A+]*[B-] - ненасыщенный раствор,
ПРАВ < [Ag+]*[B-] - перенасыщенный раствор.
Be(OH)3  Bi3++3OH-
Bi3++3OH-
ПРBi(OH)3 = [Bi3+]*[OH--]3.
Добавление в раствор одноимённых ионов труднорастворимого электролита способствует выпадению в осадок иона противоположного знака
PbSO4 = Pb2+ + SO42-
ПРPbSO4 = [Pb2+]*[ SO42-] = 2,2*10-1
Na2SO4 = 2Na+ + SO42-
[Pb2+] 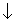 .
.
У словием образования осадка является превышение произведения концентраций ионов (ПК) малорастворимого электролита над его произведением растворимости, т.е. ПК > ПР.
При увеличении концентрации одного из ионов ТРЭ в его насыщенном растворе (например, путем введения хорошо растворимого электролита, содержащего тот же ион) произведение концентраций ионов электролита (ПК) становится больше ПР. При этом равновесие между твердой фазой и раствором смещается в сторону образования осадка. Например, если в насыщенный раствор Ag CI добавить сильный электролит K CI, то появление в растворе одноименного иона (CI -) приводит к смещению равновесия в сторону образования осадка (←). Когда установится новое равновесие, то произведение концентраций (ПК) ионов электролита вновь становится равным ПР, но при этом в растворе появится осадок. В состоянии нового равновесия концентрация ионов Ag+ будет меньше, а концентрация ионов CI- больш е, чем было до добавления KCI. AgCI↓ <=> Ag+ + CI- + КCI <=> K+ + CI-.
По принципу Ле-Шаталье, если [CI-] ↑, то смещение равновесие произойдет в сторону образования осадка.
Напротив, если в насыщенном растворе электролита уменьшить концентрацию одного из ионов (например, связав его каким-либо другим ионом), произведение концентраций ионов будет меньше значения ПР, раствор станет ненасыщенным, и равновесие между раствором и осадком сместится в сторону растворения осадка (→). Сu(OH)2↓ <=> Cu+2 + 2OH- + HCI <=> H+ + CI-
При добавлении HCI происходит реакция H+ + OH- <=> H2O, при этом [OH-] ↓, смещение равновесия происходит в сторону продуктов диссоциации основания.
 2018-01-21
2018-01-21 12568
12568








