При повышении концентрации реагирующих веществ скорость реакции возрастает.
Основной постулат химической кинетики – закон действующих масс
w = 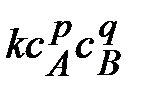
Скорость реакции пропорциональна произведению концентрации реагирующих веществ, взятых в некоторых степенях. Эти степени называются частными порядками реакции:
p - частный порядок реакции по веществу А,
q - частный порядок реакции по веществу В.
Сумма частных порядков дает полный порядок реакции n: n=p+q.
k - константа скорости реакции, это скорость реакции при концентрации реагирующих веществ, равных единице (удельная скорость ).
Константа скорости зависит от тех же факторов, что и скорость, но не зависит от концентрации веществ.
Зависимость скорости реакции от температуры. Правило Вант-Гоффа.
Скорость химической реакции увеличивается с повышением температуры. Приблизительно оценить влияние температуры на скорость реакции можно по правилу Вант-Гоффа:
при повышении температуры на каждые 10 градусов скорость реакции увеличивается в 2¸4 раза.
|
|
|
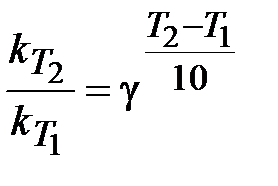 ,
,
где g - температурный коэффициент Вант-Гоффа.
k (T1) и k (T2) – константы скорости реакции при температурах Т1 и Т2 .
Для биологических процессов важен определенный температурный интервал, вне которого процесс прекращается. В этом интервале увеличение температуры активизирует протекание жизненно важных процессов до оптимального, а последующее повышение температуры быстро снижает скорость процесса вплоть до прекращения жизнедеятельности организма. Это связано с необратимой тепловой денатурацией белков биологических тканей, а также с инактивацией ферментов (биологических катализаторов).
 2018-01-21
2018-01-21 924
924








