Скорость реакции определяется числом элементарных актов взаимодействия происходящих в единицу времени в единице объема (для гомогенных реакций) или на единице поверхности раздела фаз (для гетерогенных реакций реакции). Скорость реакции обычно характеризуют изменением концентрации реагирующих веществ во времени. Концентрацию в растворе выражают в моль/л, в газах парциальным давлением, время в секундах. Изменение концентрации DС=С2-С1 за промежуток времени Dt=t2-t1 и определит скорость процесса.
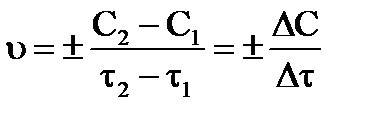
Знак «-» при уменьшении концентрации реагирующих веществ, знак «+» при увеличении концентрации продуктов реакции.
О скорости реакции можно судить по скорости изменения какого-либо свойства системы, например, окраски, электропроводности, спектра, давления, выпадения осадка, выделения газа и др.
Скорость процесса пропорциональна вероятности столкновения частиц, которая определяется их концентрацией.
Указанная закономерность установлена опытным путем в 1864-67гг К. Гульдбергом и П. Вааге, в 1865г Н.И. Бекетовым, является основным законом химической кинетики и называется законом действующих масс: при постоянной температуре скорость гомогенных химических реакций прямо пропорциональна произведению концентраций реагирующих веществ, возведенных в степень их стехиометрических коэффициентов.
Так для реакций
1) Н2+Cl2=2HCl,  ;
;
2) 2NO+O2=2NO2,  .
.
k – коэффициент пропорциональности или константа скорости, показывает какая часть от общей концентрации веществ реагирует в данных условиях, определяется природой веществ и изменяется с температурой.
Величина k численно равна скорости реакции, когда концентрации реагирующих веществ равны единице.
 2018-01-21
2018-01-21 1341
1341








