Относительная атомная масса
Атомы элементов характеризуются определённой (только им присущей) массой. Например, масса атома Н равна 1,67 . 10−23 г, атома С − 1,995 . 10−23 г, атома О − 2,66 . 10−23г.
Пользоваться такими малыми значениями неудобно, поэтому введено понятие об относительной атомной массе А r − отношении массы атома данного элемента к атомной единице массы (1,6605 . 10−24 г).
 Молекула - наименьшая частица вещества, сохраняющая химические свойства этого вещества. Все молекулы построены из атомов и поэтому также электронейтральны.
Молекула - наименьшая частица вещества, сохраняющая химические свойства этого вещества. Все молекулы построены из атомов и поэтому также электронейтральны.
Состав молекулы передаётся молекулярной формулой, которая отражает и качественный состав вещества (символы химических элементов, входящих в его молекулу), и его количественный состав (нижние числовые индексы, отвечающие числу атомов каждого элемента в молекуле).
Масса атомов и молекул
Для измерения масс атомов и молекул в физике и химии принята единая система измерения. Эти величины измеряются в относительных единицах.
Атомная единица массы (а.е.м.) равна 1/12 массы m атома углерода 12С (m одного атома 12С равна 1,993Ч10-26кг).
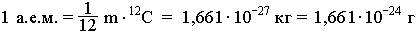
Относительная атомная масса элемента (Ar) – это безразмерная величина, равная отношению средней массы атома элемента к 1/12 массы атома 12С. При расчете относительной атомной массы учитывается изотопный состав элемента. Величины Ar определяют по таблице Д.И. Менделеева
Абсолютная масса атома (m) равна относительной атомной массе, умноженной на 1 а.е.м. Например, для атома водорода абсолютная масса определяется следующим образом:
m (H) = 1,008Ч1,661Ч10-27 кг = 1,674Ч10-27 кг
Относительная молекулярная масса соединения (M r) – это безразмерная величина, равная отношению массы m молекулы вещества к 1/12 массы атома 12С:
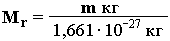
Относительная молекулярная масса равна сумме относительных масс атомов, входящих в состав молекулы. Например:
М r (C2H6) = 2Ч A r (C) + 6Ч A r (H) = 2Ч12 + 6 = 30.
Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на 1 а.е.м.
2. Что называется молярной массой эквивалента?
кон эквивалентов открыт Рихтером в 1791г. Атомы элементов взаимодействуют друг с другом в строго определенных соотношениях – эквивалентах.
В СИ эквивалент есть 1/z часть (воображаемая) частицы Х. Х – атом, молекула, ион и т.д. Z – равен числу протонов, которое связывает или отдает частица Х (эквивалент нейтрализации) или числу электронов, которое отдает или принимает частица Х (эквивалент окисления-восстановления) или заряду иона Х (ионный эквивалент).
Молярная масса эквивалента, размерность – г/моль, есть отношение молярной массы частицы Х к числу Z.
Например, молярная масса эквивалентаэлемента определяется отношением молярной массы элемента к его валентности.
в Н2О
в Аl2O3
Закон эквивалентов: массы реагирующих веществ относятся между собой, как молярные массы их эквивалентов.
Математическое выражение
где m1 и m2 – массы реагирующих веществ,
, - молярные массы их эквивалентов.
Если реагирующая порция вещества характеризуется не массой, а объемом V(x), то в выражении закона эквивалентов его молярная масса эквивалента заменяется молярным объемом эквивалента.
3. Каковы основные законы химии?
Основные законы химии. Закон сохранения массы и энергии сформулировал М. В. Ломоносов в 1748 году. Масса веществ участвующих в химических реакциях не изменяется. В 1905г Эйнштейн полагал, взаимосвязь между энергией и массой
Е=m×c2,, с=3×108м/с
Масса и энергия есть свойства материи. Масса – мера энергии. Энергия – мера движения, поэтому они не эквивалентны и не превращаются друг в друга, однако всякий раз, когда изменяется энергия тела Е, изменяется его масса m. Ощутимые изменения массы происходят в ядерной химии.
С точки зрения атомно-молекулярной теории атомы имеющие постоянную массу не исчезают и не возникают из ничего, это приводит к сохранению массы веществ. Закон доказан экспериментально. Опираясь на этот закон составляются химические уравнения. Количественные расчеты по уравнениям реакций называют стехиометрическими расчетами. В основе всех количественных расчетов лежит закон сохранения массы, и следовательно, можно планировать и контролировать производство.
4. Какие основные классы неорганических соединений существуют? Дайте определение, приведите примеры.
Простые вещества. Молекулы состоят из атомов одного вида (атомов одного элемента). В химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения). Молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.
| Неорганические вещества | |
| Простые | Металлы |
| Неметаллы | |
| Сложные | Оксиды |
| Основания | |
| Кислоты | |
| Соли |
Резкой границы между металлами и неметаллами нет, т.к. есть простые вещества, проявляющие двойственные свойства.
5. Каковы основные типы химических реакций?
Существует огромное множество различных химических реакций и несколько способов их классификации. Чаще всего химические реакции классифицируют по числу и составу реагентов и продуктов реакции. По этой классификации выделяют четыре типа химических реакций — это реакции соединения, разложения, замещения, обмена.
Реакция соединения — это реакция, реагентами которой являются два или несколько простых или сложных веществ, а продуктом — одно сложное вещество. Примеры реакций соединения:
Образование оксида из простых веществ — C + O2 = CO2, 2Mg + O2= 2MgO
Взаимодействие металла с неметаллом и получение соли — 2Fe + 3Cl2 = 2FeCl3
Взаимодействие оксида с водой — CaO + H2O = Ca(OH)2
Реакция разложения — это реакция, реагентом которой является одно сложное вещество, а продуктом — два или несколько простых или сложных веществ. Чаще всего реакции разложения протекают при нагревании. Примеры реакций разложения:
Разложение мела при нагревании: CaCO3 = CaO + CO2
Разложение воды под действием электрического тока: 2H2O = 2H2+ O2
Разложение оксида ртути при нагревании — 2HgO = 2Hg + O2
Реакция замещения — это реакция, реагентами которой являются простое и сложное вещества, а продуктами — также простое и сложное вещества, но атомы одного из элементов в сложном веществе заменены на атомы простого реагента. Примеры:
Замещение водорода в кислотах — Zn + H2SO4 = ZnSO4 + H2
Вытеснение металла из соли — Fe + CuSO4 = FeSO4 + Cu
Образование щелочи — 2Na + 2H2O = 2NaOH + H2
Реакция обмена — это реакция, реагентами и продуктами которой являются по два сложных вещества, в процессе реакции реагенты обмениваются между собой своими составными частями, в результате чего образуются другие сложные вещества. Примеры:
Взаимодействие соли с кислотой: FeS + 2HCl = FeCl2 + H2S
Взаимодействие двух солей: 2K3PO4 + 3MgSO4 = Mg3(PO4)2 + 3K2SO4
Существуют химические реакции, которые нельзя отнести ни к одному из перечисленных типов.
6. Кем, когда и какими опытами было открыто ядро атома и создана ядерная модель атома?
Ядерная модель атома. Одна из первых моделей строения атома былапредложена английским физиком Э. Резерфордом. В опытах по рассеянию а-частиц было показано, что почти вся масса атома сосредоточена в очень малом объеме — положительно заряженном ядре. Согласно моделиРезерфорда, вокруг ядра на относительно большом расстоянии непрерывно движутся электроны, причем их количество таково, что в целом атом электрически нейтрален. Позднее наличие в атоме тяжелогоядра, окруженного электронами, было подтверждено другими учеными. Первая попытка создания модели атома на основе накопленных экспериментальных данных (1903 г.) принадлежит Дж. Томсону. Он считал, что атом представляет собой электронейтральную систему шарообразной формы радиусом, примерно равным 10–10 м. Положительный заряд атома равномерно распределен по всему объему шара, а отрицательно заряженные электроны находятся внутри него (рис. 6.1.1). Для объяснения линейчатых спектров испускания атомов Томсон пытался определить расположение электронов в атоме и рассчитать частоты их колебаний около положений равновесия. Однако эти попытки не увенчались успехом. Через несколько лет в опытах великого английского физика Э. Резерфорда было доказано, что модель Томсона неверна.
| Рисунок 6.1.1. Модель атома Дж. Томсона |
7. Что нового ввел Н. Бор в представлении об атоме? Дайте краткое изложение постулатов Бора применительно к атому водорода.
Теория Бора для атома водорода
Следуя теории Бора для атома водорода, Зоммерфельд предложил такое правило квантования, что при его применении к атому водорода модель Бора не противоречит волновой природе электрона, постулированной де Бройлем. Вывести выражение для уровней энергии атома водорода, используя правило Зоммерфельда, согласно которому разрешенные электронные орбитали представляют собой окружности с длиной, кратной длине волны электрона.
Так как квантовые числа I, т и не вносят ничего в энергию электронного состояния, то все возможные состоянияв данном) радиальном уровне энергетически равны. Это значит, что в спектре будут наблюдаться только единичные линии, такие, как предсказывал Бор. Однако хорошо известно, что в спектре водородасуществует тонкая структура, изучение которой было толчком к развитию теории Бора — Зоммерфельда для атома водорода. Очевидно, что простая форма волнового уравнения не вполне адекватно описывает атом водорода, и, таким образом, мы находимся в-положении, лишь немного лучшем того, когда опирались на модель атома Бора.
8. Что определяют и какие значения могут иметь: главное квантовое число n, побочное (орбитальное) - l, магнитное - ml и спиновое - ms?
Квант овые числа.
1. Главное квантовое число, n – принимает целочисленные значения от 1 до ¥ (n=1 2 3 4 5 6 7…) или буквенные (K L M N O P Q).
max значение n соответствует числу энергетических уровней в атоме и соответствует номеру периода в таблице Д.И. Менделеева, характеризует величину энергии электрона, размер орбитали. Элемент с n=3 имеет 3 энергетических уровня, находится в третьем периоде, обладает большим размером электронного облака и энергией, чем элемент с n=1.
2. Орбитальное квантовое число l принимает значения в зависимости от главного квантового числа и имеет соответствующие буквенные значения.
l=0, 1, 2, 3… n-1
или s p d f
l – характеризует форму орбиталей:
Орбитали с одним и тем же значением n, но с разными значениями l различаются несколько по энергии т.е.уровни делятся на подуровни.
| Главное квантовое число n | Орбитальное квантовое число l | Буквенное обозначение подуровней | Число подуровней |
| s | |||
| s p | |||
| s p d | |||
| 0, 1, 2, 3 | s, p, d, f |
Число возможных подуровней равно главному квантовому числу.
3. Магнитное квантовое число ml принимает значения от -l,…0…, +l.
| Для s | l=0 | ml =0 |
| p | l=1 | ml =-1 0 +1 |
| d | l=2 | ml =-2 –1 0 +1 +2 |
| f | l=3 | ml =-3 –2 –1 0 +1 +2 +3 |
Число возможных значений магнитного квантового числа определяет число орбиталей данного вида. В пределах каждого уровня может быть только:
одна s – орбиталь, т.к. ml =0 при l=0
три р – орбитали, ml = -1 0 +1, при l=1
пять d – орбиталей ml =-2 –1 0 +1 +2, при l=2
семь f – орбиталей.
Магнитное квантовое число определяет ориентацию орбиталей в пространстве.
4. Спиновое квантовое число (спин), ms.
или
Спин характеризует магнитный момент электрона, обусловленный вращением электрона вокруг собственной оси по часовой и против часовой стрелки.
Обозначив электрон стрелкой , а орбиталь черточкой или клеточкой можно показать
,
Правила, характеризующие порядок заполнения орбиталей.
Принцип Паули: в атоме не может быть двух и более электронов с одинаковым набором всех четырех квантовых чисел. Из чего следует, что на одной орбитали могут находиться два электрона с противоположно направленными спинами.
Максимально возможное число электронов:
на s – подуровне - одна орбиталь – 2 электрона, т.е. s2;
на p- – -три орбитали – 6 электронов, т.е. р6;
на d - – - пять орбиталей – 10 электронов, т.е. d10;
на f- –– - семь орбиталей – 14 электронов, т.е. f14.
Число орбиталей на подуровнях определяется 2 l +1, а число электронов на них будет 2×(2 l +1),число орбиталей на подуровнях равно квадрату главного квантового числа n2, а на уровнях - 2n2, т.о. в первом периоде периодической системы элементов максимально может быть 2 элемента, во втором – 8, в третьем – 18 элементов, в четвертом – 32.
В соответствии с I и II правилами М.В.Клечковского заполнение орбиталей происходит в порядке возрастания суммы (n+l), при равенстве, с n – наименьшей.
Электронные формулы записываются следующим образом:
1. В виде числового коэффициента указывают номер энергетического уровня.
2. Приводят буквенные обозначения подуровня.
3. Число электронов на данном энергетическом подуровне указывают в виде показателя степени, при этом все электроны данного подуровня суммируются.
Размещение электронов в пределах данного подуровня подчиняется правилу Гунда: на данном подуровне электроны стремятся занять максимальное число свободных орбиталей, так, чтобы суммарный спин был максимальным.
9. Как объясняет теория Бора происхождение и линейчатую структуру атомных спектров?
Теория Н. Бора была предложена в 1913 году, в ней использовалась планетарная модель Резерфорда и квантовая теория Планка-Эйнштейна. Планк считал, что наряду с пределом делимости материи – атом, существует предел делимости энергии - квант. Атомы излучают энергию не непрерывно, а определенными порциями квантами
Е=h×V.
Первый постулат Н. Бора: существуют строго определенные разрешенные, так называемые стационарные орбиты; находясь на которых электрон не поглощает и не излучает энергию. Разрешенными являются только те орбиты, для которых момент количества движения равный произведению me×V×r, может меняться определенными порциями (квантами), т.е. квантуется.
Состояние атома с n=1 называют нормальным, при n=2,3… - возбужденным.
Скорость электрона с увеличением радиуса уменьшается, кинетическая и общая энергия возрастает.
Второй постулат Бора: при переходе с одной орбиты на другую электрон поглощает или излучает квант энергии.
Едальн-Еближ=h×V. Е=-21,76×10-19/n2Дж/атом=-1310кДж/моль.
Такую энергию надо затратить, чтобы перевести электрон в атоме водорода с первой боровской орбиты (n=1) на бесконечно удаленную, т.е. оторвать электрон от атома, превратив его в положительно заряженный ион.
Квантовая теория Бора объяснила линейчатый характер спектра атомов водорода.
Недостатки:
1. Постулируется пребывание электрона только на стационарных орбитах, как же в таком случае совершается переход электронов?
2. Не объясняются все детали спектров, их разная толщина.
3. Нельзя количественно рассчитать химическую связь.
10.
Что в атоме называют энергетическим уровнем и энергетическим подуровнем?
Число энергетических уровней атома равно номеру периода, в котором он расположен. Например,калий(К) -элемент четвертого периода, имеет 4 энергетических уровня (n = 4). Энергетический подуровень — совокупность орбиталей с одинаковыми значениями главного и орбитального квантовых чисел.
11. Какую форму имеют s-, p- и d- электронные облака.
При химических реакциях ядра атомов остаются без изменений, изменяется лишь строение электронных оболочек вследствие перераспределения электронов между атомами. Способностью атомов отдавать или присоединять электроны определяются его химические свойства.
Электрон имеет двойственную (корпускулярно-волновую) природу. Благодаря волновым свойствам электроны в атоме могут иметь только строго определенные значения энергии, которые зависят от расстояния до ядра. Электроны, обладающие близкими значениями энергии образуют энергетический уровень. Он содержит строго определенное число электронов - максимально 2n2. Энергетические уровни подразделяются на s-, p-, d- и f- подуровни; их число равно номеру уровня.
Состояние каждого электрона в атоме обычно описывают с помощью четырех квантовых чисел: главного (n), орбитального (l), магнитного (m) и спинового (s). Первые три характеризуют движение электрона в пространстве, а четвертое - вокруг собственной оси.
Главное квантовое число (n). Определяет энергетический уровень электрона, удаленность уровня от ядра, размер электронного облака. Принимает целые значения (n = 1, 2, 3...) и соответствует номеру периода. Из периодической системы для любого элемента по номеру периода можно определить число энергетических уровней атома и какой энергетический уровень является внешним.
Пример.
Элемент кадмий Cd расположен в пятом периоде, значит n = 5. В его атоме электроны раcпределены по пяти энергетическим уровням (n = 1, n = 2, n = 3, n = 4, n = 5); внешним будет пятый уровень (n = 5).
Орбитальное квантовое число (l) характеризует геометрическую форму орбитали. Принимает значение целых чисел от 0 до (n - 1). Независимо от номера энергетического уровня, каждому значению орбитального квантового числа соответствует орбиталь особой формы. Набор орбиталей с одинаковыми значениями n называется энергетическим уровнем, c одинаковыми n и l - подуровнем.
Для
l=0 s- подуровень, s- орбиталь – орбиталь сфера
l=1 p- подуровень, p- орбиталь – орбиталь гантель
l=2 d- подуровень, d- орбиталь – орбиталь сложной формы
f-подуровень, f-орбиталь – орбиталь еще более сложной формы
| S - орбиталь | Три p – орбитали |
| Пять d – орбиталей |
На первом энергетическом уровне (n = 1) орбитальное квантовое число lпринимает единственное значение l = (n - 1) = 0. Форма обитали - сферическая; на первом энергетическом только один подуровень - 1s. Для второго энергетического уровня (n = 2) орбитальное квантовое число может принимать два значения: l = 0, s- орбиталь - сфера большего размера, чем на первом энергетическом уровне; l = 1, p- орбиталь - гантель. Таким образом, на втором энергетическом уровне имеются два подуровня - 2s и 2p. Для третьего энергетического уровня (n = 3) орбитальное квантовое число l принимает три значения: l = 0, s- орбиталь - сфера большего размера, чем на втором энергетическом уровне; l = 1, p- орбиталь - гантель большего размера, чем на втором энергетическом уровне; l = 2, d- орбиталь сложной формы.
Таким образом, на третьем энергетическом уровне могут быть три энергетических подуровня - 3s, 3p и 3d.
12. Дайте формулировку принципа Паули и правила Гунда.
Принцип Паули: в атоме не может быть двух и более электронов с одинаковым набором всех четырех квантовых чисел. Из чего следует, что на одной орбитали могут находиться два электрона с противоположно направленными спинами.
Максимально возможное число электронов:
на s – подуровне - одна орбиталь – 2 электрона, т.е. s2;
на p- – -три орбитали – 6 электронов, т.е. р6;
на d - – - пять орбиталей – 10 электронов, т.е. d10;
на f- –– - семь орбиталей – 14 электронов, т.е. f14.
Число орбиталей на подуровнях определяется 2 l +1, а число электронов на них будет 2×(2 l +1),число орбиталей на подуровнях равно квадрату главного квантового числа n2, а на уровнях - 2n2, т.о. в первом периоде периодической системы элементов максимально может быть 2 элемента, во втором – 8, в третьем – 18 элементов, в четвертом – 32.
В соответствии с I и II правилами М.В.Клечковского заполнение орбиталей происходит в порядке возрастания суммы (n+l), при равенстве, с n – наименьшей.
Электронные формулы записываются следующим образом:
1. В виде числового коэффициента указывают номер энергетического уровня.
2. Приводят буквенные обозначения подуровня.
3. Число электронов на данном энергетическом подуровне указывают в виде показателя степени, при этом все электроны данного подуровня суммируются.
Размещение электронов в пределах данного подуровня подчиняется правилу Гунда: на данном подуровне электроны стремятся занять максимальное число свободных орбиталей, так, чтобы суммарный спин был максимальным.
13. Дайте формулировку правил Клечковского. Как они определяют порядок заполнения АО?
В соответствии с I и II правилами М.В.Клечковского заполнение орбиталей происходит в порядке возрастания суммы (n+l), при равенстве, с n – наименьшей.
Электронные формулы записываются следующим образом:
1. В виде числового коэффициента указывают номер энергетического уровня.
2. Приводят буквенные обозначения подуровня.
3. Число электронов на данном энергетическом подуровне указывают в виде показателя степени, при этом все электроны данного подуровня суммируются.
14. Что называют энергией ионизации, сродством к электрону, электроотрицательностью и в каких единицах они измеряются?
Атомные характеристики. Химическая природа элемента обуславливается способностью его атома терять или приобретать электроны. Эта способность количественно может быть оценена энергией ионизации атома и его сродством к электронам.
Энергией ионизации называется энергия, которую необходимо затратить для отрыва электрона от атома (иона или молекулы). Она выражается в джоулях или электронвольтах. 1 ЭВ = 1,6×10-19 Дж.
Энергия ионизации, I, является мерой восстановительной способности атома. Чем меньше I, тем больше восстановительная способность атома.
Наименьшими значениями I обладают s элементы первой группы. Значения же I2 для них резко возрастают. Аналогично для s элементов II группы резко возрастает I3.
Наибольшими значениями I1 обладают p-элементы VIII группы. Это возрастание энергии ионизации при переходе от s элементов I группы к p элементам VIII группы обуславливается возрастанием эффективного заряда ядра.
Сродством к электрону называется энергия, которая выделяется при присоединении электрона к атому (иону или молекуле). Выражается также в Дж или эВ. Можно сказать, что сродство к электрону – мера окислительной способности частиц. Надежные значения Е найдены лишь для небольшого числа элементов.
Наибольшим сродством к электрону обладают р-элементы VII группы (галогены), так как присоединяя один электрон к нейтральному атому они приобретают законченный октет электронов.
E(F) = 3,58 эВ, Е(Cl) = 3,76 эВ
Наименьшие и даже отрицательные значения Е имеют атомы с конфигурацией s2 и s2p6 или наполовину заполненным р-подуровнем.
Е(Mg) = -0,32 эВ, Е(Ne) = -0.57 эВ, Е(N) = 0,05 эВ
Присоединение последующих электронов невозможно. Так, многозарядные анионы О2-, N3- не существуют.
Электроотрицательностью называется количественная характеристика способности атома в молекуле притягивать к себе электроны. Эта способность зависит от I и Е. По Малликену: ЭО = (I+E)/2.
Электроотрицательности элементов по периоду возрастают, по группе – уменьшаются.
 2018-01-21
2018-01-21 11199
11199