Немногие химические реакции протекают в одном направлении, т.е. до полного превращения исходных веществ в продукты реакции. Например:
2КClO3® 2KCl+3O2
Большинство реакций обратимы. Уменьшение концентрации исходных веществ приводит к увеличению концентрации продуктов реакции, которые взаимодействуя между собой образуют исходные вещества. В обратимых реакциях знак = заменяется на  .
.
В состоянии равновесия прямая и обратная реакции не прекращаются. Поэтому такое равновесие называется подвижным или динамическим равновесием. И поскольку действие обеих реакций взаимно уничтожается,то в реагирующей смеси видимых изменений не происходит: концентрации всех реагирующих веществ — как исходных,так и образующихся — остаются строго постоянными. Концентрации реагирующих веществ,которые устанавливаются при химическом равновесии, называются равновесными.Они обычно обозначаются формулами реагирующих веществ, заключенными в квадратные скобки, например [Н2], [N2], [NH3],тогда как неравновесные концентрации обозначают так:
CH2, CN2, CNH3.
Смешение двух газов СО и NO2 идет с уменьшением окраски, затем прекращается вследствие сравнивания скорости прямой и обратной реакции, т.е. наступления химического равновесия.
NO2+CO  NO+CO2
NO+CO2
Скорость прямой реакции  .
.
Скорость обратной реакции 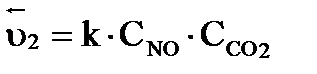 .
.
 2018-01-21
2018-01-21 1340
1340
