Зависимость скорости химической реакции от температуры описывается экспериментально найденным правилом Вант-Гоффа: при увеличении температуры на каждые 100С скорость реакции возрастает в 2-4 раза
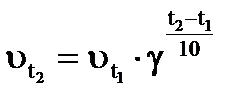
g - температурный коэффициент скорости реакции, значение которого лежит в пределах 2-4.
При значении g=2 и повышении температуры на 1000С, скорость химической реакции увеличивается в 1024 раза, т.к.
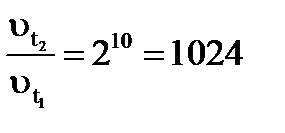
хотя число столкновений при этом возрастает в 1,2 раза.
Таким образом, при повышении температуры на каждые 100С число таких молекул возрастает в 2-4раза.
 2018-01-21
2018-01-21 721
721








