изменения по группам

Как видно из рисунка, р-элементы начинаются в периодической системе с 3-й группы. До них идут s-элементы.
Начинается заполнение электронами р-подуровня:
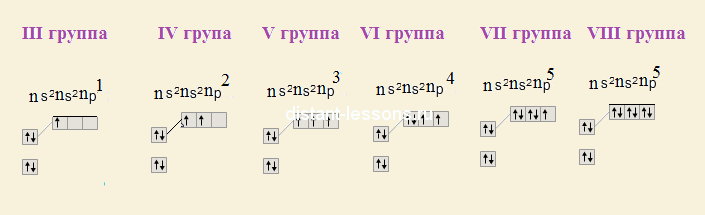
Как видите, идет последовательное заполнение электронами p-подуровня.
Давайте рассмотрим варианты валентности и степени окисления для элементов этих групп:
§ III группа (главная подгруппа) - 3 электрона на внешнем уровне - валентность элементов будет равна номеру группы - 3; степень окисления +3
§ IV группа - на внешнем уровне 4 электрона - максимальная валентность будет равна 4, 2 неспаренных электрона - есть еще валентность =2.
§ V группа - максимальная валентность - 5, еще возможна 3; степень окисления +5, +3 и -3
§ VI группа - максимальная валентность 6, еще возможна 4, 2; степень окисления: +6, +4, +2, -2.
§ VI группа - инертные газы... и этим все сказано.
Обратите внимание - слева на право по периодам количество электронов увеличивается (при этом радиус атома уменьшается) - для достижения стабильного состояния (завершенной 8-ми электронной оболочки) проще принять электроны, чем отдать, значит, НЕМЕТАЛЛИЧЕСКИЕ свойства усиливаются!

5 вопрос
В настоящее время периодическая система охватывает 117 элементов. Из них все трансурановые элементы (Z' = 93 — 117), а также элементы с Z = 43 (технеций), 61 (прометий), 85 (астат), 87 (франций) получены искусственно. За всю историю существования периодической системы было предложено большое количество (> 500) вариантов ее графического изображения, преимущественно в виде таблиц, а также в виде различных геометрических фигур (пространственных и плоскостных), аналитических кривых (спиралей и пр.) и т.д. Наибольшее распространение получили короткая, длинная и лестничная формы таблиц Менделеева.
В настоящее время предпочтение отдается короткой.
Фундаментальным принципом построения периодической системы является ее подразделение на группы и периоды. Менделеевское понятие рядов элементов ныне не употребляется, поскольку лишено физического смысла. Группы, в свою очередь, подразделяются на главную (а) и побочную (b) подгруппы. В каждой подгруппе содержатся элементы — химические аналоги. Элементы а- и b-подгрупп в большинстве групп также обнаруживают между собой определенное сходство, главным образом в высших степенях окисления, которые, как правило, равны номеру группы.
Периодом называется совокупность элементов, которая начинается щелочным металлом и заканчивается инертным газом (особый случай — первый период). Каждый период содержит строго определенное количество элементов. Периодическая система состоит из восьми групп и семи периодов, причем седьмой пока не завершен.
Особенность первого периода заключается в том, что он содержит всего 2 элемента: водород и гелий. Место водорода в системе неоднозначно. Поскольку он проявляет свойства, общие со щелочными металлами и с галогенами, то его помещают либо в I А-, либо в VII А-подгруппу, причем последний вариант употребляется чаще. Гелий-первый представитель VIII А-подгруппы. Долгое время гелий и все инертные газы выделяли в самостоятельную нулевую группу. Это положение потребовало пересмотра после синтеза химических соединений криптона, ксенона и радона. В результате инертные газы и элементы бывшей VIII группы (железо, кобальт, никель и платиновые металлы) были объединены в рамках одной группы. Этот вариант не безупречен, так как инертность гелия и неона не вызывает сомнений.
Второй период содержит 8 элементов. Он начинается щелочным металлом литием, единственная степень окисления которого + 1. Далее следует бериллий (металл, степень окисления + 2). Бор проявляет уже слабо выраженный металлический характер и является неметаллом (степень окисления + 3). Следующий за бором углерод — типичный неметалл, который проявляет степень окисления как +4, так и — 4. Азот, кислород, фтор и неон — все неметаллы, причем у азота высшая степень окисления + 5 соответствует номеру группы; для фтора известна степень окисления + 7. Инертный газ неон завершает период.
Третий период (натрий — аргон) также содержит 8 элементов. Характер изменения их свойств во многом аналогичен тому, который наблюдался для элементов второго периода. Но здесь есть и своя специфика. Так, магний в отличие от бериллия более металличен, так же как и алюминий по сравнению с бором. Кремний, фосфор, сера, хлор, аргон — все это типичные неметаллы. И все они, кроме аргона, проявляют высшие степени окисления, равные номеру группы.
Как видим, в обоих периодах по мере увеличения Z наблюдается ослабление металлических и усиление неметаллических свойств элементов. Д. И. Менделеев называл элементы второго и третьего периодов (по его словам, малых) типическими. Элементы малых периодов принадлежат к числу самых распространенных в природе. Углерод, азот и кислород (наряду с водородом) — органогены, т.е. основные элементы органической материи.
Все элементы первого — третьего периодов размещаются в А-подгруппах.
Четвертый период (калий — криптон) содержит 18 элементов. По Менделееву, это первый большой период. После щелочного металла калия и щелочноземельного металла кальция следует ряд элементов, состоящий из 10 так называемых переходных металлов (скандий — цинк). Все они входят в b-подгруппы. Большинство переходных металлов проявляют высшие степени окисления, равные номеру группы, кроме железа, кобальта и никеля. Элементы, начиная с галлия и кончая криптоном, принадлежат к А-подгруппам. Криптон в отличие от предшествующих инертных газов может образовывать химические соединения.
Пятый период (рубидий — ксенон) по своему построению аналогичен четвертому. В нем также содержится вставка из 10 переходных металлов (иттрий — кадмий). У элементов этого периода есть свои особенности. В триаде рутений — родий — палладий для рутения известны соединения, где он проявляет степень окисления +8. Все элементы А-подгрупп проявляют высшие степени окисления, равные номеру группы, исключая ксенон. Можно заметить, что особенности изменения свойств у элементов четвертого и пятого периодов по мере роста Z имеют по сравнению со вторым и третьим периодами более сложный характер.
Шестой период (цезий — радон) включает 32 элемента. В этом периоде кроме 10 переходных металлов (лантан, гафний — ртуть) содержится еще и совокупность из 14 лантаноидов — от церия до лютеция. Элементы от церия до лютеция химически очень похожи, и на этом основании их давно включают в семейство редкоземельных элементов. В короткой форме периодической системы ряд лантан видов включают в клетку лантана и расшифровку этого ряда дают внизу таблицы.
В чем состоит специфика элементов шестого периода? В триаде осмий — иридий — платина для осмия известна степень окисления +8. Астат имеет достаточно выраженный металлический характер. Радон, по всей вероятности, обладает наибольшей реакционной способностью из всех инертных газов. К сожалению, из-за того, что он сильно радиоактивен, его химия мало изучена).
Седьмой период начинается с франция. Подобно шестому, он также должен содержать 32 элемента, но из них пока известен 21. Фракций и радий соответственно являются элементами I а- и I I а-подгрупп, актиний принадлежит к III b-подгруппе. Дальнейшее построение седьмого периода спорно. Наиболее распространено представление о семействе актиноидов, которое включает элементы от тория до лоуренсия и аналогично лантаноидам. Расшифровка этого ряда элементов также дается внизу таблицы.
 2018-01-21
2018-01-21 750
750








