B гидросульфат тетрааминмеди
C сульфат аминмеди
D сульфат тетрааминмеди
E сульфат тетрааминмеди (І
73. Укажите какой комплексный ион будет наиболее устойчив,
если константа нестойкости комплексних ионов составляет:
A. 
B. 
C. 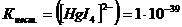
D. Нет ответа.
E. Нет однозначного ответа
74.Рассчитайте массу навески гидроксида натрия, необходимую для приготовления 1 л раствора с молярной концентрацией эквивалента 0,1 моль/л.
A. 4г.;
B. 40г.;
C. 0,4г;
D. 0,1.
E. 10г.
75. Укажите, случаи совпадения точки эквивалентности с точкой нейтрализации при титровании:
A. соляной кислоты раствором едкого натрия;
B. уксусной кислоты раствором едкого натрия;
C. муравьиной кислоты раствором едкого натрия.
D. соляной кислоты раствором аммиака
E. нет ответа
76.Укажите формулу для расчета титра стандартного раствора:
A. в/С
B. T = m /С;
C. T = С/m;
D. T = С/V.
E. Т = m/V;
77. Врач направил на анализ желудочный сок больного. В каких единицах измерения определяется кислотность желудочного:
A. рН;
B. ммоль/л;
C. титриметрических единицах;
D. электрон - вольт;
E. массовых долях
78. Что является мерой активной кислотности среды?
A рН
B Сa
C рКb
D Kдис.
E рКа
79. Для кислой среды значения рН и [Н+] соответственно равны:
A рН > 7; [ОН-] < 10-1
B рН = 7; [Н+] = 10-7
C рН < 7; [Н+] > 10-7
D рН › 7; [Н+] = [ОН-]
E рН > 7; [Н+] < 10-7
80. В каком из приведенных растворов водородный показатель равен нулю:
A в 1м НСl
B в 0,1 м КОН
C в 0, 1 м НСl
D в 1 м Н2SO4
E 1м КОН
81. Как рассчитать рН в растворе уксусной кислоты?
A. рН = 14 - lgC[H+]
B. pH = Ca
C. pH = -lg Cк-ты a;
D. pH = -lnCa
E. pH = -lgC[H+]
82. Сколько лигандов координируется вокруг комплексообразователя в гемоглобине?
A. 3
B. 4
C. 2
D. 5
E. 6
83.Сколько лигандов координируется вокруг комплексообразователя в цианокобаламине (Вит.В12)?
A. 3
B. 4
C. 2
D. 5
E. 6
84.Сколько лигандов координируется вокруг комплексообразователя в хлорофилле?
A. 2
B. 4
C. 1
D. 3
E. 5
85. Чему равно координационное число комплексообразователя в карбоангидразе?
A. 2
B. 6
C. 1
D. 4
E. 3
86. Какой из приведенных лигандов входит в состав оксигемоглобина?
A. O2
B. 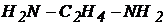 .
.
C. 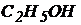
D. NH3
E. 
87. Какой из приведенных лигандов входит в состав гемоглобина?
A. Порфирин
B. Парафин
C. Пиррол
D. Пиридин
E. Имидазол
88. Какой из приведенных лигандов входит в состав хлорофилла?
A. Имидазол
B. Пиррол
C. Парафин
D. Пиридин
E. Порфирин
89. Какое из нарушений функционирования организма приводит к метаболическому алкалозу?:
A. Потеря протонов водорода вследствие кишечной непроходимости;
B. Гипервентиляция легких при лихорадочном состоянии и истерии;
C. Избыточное образование стойких кислот при голодание и рвоте;
D. Снижение вентиляции легких в следствии попадания инородного тела;
E. Нет ответа
90. рН желудочного сока равен 2. Какому значению активной кислотности в титриметрических единицах соответствует этот показатель?:
A. 10-15
B. 40-60
C. 50
D. 20-40
E. 45
91. Какое из нарушений функционирования организма приводит к метаболическому ацидозу?:
A. Избыточное образование стойких кислот при голодание и рвоте;
B. Потеря протонов водорода вследствие кишечной непроходимости;
C. Гипервентиляция легких при лихорадочном состоянии и истерии;
D. Снижение вентиляции легких в следствии попадания инородного тела;
E. Нет ответа
92. Какое из нарушений функционирования организма приводит к дыхательному (респираторному) ацидозу?:
A. Гипервентиляция легких при лихорадочном состоянии и истерии
B. Избыточное образование стойких кислот при голодание и рвоте;
C. Потеря протонов водорода вследствие кишечной непроходимости;
D. Снижение вентиляции легких в следствии попадания инородного тела;
E. Нет ответа
93. Какое утверждение верно?:
A. в цитохромах степень окисления железа изменяется от +3 до +2 и наоборот
B. в цитохромах степень окисления железа равна 0
C. в цитохромах степень окисления железа всегда равна +3
D. в цитохромах степень окисления железа всегда равна +2
E. в цитохромах степень окисления железа изменяется только от +3 до +2
94. рН раствора едкого натра равен 12. Чему равна его молярная концентрация?:
A. 0.01 моль/л
B. 0,1 моль/л
C. 1,0 моль/л
D. 0.02 моль/л
E. 0.2 моль/л
95.рН раствора соляной кислоты равен 2. Чему равна его молярная концентрация?:
A. 0,1 моль/л
B. 1,0 моль/л
C. 0.01 моль/л
D. 0.02 моль/л
E. 0.2 моль/л
96. Чему равно рН 0,01 М раствора едкого натра?:
A. 13
B. 1
C. 2
D. 12
E. 10
97. Чему равно рН 0,01 М раствора соляной кислоты?:
A. 2
B. 1
C. 3
D. 12
E. 13
98. Чему равна процентная концентрация раствора, в 500 граммах которого растворено 40 грамм едкого натра?:
A. 8%
B. 5%
C. 40%
D. 12%
E. 80%
99. Чему равна молярная концентрация раствора, в 500 мл которого растворено 0,5 моля едкого натра?:
A. 1 моль/л
B. 2 моль/л
C. 0,2 моль/л
D. 0,1 моль/л
E. 0,5 моль/л
100. Какое из соотношений верно для рассчитанных осмотических давлений 0,2% -ных растворов хлорида натрия и глюкозы?:
A. Р1 > Р2
B. Р1 = Р2
C. Р1 < Р2
D. Нужны дополнительные сведения
E. Нет ответа
 2018-01-21
2018-01-21 515
515







