Ковалентная связь – наиболее общий вид химической связи, возникающий за счет обобществления электронной пары посредством обменного механизма, когда каждый из взаимодействующих атомов поставляет по одному электрону, или по донорно-акцепторному механизму, если электронная пара передается в общее пользование одним атомом (донором) другому атому (акцептору) (рис. 3.2).
Классический пример неполярной ковалентной связи (разность электроотрицательностей равна нулю) наблюдается у гомоядерных молекул: H–H, F–F. Энергия двухэлектронной двухцентровой связи лежит в пределах 200–2000 кДж∙моль–1.
При образовании гетероатомной ковалентной связи электронная пара смещена к более электроотрицательному атому, что делает такую связь полярной. Ионность полярной связи в процентах вычисляется по эмпирическому соотношению 16(χA – χB) + 3,5(χA – χB)2, где χA и χB – электроотрицательности атомов А и В молекулы АВ. Кроме поляризуемости ковалентная связь обладает свойством насыщаемости – способностью атома образовывать столько ковалентных связей, сколько у него имеется энергетически доступных атомных орбиталей. О третьем свойстве ковалентной связи – направленности – речь пойдет ниже (см. метод валентных связей).
Ионная связь – частный случай ковалентной, когда образовавшаяся электронная пара полностью принадлежит более электроотрицательному атому, становящемуся анионом. Основой для выделения этой связи в отдельный тип служит то обстоятельство, что соединения с такой связью можно описывать в электростатическом приближении, считая ионную связь обусловленной притяжением положительных и отрицательных ионов. Взаимодействие ионов противоположного знака не зависит от направления, а кулоновские силы не обладают свойством насыщености. Поэтому каждый ион в ионном соединении притягивает такое число ионов противоположного знака, чтобы образовалась кристаллическая решетка ионного типа. В ионном кристалле нет молекул. Каждый ион окружен определенным числом ионов другого знака (координационное число иона). Ионные пары могут существовать в газообразном состоянии в виде полярных молекул. В газообразном состоянии NaCl имеет дипольный момент ~3∙10–29 Кл∙м, что соответствует смещению 0,8 заряда электрона на длину связи 0,236 нм от Na к Cl, т. е. Na0,8+Cl0,8–.
Металлическая связь возникает в результате частичной делокализации валентных электронов, которые достаточно свободно движутся в решетке металлов, электростатически взаимодействуя с положительно заряженными ионами. Силы связи не локализованы и не направлены, а делокализированные электроны обусловливают высокую тепло- и электропроводность.
Водородная связь. Ее образование обусловленно тем, что в результате сильного смещения электронной пары к электроотрицательному атому атом водорода, обладающий эффективным положительным зарядом, может взаимодействовать с другим электроотрицательным атомом (F, O, N, реже Cl, Br, S). Энергия такого электростатического взаимодействия составляет 20–100 кДж∙моль–1. Водородные связи могут быть внутри- и межмолекулярными. Внутримолекулярная водородная связь образуется, например, в ацетилацетоне и сопровождается замыканием цикла (рис. 3.3).
Молекулы карбоновых кислот в неполярных растворителях димеризуются за счет двух межмолекулярных водородных связей (рис. 3.4).
Исключительно важную роль водородная связь играет в биологических макромолекулах, таких неорганических соединениях как H2O, H2F2, NH3. За счет водородных связей вода характеризуется столь высокими по сравнению с H2Э (Э = S, Se, Te) температурами плавления и кипения. Если бы водородные связи отсутствовали, то вода плавилась бы при –100 °С, а кипела при –80 °С.
Ван-дер-ваальсова (межмолекулярная) связь – наиболее универсальный вид межмолекулярной связи, обусловлен дисперсионными силами (индуцированный диполь – индуцированный диполь), индукционным взаимодействием (постоянный диполь – индуцированный диполь) и ориентационным взаимодействием (постоянный диполь – постоянный диполь). Энергия ван-дер-ваальсовой связи меньше водородной и составляет 2–20 кДж∙моль–1.
Химическая связь в твердых телах. Свойства твердых веществ определяются природой частиц, занимающих узлы кристаллической решетки и типом взаимодействия между ними.
Твердые аргон и метан образуют атомные и молекулярные кристаллы соответственно. Поскольку силы между атомами и молекулами в этих решетках относятся к типу слабых ван-дер-ваальсовых, такие вещества плавятся при довольно низких температурах. Большая часть веществ, которые при комнатной температуре находятся в жидком и газообразном состоянии, при низких температурах образуют молекулярные кристаллы.
Температуры плавления ионных кристаллов выше, чем атомных и молекулярных, поскольку электростатические силы, действующие между ионами, намного превышают слабые ван-дер-ваальсовы силы. Ионные соединения более твердые и хрупкие. Такие кристаллы образуются элементами с сильно различающимися электроотрицательностями (например, галогениды щелочных металлов). Ионные кристаллы, содержащие многоатомные ионы, имеют более низкие температуры плавления; так для NaCl t пл. = 801 °C, а для NaNO3 t пл = 306,5 °C.
В ковалентных кристаллах решетка построена из атомов, соединенных ковалентной связью, поэтому эти кристаллы обладают высокими твердостью, температурой плавления и низкими тепло- и электропроводностью.
Кристаллические решетки, образуемые металлами, называются металлическими. В узлах таких решеток находятся положительные ионы металлов, в межузлиях – валентные электроны (электронный газ).
Наибольшую температуру плавления из металлов имеют d -элементы, что объясняется наличием в кристаллах этих элементов ковалентной связи, образованной неспаренными d -электронами, помимо металлической, образованнной s -электронами.
Вопрос
Гибридизация орбиталей – выравнивание энергии и формы орбиталей.
Суть процесса гибридизации атомных орбиталей состоит в том, что электрон вблизи ядра связанного атома характеризуется не отдельной атомной орбиталью, а комбинацией атомных орбиталей с одинаковым главным квантовым числом. Такая комбинация называется гибридной орбиталью. Гибридизация затрагивает лишь высшие и близкие по энергии атомные орбитали, занятые электронами.
Гибридные орбитали имеют асимметричную форму, вытянутую в сторону присоединяемого атома.
Вид гибридной атомной орбитали, образованной смешением s- и p- орбиталей.
Электронные облака взаимно отталкиваются и располагаются в пространстве максимально удалённом расстоянии друг от друга, что соответствует минимуму энергии межэлектронного отталкивания. При этом оси четырёх sр3-гибридных орбиталей оказываются направленными к вершинам тетраэдра (правильной треугольной пирамиды), а углы между этими орбиталями – тетраэдрические, равные 109°28'.
Тип гибридизации определяет геометрию молекулы или иона.
Типы гибридизации
| Тип гибридизации | Составляющие | Геометрическая форма | Угол между связями | Примеры |
| sp | 1 s- орбиталь и 1 p- орбиталь | линейная | 180o | BeCl2 |
| sp 2 | 1 s- орбиталь и 2 p- орбитали | треугольная | 120o | BCl3 |
| sp 3 | 1 s- орбиталь и 3 p- орбитали | тетраэдрическая | 109,5o | CH4 |
| sp 3 d | 1 s- орбиталь, 3 p- орбитали и 1 d- орбиталь | тригонально-бипирамидальная | 90o; 120o | PCl5 |
| sp 3 d 2 | 1 s- орбиталь, 3 p- орбитали и 2 d- орбитали | октаэдрическая | 90o | SF6 |
Вершины электронных орбиталей могут перекрываться друг с другом. Перекрытие электронных облаков по линии, проходящей через центры атомов, называют сигма (ϭ)-связью.
Ковалентная связь, образующаяся путем бокового перекрывания р -орбиталей соседних углеродных атомов, называется пи (π)-связью.
Вопрос
КРАТНЫЕ СВЯЗИ, хим. связи двухцентрового типа, к-рые в отличие от простой связи образованы более чем однойпарой электронов. По числу пар электронов, образующих кратные связи, различают двойные, тройные и четверные связи. В приближении молекулярных орбиталей методов кратные связи сопоставляются с мол. орбиталями, к-рые по св-вам симметрии делят на -, - и -орбитали. -Орбитали антисимметричны относительно плоскости, проходящей через связь. В многоатомных молекулах эта плоскость является общей для всей молекулы или для мол. фрагмента, включающего эту связь. -Орбитали антисимметричны относительно двух взаимно перпендикулярных плоскостей, проходящих через связь. При образовании кратных связей возникает, как правило, одна (или более) -орбиталь и обязательно хотя бы одна - или -орбиталь. По этой причине составляющие кратных связей, определяемые - или-орбиталями, наз. соотв. - или -связями. Атомы непереходных элементов в молекулах и ионах м. б. связаны простой, двойной и тройной связями. Образование простой -связи С—С в молекуле этана соотносят с перекрыванием двух sp3-гибридных орбиталей атомов углерода. В молекуле этилена кроме -связи С—С присутствует одна, а в молекуле ацетилена с тройной связью - две -связи:
Четверная связь (и м. б. связи более высокой кратности) характерна только для переходных металлов. -Перскрываниe ведет к образованию четверных связей в солях октагалогеиодиренат-аниона Re2Hal82-, карбоксилатахмолибдена и вольфрама M(OOCR)4, внутрикомплексных соед. хрома и ванадия М2А2, где А - 2,6-диметоксифенил.Энергетич. вклады, приходящиеся на связи разл. типов, неравноценны. Обычно энергия -связи составляет в среднем около 80% энергии -связи, а вклад -связи оценивается, напр., в солях октахлородиренат-аниона всего в 14% от полной энергии связи. Чем выше кратность связи, тем больше ее прочность (энергия диссоциации), короче межатомное расстояние и больше силовая постоянная связи.
Две или больше кратные связи могут образовывать в хим. соединении системы кумулированных и сопряженных связей. В первом случае две двойные связи примыкают к одному и тому же атому как, напр., в аллене Н2С=С=СН2; во втором - двойные или (и) тройные связи разделены одной простой, как, напр., в 1,3-бутадиене Н2С=СН—СН=СН2 илиакрилонитриле 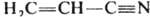 . В сопряженных системах кратность связи не м. б. определена целым числом. Мерой кратности связи (заселенности ее электронами) служит дробная величина порядка связи, расчет к-рой осуществляется обычно при помощи методов квантовой химии.
. В сопряженных системах кратность связи не м. б. определена целым числом. Мерой кратности связи (заселенности ее электронами) служит дробная величина порядка связи, расчет к-рой осуществляется обычно при помощи методов квантовой химии.
Вопрос
Водородная связь – связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженныматомом другой молекулы.
Механизм возникновения водородной связи – частично электростатический и частично донорно-акцепторный.
Характерной чертой водородной связи является расстояние между атомом водорода и другим атомом, её образующим. Оно должно быть меньше, чем сумма радиусов этих атомов.
Водородная связь подразделяется:
1. Межмолекулярная водородная связь образуется между молекулами веществ, в состав которых входят водород и сильно электроотрицательный элемент – фтор, кислород, азот, хлор, сера. Сильно смещенная общая электронная пара от водорода к атому отрицательно заряженного элемента, при этом положительный заряд водорода сконцентрирован в малом объеме, приводит взаимодействие протона с неподеленной электронной парой другого атома или иона, обобществляя её.
Водородную связь обозначают точками, указывая, что она намного слабее ковалентной связи (примерно в 15-20 раз).
2. Внутримолекулярная водородная связь присутствует в многоатомных спиртах, углеводах, белках и других органических веществах.
Вещества с водородной связь имеют молекулярные кристаллические решетки, в узлах которой находятся молекулы.
Примеры: вода в виде льда, йод, хлор, бром, «сухой лёд» (твердый диоксид углерода), твёрдый аммиак, а также твёрдые органические вещества (метан, бензол, фенол, нафталин, белки и т.д.).
 2018-01-21
2018-01-21 1944
1944
