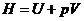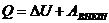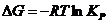1-й уровень
1. Для несамопроизвольных процессов в неизолированных системах:
а)DH < 0. б)DH > 0. в)DH = 0. г)DU < 0.
д)DU > 0. е)DG = 0. ж)DG < 0. з)DG > 0.
2. Для самопроизвольных процессов в неизолированных системах:
а)DU < 0. б)DU > 0. в)DH < 0. г)DH > 0.
д)DH = 0. е)DG = 0. ж)DG < 0. з)DG > 0.
3. Изменение энергии Гиббса при протекании химической реакции вычисляется по уравнению:
|
4. Формула для расчета изменения энтропии:
а) 
| б) 
| в) 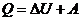
| г) 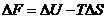
|
5. Самопроизвольные процессы для своего осуществления
а)требуют совершения работы. б)не требуют совершения работы.
в)сопровождаются выделением тепла. г)сопровождаются поглощением тепла.
д)стремятся к беспорядочному состоянию системы.
е)стремятся к упорядоченному состоянию системы.
2-й уровень
1. Самопроизвольные процессы в изолированной системе сопровождаются…
а)увеличением энтальпии. б)увеличением энтропии.
в)уменьшением энтропии. г)уменьшением объема.
2. Самопроизвольные процессы в неизолированной системе сопровождаются
а)уменьшением энергии Гибббса. б)увеличение энергии Гиббса.
в)уменьшением энтропии. г)уменьшением объема.
3. Неизолированная система находится в состоянии равновесия, если
а)энергия Гиббса уменьшается. б)энергия Гиббса возрастает.
в)энергия Гиббса не изменяется. г)совершается работа против внешних сил.
4. Энергия Гиббса является функцией состояния и ее изменение равно
а) сумме энергий Гиббса исходных веществ и конечных продуктов.
б) разности между суммой энергий Гиббса начальных веществ и суммой энергий Гиббса конечных веществ.
в) разности между суммой энергий Гиббса конечных веществ и суммой энергий Гиббса начальных веществ.
г) определяется способом проведения процесса.
5. Энтропия является функцией состояния и ее изменение равно
а) сумме энтропий исходных веществ и конечных продуктов.
б) разности между суммой энтропий начальных веществ и суммой энтропий веществ.
в) разности между суммой энтропий конечных веществ и суммой энтропий начальных веществ.
г) определяется способом проведения процесса.
3-й уровень
1. Энтропия при протекании реакции N2(Г) + O2(Г) " 2NO(Г).
а)увеличится. б)не изменится. в)равна нулю. г)уменьшится.
2. Соответствие между цифрами и словами
|
|

а)твердое. 1 б)жидкое 2. в)газообразное.3 г)ионное.
3. Энтропии при протекании реакции N2(Г) + 3H2(Г) " 2NH3(Г).
а)увеличится. б)не изменится. в)равна нулю. г)уменьшится.
4. Самопроизвольно в прямом направлении протекает реакция:
а) CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г); DG = 170,63 кДж.
б) Fe2O3(Т) + 3H2(Г) D 2Fe(Т) + 3H2(Г), DG = 55,28 кДж.
в) 4NH3(Г) + 5O2(Г) D 4NO(Г) + 6H2(Г), DG = -959,81 кДж.
г) H2(Г) + CO2(Г) D CO(Г) + H2(Ж), DG > 0.
5. Самопроизвольно в обратном направлении протекают реакции:
а) CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г); DG = 170,63 кДж.
б) Fe2O3(Т) + 3H2(Г) D 2Fe(Т) + 3H2O (Г), DG = 55,28 кДж.
в) 4NH3(Г) + 5O2(Г) D 4NO(Г) + 6H2(Г), DG = -959,81 кДж.
г) CO(Г) + Cl2(Г) D COCl2(Г), DG < 0.
6. Самопроизвольно в системе Fe2O3(Т) + 3H2(Г) D 2Fe(Т) + 3H2O (Г), DG = 55,28 кДж. будет протекать
а)прямая реакция. б)обратная реакция.
в)обе реакции равновероятны. г)химические изменения невозможны.
7. Реакция протекает самопроизвольно при
а)DGХР = -155,2 кДж/моль. б)DGХР = +155,2 кДж/моль.
в)DGХР = 0 кДж/моль. г)DGХР = -DHХР.
8. Энтропии в ходе реакции 2C4H10(Г) + 13O2(Г) " 8CO2(Г) + 10H2O(Г)
а)увеличится. б)уменьшится. в)не изменится. г)останется прежней.
9. Энтропия при протекании реакции 2C(Т) + 3H2(Г) " C2H6(Г)
а)увеличится. б)не изменится. в)равна нулю. г)уменьшится.
10. Энтропия при протекании реакции 3Fe(Т) + 2CO(Г) " Fe3C(Т) + CO2(Г)
а)уменьшится. б)увеличится. в)не изменится. г)равна нулю.
4-й уровень
1. Изменение энтропии реакции:
2C4H10(Г) + 13O2(Г) " 8CO2(Г) + 10H2O(Г), если SC4H10 = a, SO2 = b, SCO2 = c, SH2O = d,
а)DS = 2a - 13b + 8c - 10d. б)DS = 8c + 10d - a - 13b.
в)DS = 8c + 10d - 2a - 13b. г)DS = 2a + 13b - 8c - 10d.
 2018-01-21
2018-01-21 741
741