1. Массовая доля вещества в растворе вычисляется по формуле:
а) 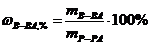 . б)
. б) 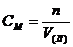 . в)
. в) 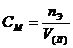 .
.
г) 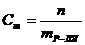 . д)
. д) 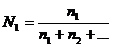 .
.
2. Молярная концентрация вещества в растворе вычисляется по формуле:
а) 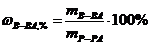 . б)
. б) 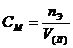 . в)
. в) 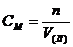 .
.
г) 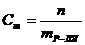 . д)
. д) 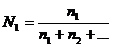 .
.
3. Нормальная концентрация вещества в растворе вычисляется по формуле:
а) 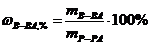 . б)
. б) 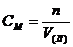 . в)
. в) 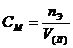 .
.
г) 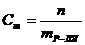 . д)
. д) 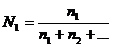 .
.
4. Моляльная концентрация вычисляется по формуле:
а) 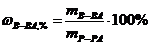 . б)
. б) 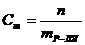 . в)
. в) 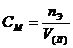 .
.
г) 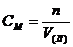 . д)
. д) 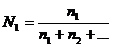 .
.
5. Мольная доля вещества вычисляется по формуле:
а) 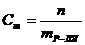 . б)
. б) 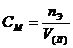 . в)
. в) 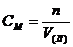 .
.
г) 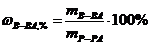 . д)
. д) 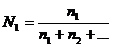 .
.
6. Растворами называют …
а) гетерогенные системы, состоящие из нескольких компонентов.
б) гомогенные системы, изолированные от окружающей среды.
в) гомогенные системы, состоящие из 2-х или более компонентов и продуктов их взаимодействия.
г) гомогенные системы, образующиеся в результате установления химического равновесия между 2-мя реагирующими веществами.
7. Концентрация - это количественная мера…
а) описания состава раствора.
б) содержания растворенных веществ в растворе.
в) содержания растворенного вещества в растворе.
г) описания способа приготовления раствора.
8. Гидратация - это взаимодействие растворенного вещества с…
а) любым растворителем.
б) водой.
в) другим веществом.
г) окружающей средой.
1. Осмосом называют процесс…
а) диффузии вещества при растворении.
б) самопроизвольного переноса вещества через полупроницаемую мембрану.
в) самопроизвольного переноса растворителя через полупроницаемую мембрану.
г) самопроизвольного перемешивания раствора.
2. Соответствие способа выражения концентрации и формул:
| а) | молярная концентрация | 1) | 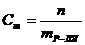
| |
| б) | нормальная концентрация | 2) | 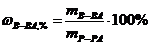
| |
| в) | массовая доля вещества | 3) | 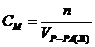
| |
| г) | мольная доля | 4) | 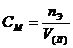
| |
| д) | моляльная концентрация | 5) | 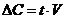
| |
| 6) | 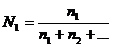
|
3. Закон Рауля: при постоянной температуре относительное понижение давления насыщенного пара растворителя над раствором равно … растворенного вещества.
а) массовой доле
б) молярной концентрации
в) моляльной концентрации
г) мольной доле.
4. Понижение температуры замерзания раствора прямопроцорционально… растворенного вещества.
а)массой доле б)молярной концентрации
в)моляльной концентрации г)мольной доле
5. Повышение температуры кипения вычисляется по формуле 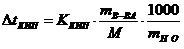 , где М
, где М
а) масса вещества
б) масса растворителя
в) молярная масса вещества
г) молярная масса растворителя
6. Температура замерзания раствора …
а) равна температуре замерзания растворителя.
б) выше температуры замерзания растворителя.
в) ниже температуры замерзания растворителя.
г) равна температуре замерзания растворенного вещества.
д) зависит от агрегатного состояния растворителя.
1. Соответствие между обозначением и его физическим смыслом в формуле закона Вант-Гоффа 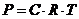 :
:
а) 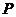
| 1) | атмосферное давление. | ||
б) 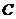
| 2) | осмотическое давление. | ||
в) 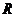
| 3) | универсальная газовая постоянная. | ||
г) 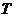
| 4) | молярная концентрация. | ||
| 5) | нормальная концентрация. | |||
| 6) | время измерений. | |||
| 7) | абсолютная температура. |
2. Соответствие между обозначением и его физическим смыслом в формуле 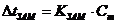 :
:
а) 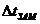
| 1) | понижение температуры замерзания. | ||
б) 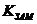
| 2) | температура замерзания. | ||
в) 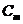
| 3) | повышение температуры замерзания. | ||
| 4) | моляльная концентрация. | |||
| 5) | молярная концентрация. | |||
| 6) | криоскопическая постоянная. |
3. Осмотическое давление зависит от ….
а)природы растворителя. б)температуры.
в)природы вещества. г)концентрации растворенного вещества.
в)объема раствора.
4. Зависимость растворимости газов от парциального давления




5. Соответствие между способом выражения концентрации вещества в растворе и размерностью:
| а) | Нормальная 5 | 1) | безразмерная. | |
| б) | Моляльная 6 | 2) | % массовые. | |
| в) | Молярная 4 | 3) | г/л. | |
| г) | массовая доля 3 | 4) | моль/л. | |
| д) | процентная концентрация | 5) | моль-экв/л. | |
| е) | мольная доля | 6) | моль/кг. | |
| 7) | %/кг. |
1. Количество гидроксида натрия, необходимого для приготовления 200 г 20%-ного раствора:
а)4 г. б)40 г. в)400 г. г)10 г.
2. Количество гидроксида натрия, необходимого для приготовления 3 л 10% -ного раствора плотностью 1,109 г/мл
а)500 г. б)500 мл. в)554,5 мл. г)554,5 г.
3. Количество азотной кислоты в 100 миллилитрах 0,2 М раствора (Молярная масса кислоты 63 г/моль)
а)1,26 г. б)20 г. в)0,1 г. г)63 г.
4. Раствор, содержащий в 300 мл 10,5 г КОН, имеет молярную концентрацию (молярная масса гидроксида калия 56 г/моль)…
а)0,625М. б)0,3М. в)0,105М. г)56М.
 2018-01-21
2018-01-21 630
630








