В предыдущих параграфах вы подробно познакомились с двумя типами связи: ионной и ковалентной. Вспомним, что ионная связь образуется при полной передаче электрона от одного атома другому. Ковалентная – при обобществлении неспаренных электронов связываемых атомов.
Кроме этого, существует еще один механизм образования связи. Рассмотрим его на примере взаимодействия молекулы аммиака с молекулой трифторида бора:

У атома азота в молекуле аммиака после образования связей с атомами водорода остается еще одна валентная орбиталь с неподеленной парой электронов (в структурной формуле обозначена точками). У атома бора в молекуле трифторида бора после образования связей с атомами фтора остается одна свободная валентная орбиталь (в структурной формуле обозначена •). Неподеленную пару валентных электронов атом азота может предоставить атому бора " в совместное использование", " поделиться" с ним этой электронной парой. При этом электроны бывшей неподеленной пары становятся общими для атомов азота и бора, то есть между ними образуется ковалентная связь. Но при этом у атомов бора и азота возникают еще и формальные заряды: – 1 е у атома бора и +1 е у атома азота:

В результате между атомами азота и бора возникает и ковалентная, и ионная связь. При этом атом азота является донором электронной пары (" дает" ее для образования связи), а атом бора – акцептором (" принимает" ее при образовании связи). Отсюда и название механизма образования такой связи – " донорно-акцепторный".
| Донорно-акцепторный механизм образования связи – механизм образования связи, при котором один из связываемых атомов является донором электронной пары, а другой – акцептором. |
При образовании связи по донорно-акцепторному механизму образуются одновременно и ковалентная связь, и ионная.
Конечно, после образования связи за счет разницы в электроотрицательности связываемых атомов происходит поляризация связи, возникают частичные заряды, снижающие эффективные (реальные) заряды атомов.

Рассмотрим другие примеры.
Если рядом с молекулой аммиака окажется сильно полярная молекула хлороводорода, в которой на атоме водорода имеется значительный частичный заряд 
 , то в этом случае роль акцептора электронной пары будет выполнять атом водорода. Его 1 s -АО хоть и не совсем пустая, как у атома бора в предыдущем примере, но электронная плотность в облаке этой орбитали существенно понижена.
, то в этом случае роль акцептора электронной пары будет выполнять атом водорода. Его 1 s -АО хоть и не совсем пустая, как у атома бора в предыдущем примере, но электронная плотность в облаке этой орбитали существенно понижена.

Пространственное строение получившегося катиона, иона аммония NH4  , подобно строению молекулы метана, то есть все четыре связи N—H совершенно одинаковы.
, подобно строению молекулы метана, то есть все четыре связи N—H совершенно одинаковы.
Образование ионных кристаллов хлорида аммония NH4Cl можно наблюдать, смешав газообразный аммиак с газообразным хлороводородом:
NH3(г)+ HCl(г) = NH4Cl(кр)
Донором электронной пары может быть не только атом азота. Им может быть, например, атом кислорода молекулы воды. С тем же хлороводородом молекула воды будет взаимодействовать следующим образом:
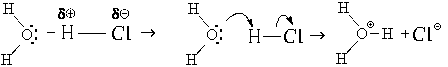
Образующийся катион H3O  называется ионом оксония и, как вы скоро узнаете, имеет огромное значение в химии.
называется ионом оксония и, как вы скоро узнаете, имеет огромное значение в химии.
В заключение рассмотрим электронное строение молекулы угарного газа (монооксида углерода) СО:

В ней, кроме трех ковалентных связей (тройной связи), есть еще и ионная связь.
Условия образования связи по донорно-акцепторному механизму:
1) наличие у одного из атомов неподеленной пары валентных электронов;
2) наличие у другого атома свободной орбитали на валентном подуровне.
Донорно-акцепторный механизм образования связи распространен довольно широко. Особенно часто он встречается при образовании соединений d -элементов. Атомы почти всех d -элементов имеют много свободных валентных орбиталей. Поэтому они являются активными акцепторами электронных пар.
 ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ ОБРАЗОВАНИЯ СВЯЗИ, ИОН АММОНИЯ, ИОН ОКСОНИЯ, УСЛОВИЯ ОБРАЗОВАНИЯ СВЯЗИ ПО ДОНОРНО-АКЦЕПТОРНОМУ МЕХАНИЗМУ.
ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ ОБРАЗОВАНИЯ СВЯЗИ, ИОН АММОНИЯ, ИОН ОКСОНИЯ, УСЛОВИЯ ОБРАЗОВАНИЯ СВЯЗИ ПО ДОНОРНО-АКЦЕПТОРНОМУ МЕХАНИЗМУ.
 1.Составьте уравнения реакций и схемы образования
1.Составьте уравнения реакций и схемы образования
а) бромида аммония NH4Br из аммиака и бромоводорода;
б) сульфата аммония (NH4)2SO4 из аммиака и серной кислоты.
2.Составьте уравнения реакций и схемы взаимодействия а) воды с бромоводородом; б) воды с серной кислотой.
3.Какие атомы в четырех предыдущих реакциях являются донорами электронной пары, а какие акцепторами? Почему? Ответ поясните диаграммами валентных подуровней.
4.Структурная формула азотной кислоты  Углы между связями O– N– O близки к 120o. Определите:
Углы между связями O– N– O близки к 120o. Определите:
а) тип гибридизации атома азота;
б) какая АО атома азота принимает участие в образовании  -связи;
-связи;
в) какая АО атома азота принимает участие в образовании  -связи по донорно-акцепторному механизму.
-связи по донорно-акцепторному механизму.
Как вы думаете, чему примерно равен угол между связями H– O– N в этой молекуле? 5.Составьте структурную формулу цианид-иона CN  (отрицательный заряд – на атоме углерода). Известно, что цианиды (соединения, содержащие такой ион) и угарный газ СО – сильные яды, и биологическое действие их очень близко. Предложите свое объяснение близости их биологического действия.
(отрицательный заряд – на атоме углерода). Известно, что цианиды (соединения, содержащие такой ион) и угарный газ СО – сильные яды, и биологическое действие их очень близко. Предложите свое объяснение близости их биологического действия.
Билет 9.
 2018-01-21
2018-01-21 3076
3076
