Концентрация соли. Поскольку гидролиз — процесс обратимый, то добавление воды в раствор будет способствовать смещению этой равновесной реакции вправо, т. е. разбавление соли усиливает ее гидролиз.
Температура. Все реакции нейтрализации идут с выделением теплоты. Следовательно, гидролиз — процесс эндотермический:
соль + вода = продукты гидролиза — Q.
Согласно принципу Ле-Шателье повышение температуры для таких процессов способствует смещению равновесия вправо, т. е. усиливает гидролиз соли.
Влияние кислот и оснований. Процессы гидролиза солей сопровождаются выделением ионов Н+ или ОН–. Поэтому добавление кислоты к раствору соли, гидролиз которой проходит по катиону, т. е. с образованием ионов Н+, смещает равновесие обратимого процесса влево, процесс гидролиза подавляется. Добавление к этому же раствору щелочи, наоборот, приводит к смещению равновесия вправо, так как ионы ОН– будут связывать ионы Н+ в молекулы воды, т. е. гидролиз усилится.
Вопрос 44.
Комплексные соединения — частицы (нейтральные молекулы или ионы), которые образуются в результате присоединения к данному иону (или атому), называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами. Теория комплексных соединений (координационная теория) была предложена в 1893 г. А. Вернером.
Комплексные соединения мало диссоциируют в растворе (в отличие от двойных солей). Комплексные соединения могут содержать комплексный малодиссоциирующий анион ([Fe(CN)6]3−), комплексный катион ([Ag(NH3)2]+), либо вообще не диссоциировать на ионы (соединения типа неэлектролитов, например карбонилы металлов). Комплексные соединения разнообразны и многочисленны.
Комплексообразователь (центральный ион)-
центральный атом комплексной частицы. Обычно комплексообразователь — атом элемента, образующего металл, но это может быть и атом кислорода, азота, серы, йода и других элементов, образующих неметаллы. Комплексообразователь обычно положительно заряжен и в таком случае именуется в современной научной литературе металлоцентром; заряд комплексообразователя может быть также отрицательным или равным нулю.
Лиганды — атомы или изолированные группы атомов, располагающиеся вокруг комплексообразователя образуют внутреннюю координационную сферу. Лигандами могут быть частицы, до образования комплексного соединения представлявшие собой молекулы (H2O, CO, NH3 и др.), анионы (OH−, Cl−, PO43− и др.), а также катион водорода H+.
Число лигандов, окружающих центральный ион называется координационным числом.
Номенкулатура:
CO- - карбонил С2O4 – оксалато
H2O – аква S2O3 - тиусульфато
NH-3 – аммин SO4 - сульфато
Сl- - хлоро
Br- - бромо
F- - фторо
I- - йодо
OH- - гидроксо
NO2- - нитро
CN- - циано
При названии комплексного аниона используется латинское название комплескообразователя в родительном падеже с указанием его валентности:
[Fe3+(H2O]04SO42-]+Cl- - хлоридсульфатотетрааква железа(III)
К2[Zn2+Cl4-]2- - тетрахлороцинкат (II) калия
Вопрос 45.
Комплексные ионы тоже могут диссоциировать в растворе. Например:
[CoCl4]2- Û Co2++4Cl-.
Устойчивость Комплексные соединения в растворе определяется константой диссоциации К его комплексного иона:
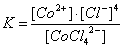 .
.
(При записи константы диссоциации в квадратные скобки берут равновесные концентрации ионов). Константа диссоциации характеризует термодинамическую устойчивость комплекса, зависящую от энергии связи между центральным атомом и лигандом. Различают также кинетическую устойчивость, или инертность, комплексной группировки — неспособность комплексного иона быстро обменивать внутрисферные ионы или молекулы на другие адденды. Например, [Fe (H2O)6]3+ и [Сr (H2O)6]3+ имеют почти одинаковые энергии связи Me — H2O (116 и 122 ккал/моль), но первый комплекс обменивает лиганды быстро, а второй (инертный) — медленно. Комплексные ионы тоже могут диссоциировать в растворе. Например:
[CoCl4]2- Û Co2++4Cl-.
Устойчивость Комплексные соединения в растворе определяется константой диссоциации К его комплексного иона:
(При записи константы диссоциации в квадратные скобки берут равновесные концентрации ионов). Константа диссоциации характеризует термодинамическую устойчивость комплекса, зависящую от энергии связи между центральным атомом и лигандом. Различают также кинетическую устойчивость, или инертность, комплексной группировки — неспособность комплексного иона быстро обменивать внутрисферные ионы или молекулы на другие адденды. Например, [Fe (H2O)6]3+ и [Сr (H2O)6]3+ имеют почти одинаковые энергии связи Me — H2O (116 и 122 ккал/моль), но первый комплекс обменивает лиганды быстро, а второй (инертный) — медленно.
Вопрос 46.
В основе метода валентных связей лежит идея донорно-акцепторного механизма образования связей между комплексообразователем (акцептор) и легандами (донор). (посмотреть в тетради.)
 2018-01-21
2018-01-21 1257
1257
