У азота нет возможности перехода электронов в возбужденное состояние, так как ближайшие орбитали при n = 3 слишком высоки по энергии.
Поэтому максимальная валентность азота равна четырем. Азот проявляет большое разнообразие степеней окисления: -3, -2, -1, 0, +1, +2, +3, +4 и +5. Наиболее часто встречаются степени окисления -3,+5 и +3 (NH3, HNO3 и NaNO2).
Переход атома в возбужденное состояние происходит при облучении или нагревании вещества. Состояние которое требует для повышения энергии электрона наименьших энергетически затрат называют первым возбужденным состоянием.
Возбужденное состояние атома является неустойчивым и через некоторое время электрон теряет энергию, перейдя на энергетическую орбиталь с меньшей энергией.
Азот может иметь степени окисления: 5, 4, 3, 2, -3
Фосфор может иметь степени окисления: 5, 3, -3
Билет 5 Сравните строение атомов Кислорода (Оксигену) и Серы (Сульфуру) объясните степени окисления, что они выявляют (возбужденное состояние атома)
Кислород 8O и Сера 16S элементы шестой группы, основной подгруппы.
Строение электронной оболочки этих атомов схоже, оба на последнем энергетическом уровне содержат по 6 электронов, но из них только 2 неспаренных.
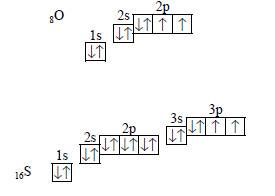
Кислород во втором периоде – т.е. 2 энергетичских уровня.
У кислорода возможность распаривания отсутствует, поэтому у него только 2 неспаренных электрона и атом кислорода может образовать 2 связи.
Кислород имеет постоянную валентность 2 и проявляет степень окисления +2.
Сера в третьем периоде – т.е. 3 энергетических уровня.
Однако, в атоме серы на внешнем электронном уровне есть еще пустые 3d-орбитали, на которые могут переходить электроны с 3s- и 3р-орбиталей, в результате в атоме серы становится шесть неспаренных электронов
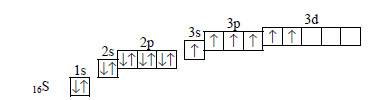
Получается, что сера может образовать 4 и 6 связей (по числу неспаренных электронов).
Возможные степени окисления серы -2, 0, +4,+6
Сера может проявлять валентности 2, 4, 6 (2 в простом веществе, сероводороде и сульфидах, где сера имеет степень окисления -2 )
 2018-01-21
2018-01-21 1896
1896
