Исследуем зависимость изохорной и изобарной теплоёмкости реальных и идеальных газов от величины температуры:
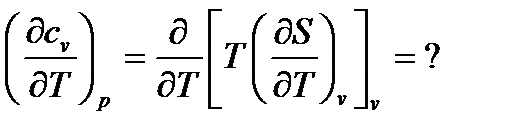
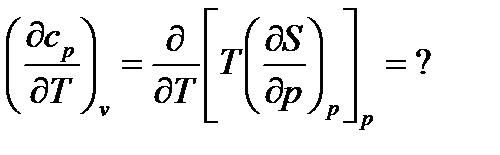
Поменять порядок дифференцирования и применить затем дифференциальные соотношения термодинамики не удается, то есть термодинамика на этот вопрос не отвечает.
Вывод:з ависимость изохорной и изобарной теплоёмкости реальных и идеальных газов от температуры может быть установленатолько опытным путём, либо с помощью какой-либо физической теории.
Опытные значения зависимости теплоёмкости от температуры представляются в виде таблиц, графиков и эмпирических зависимостей. У большинства технических газов cv и cp возрастают с ростом температуры.
Из физики известно, что температура газа не связана колебательным движением атомов и молекул, а зависит от кинетической энергии их поступательного движения. Подводимая к газу теплота по мере роста температуры перераспределяется всё более и более в пользу колебательного движения и поэтому прирост температуры при одинаковом подводе теплоты замедляется.
| t |
| с0 |
| с |
| Рис.8. Зависимость теплоемкости от температуры. |
На рис.8 опытные данные обозначены в виде звездочек. Сплошная линия –это кривая, аппроксимирующаяопытные данные с использованием метода наименьших квадратов или других аналогичных математических методов.Аппроксимирующая кривая подчиняющаяся уравнению
c=c0 + at + bt2 + dt3 +…
Здесь: t- температурав градусах Цельсия; c0, a, b, d и т.д – эмпирические коэффициенты (коэффициенты, полученные опытным путем). В инженерных расчетах ограничиваются первыми двумя слагаемыми в правой части уравнения,то есть полагают зависимость теплоемкости от температуры линейной:
C=c0 + at
Вчастности:
| cv=c0v + at |
и
| cр=c0р + at |
Все ранее полученные формулыотносятся к истинной теплоемкости, то есть теплоемкости для конкретной (заданной) температуры
В практических расчётах часто требуется знать среднее значение теплоёмкостей в заданном интервале температур отt1 до t2.
Обозначение средней теплоемкости: 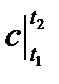 , или
, или 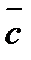 .
. 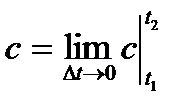 .
.
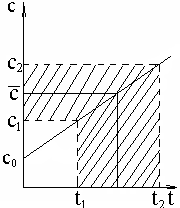 Средняя теплоемкость определяется каксредняя линия трапеции на рисунке:
Средняя теплоемкость определяется каксредняя линия трапеции на рисунке:
| рис.9.К |
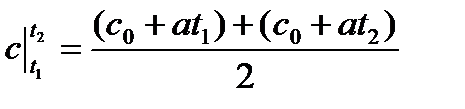
или окончательно
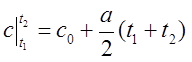
|
Рисунок.К определению средней теплоемкости
Конкретные значения эмпирических коэффициентов С0 и а содержатся в справочной литературе по теплофизическим характеристикам веществ.
В тех случаях, когда зависимость теплоёмкости от температуры не удаётся удовлетворительно аппроксимировать линейной зависимостью вида c=c0+at, то следует воспользоваться формулой для нелинейной зависимости:
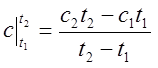
|
Для оценочных (не очень точных) расчетов, когда отсутствуют опытные данные для теплоемкости в виде таблиц или эмпирических формул, можно воспользоваться результатами молекулярно-кинетической теории газов, в которой п онятию идеального газа соответствуют одноатомные газы при малых давлениях
Из молекулярно-кинетической теории газов известно соотношение Um = 12,56T,КДж/кмоль.
Здесь Um - внутренняя энергия одного киломоля идеального газа, Т - абсолютная термодинамическая температура, К.
Для массовой изохорной теплоемкости идеального газа, ранее было получено: 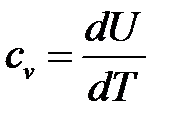 Молярнаяизохорная изобарную теплоемкость определяется аналогично:
Молярнаяизохорная изобарную теплоемкость определяется аналогично: 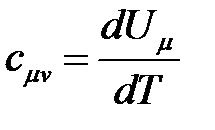
Подставляя в cmv значение Um = 12,56T получим
cmv =12,56, КДж/(кмоль*К)
Молярную изобарную теплоемкость сµp найдем из уравнения Майера:
cmp=cmv+Rm=12,56+8,314@ 20,93 КДж/(кмоль*К)
Как следует из полученных результатов, по молекулярно-кинетической теориигазов теплоемкости не зависят от температуры, то есть берутся средним значениеми во всем диапазоне температур. Именно в этом заключается оценочный характер этих значений.
На практике, чаще всего приходится иметь дело с двухатомными, трехатомными и болееатомными газами. Воздух считается в инженерных расчетах двухатомным газом,состоящим по объёмуна 79% из азота (N2) и на 21% из кислорода (O2).
Для оценочны х расчетов можно пользоваться следующей таблицей теплоемкостей идеальных газов:
| Газ | cmv, 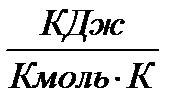
| cmp, 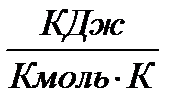
|
| Одноатомный | 12,56 | 20,93 |
| Двухатомный | 20,93 | 29,31 |
| Трех и более атомный | 29,31 | 37,68 |
В этой таблице, во второй и третьей строках теплоемкости скорректированы по результатам опытов.
У реальных газов, в отличие от идеального, теплоёмкости могут зависеть не только от температуры, но и от объёма и давления.
Вычисление энтропии.
Энтропию называют «тенью» внутренней энергии и она, также как U, является функцией состояния. Таким образом,dS – полный дифференциал энтропии.
Энтропию, как функцию состояния, для термодеформационной системы можно выразить через любое из трех сочетаний термодинамических параметров T, V, P:
S=S(T, V), S=S(T,P) иS=S(P,V)
и получить три группы равнозначных формул.
Первая группа формул для расчета удельной энтропии идеального газа (при S = S(T,V)):

|
Для практики наибольший интерес представляет не абсолютное значение S, а её изменение dS, для этого проинтегрируем уравнение:
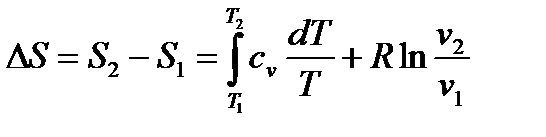
а) Пусть 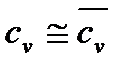 тогда
тогда
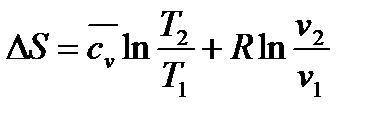 ,
, 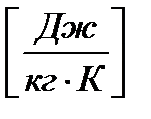 .
.
Из этой формулы, применимой для любого процесса идеального газа,
следуютдва частных случая:
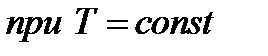
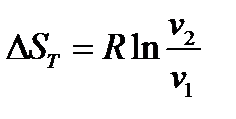
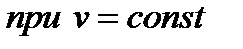
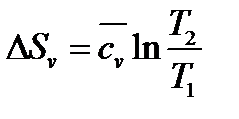
Энтропия – это мера неупорядоченности системы (чем больше энтропия, тем больше беспорядок).
При S = 0 должно отсутствовать не только макроскопическое, но и микроскопическое движение частиц, поэтому энтропия может быть равна нулю только при абсолютном нуле температур.
 2018-01-21
2018-01-21 1179
1179








