«Безлигандные» кластеры
Термин «кластер» происходит от английского слова cluster, означающего рой, гроздь, скопление. Введен в научный обиход американским физико-химиком Ф.Коттоном и в первоначальном своем смысле обозначал полиядерные металлорганические соединения, содержащие не менее трех атомов металла, расстояния между которыми допускают прямое валентное (химическое) взаимодействие, т.е. являются заметно меньшими суммы ковалентных радиусов и меньшими, чем в компактных металлах. С точки зрения этого определения понятия «кластер» моно- или биядерные частицы кластерами не являются, хотя из них последние и строятся.
В дальнейшем по мере проникновения этого термина в научную среду и, исходя из общего его смысла, слово «кластер» стало использоваться практически во всех разделах современного знания от естественных наук (например, в астрономии им обозначают скопление звезд и галактик) до гуманитарных (в социологии «кластером» обозначают социально однородную группу людей).
В современной химии понятие «кластер» обычно относят к трем видам объектов, связанных друг с другом взаимными превращениями (рис.). Это: 1- ультрадисперсные металлические порошки с размером частиц меньше 300 Å, т.е. имеющими размер, ставящих их в разряд наночастиц, и безлигандные кластеры; 2- молекулярные или ионные соединения металлов, стабилизированные органическими или неорганическими лигандами; 3- кластерные материалы. Несколько особняком в этой классификации располагается большая группа соединений, называемых обменными кластерами, в которых связь между атомами металла осуществляется через обменные взаимодействия различных типов, например через мостиковые лиганды. Однако помимо «обычного» использования это понятие сейчас уже не менее широко используется и для совершенно иных объектов химии, в том числе и не содержащих металлы и связанных не валентными взаимодействиями, например кластеры «воды», «бензола» и т.п., т.е. то, что еще совсем недавно обозначалось как «димеры», «тримеры», «ассоциаты» и т.д. При этом полностью игнорируется тот факт, что рассматриваемые «кластеры» являются не вполне устойчивыми образованиями. Но совсем недопустимы пассажи типа «Под кластерами понимают группу атомов или молекул, объединенных физическим взаимодействием в единый ансамбль, но сохраняющих внутри него индивидуальное поведение. Возможности прямого наблюдения кластеров ограничены, и поэтому экспериментаторы компенсируют аппаратурные недостатки интуицией и теоретическими построениями» (В.Белянин, Е. Романова, Наука и жизнь, 2004, №10). В этой цитате почти все неверно, начиная с того, что авторы понимают под физическим взаимодействием, и кончая трудностями изучения кластеров. Если под физическим взаимодействием понимается любой из известных типов вандерваальсова взаимодействия, то мы уже рассматривали с вами подобные объекты и отнесли их в раздел супрамолекулярной химии. Естественно, что в этом разделе могут быть размещены и кластеры в их понимании Коттоном.
Ультрадисперсное состояние вещества и металлов в частности, имеющих размер частиц менее 300 Å (<30 нм), занимает особое положение между индивидуально молекулой или атомом, с одной стороны, и веществом в компактном («обычном») состоянии, с другой. Его отличительными особенностями являются: 1-доля поверхностных атомов соизмерима с числом атомов внутренних; 2- соизмеримы и их энергии; 3-структура частицы отличается от структуры массивного вещества, например металла, часто отсутствует плотная упаковка, изменены расстояния и т.п.; 4- форма и структура носят ярко выраженный неравновесный характер, которые отвечают энергонасыщенным состояниям. Последнее обстоятельство может проявляться в значительном снижении т. пл., в выделении энергии в процессе хранения, причем в количествах достаточных для самопроизвольного спекания частиц или для их взаимодействия с матрицей, в которой они диспергированы, и т.д. При этом для УДЧ изменяются многие физико-химические и физические характеристики, такие как твердость, которая может достигать теоретических значений, увеличение вязкости и предела текучести, проводимость, магнитные свойства и т.д. Естественно, что все эти состояния неравновесны. В одних случаях это метастабильное состояние, в других кинетически заторможенное. Однако время релаксации для них сравнительно велико, локальное равновесие успевает установиться и, в ряде случаев, при описании таких систем применим термодинамический подход, но в более сложном варианте, поскольку требует учета дисперсности частицы, т.е. введения дополнительной координаты в обычно используемом в физико-химическом методе анализа описании «состав-свойство». Действительно, уже имеются работы, в которых показано, что алмаз в ультрадисперсном состоянии (до 40 Å) термодинамически более стабилен, чем графит такого же размера, и последний переходит в первый при довольно умеренных температурах и даже в вакууме. Хорошо известны исследования по синтезу поликристаллических алмазных пленок путем пиролиза ацетилен-водородных пламен при 800-900 0С и давлении меньше атмосферного, что существенно отличается от условий классического фазового перехода «графит-алмаз» в компактном материале. Совсем недавно в 2004 г. опубликована работа, согласно которой алмаз можно получить простым нагреванием изомера полиацетилена (СН)n с sp3-гибридизованными атомами углерода и синтезированного дебромированием бромоформа Na/K сплавом или вообще при взаимодействии двуокиси углерода или карбонатов с парами натрия при 600-700 0С. Неудивительно, что появились работы, в которых делается попытка пересмотра расчетов Лейпунского и на основании которых построена фазовая диаграмма углерода с одной стабильной фазой – графитом. Однако вряд ли это удастся сделать, поскольку имеется достаточно много убедительных доказательств метастабильности алмаза и последнее по времени из этих доказательств связано с изучением фазового перехода «графит-алмаз» in situ под давлением до 17 ГПа при комнатной температуре. В этой работе убедительно показано, что при снятии давления прозрачная алмазоподобная фаза, образующаяся из графита только за счет воздействия очень высокого давления, вновь достаточно быстро и на 100 % переходит в исходное состояние, т.е. в графит.
Из других примеров: обнаружен переход «металл«диэлектрик», возникающий с изменением размера частицы металла. Так, температура плавления золота в УД состоянии на 300-500 Со ниже, чем в компактном состоянии. Более того, в наносостоянии золото реагирует с СО2, давая окись и аморфный углерод!
На рис. 53 приводится зависимость изменения температуры плавления алюминия от размера частиц, а на рис. 54 зависимость доли поверхностных атомов алюминия от их
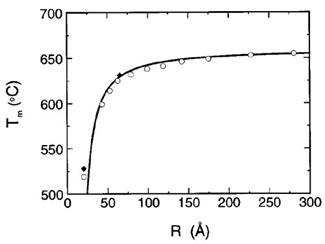
Рис. 53. Зависимость температуры плавления наночастиц алюминия Tm от их радиуса.
общего количества в некой произвольной единице объема.
В кубике из алюминия с ребром 1 см число поверхностных атомов будет равно 36.1014, а число внутренних атомов - 6.1022. Отсюда доля поверхностных атомов будет составлять 6.10-8. Если сделать такие же вычисления для кубика из алюминия размером 5 нм, то на его поверхности окажется уже 12% всех его атомов, а на поверхности кубика

Рис. 54. Зависимость «поверхностной» доли атомов (ось ординат) от кубического корня из их числа N в кубике кристаллического вещества.
размером 1 нм, вообще, больше половины всех атомов.
Появившееся в последнее время большое количество работ по нанокластерам углерода, начиная с фуллерена и кончая графеном, не перестают удивлять. Из последних достижений можно отметить определение теплопроводности графенового листа (рис. 55), которая оказалась равной 5300 Вт/м∙К против 3500 Вт/м∙К для одностенных нанотрубок и 2200 Вт/м∙К для алмаза, который еще совсем недавно считался чемпионом по этому показателю. Из подобных фактов, а их уже имеется достаточно много, можно сделать вывод, что размер частицы является активной переменной, определяющей вместе с другими термодинамическими функциями состояние системы, ее реакционную способность и даже физическую сущность. Условно размер частицы при проведении твердофазной реакции можно приравнять к эквиваленту температуры, и отсюда предположить
Рис. 55. Схематическое изображение подготовленного для эксперимента листа графена на подложке из кремния
возможность протекания для наночастиц реакций, которые в этих условиях никогда не наблюдаются для компактного вещества. Так, например, алюминий, диспергированный с применением методов механохимии в присутствии графита, реагирует с ним с образованием Al4C3 не при 1500 Со, а при 500-600 Со. В общем же размерные явления в химии выражаются в качественном изменении химических свойств и реакционной способности в зависимости от количества атомов или молекул в частице вещества и эта эволюция свойств, изучение мостов между единичной молекулой, атомом и макроскопическим миром вещества наиболее интересная составляющая в фундаментальных исследованиях наносостояния материи. Существуют экспериментальные попытки связать число атомов в частице, формы или способа ее организации с изменением химических и физических свойств и даже создать некое подобие Периодической таблицы, хотя для подобного обобщения явно не хватает материала и поэтому предлагаемые в литературе подходы следует признать преждевременными.
Из вышеприведенных рассуждений и примеров следует, что рассматривать наночастицы и производную от них - нанохимию как химию просто мелких частиц пусть даже, если их размер находится в нанодиапазоне, принципиально неверно, ибо помимо размера эти частицы должны обладать неким комплексом свойств, отличающим их от компактного или массивного вещества, материала, металла. Иными словами, подобное состояние вещества следует отнести к особому промежуточному состоянию - состоянию между отдельными атомами и твердым веществом с оригинальным набором свойств, отличающим его от последних двух. В соответствии с этим для этого состояния выработаны самостоятельные дефиниции.
Обычно к наночастицам относят гомо- или гетероатомные объекты с размером 1-10 нм, хотя в некоторых случаях они могут иметь и больший размер, но при этом должны обязательно проявлять свойства отличные от компактного вещества и молекулярных кластеров. Отсюда следует, что понятие УДЧ более широкое, поскольку включает частицы с размером от нескольких до сотен ангстрем. Наноструктура – совокупность наночастиц определенного размера, связанных друг с другом химическими или физическими силами. Нанокомпозиты – сложные объекты, состоящие из наночастиц и связующего, или двух и более типов наночастиц, или из них и связующего, но во всех случаях межчастичные взаимодействия в них становятся настолько сильными, что маскируют свойства изолированных частиц, т.е. весь объект приобретает новые свойства не типичные для составляющих его компонентов или фаз. При этом следует иметь ввиду, что и понятие фаза для веществ подобного размера выражено менее однозначно, поскольку граница между гомогенной и гетерогенной фазами становится размытой и определить ее строго количественными критериями невозможно. Более того, следует признать, что попытки проведения работ в этом направлении просто бесперспективны по всем параметрам. На сегодняшний день эта нижняя граница (верхняя – это один атом или одна молекула) скорее определяется здравым смыслом экспериментатора, чем некими строго сформулированными законами. Этот смысл базируется на двух понятиях наночастица и нанореактор. В чем их различие? Первое характеризует размерный параметр наночастицы, второе ее функциональную особенность или просто функцию.
Простейшие нанореакторы с пространственно организованными реагентами, находящиеся на верхней границе размеров – ван-дер-ваальсовы молекулы, т.е. образования слабосвязанных ионов, атомов, радикалов, молекул. В настоящее время известно огромное число таких молекул, например He·NH3, C2H4·Ar, Ar·I2, Al·N2 и др., которые являются надежным источником для определения атом-атомных потенциалов, ответственных за молекулярную организацию кристаллов, саморепликацию биомолекул и самоорганизацию супрамолекулярных ансамблей и определяющих макросвойства газов, фазовые переходы и многое другое. Более сложные образования, но также относящиеся к нанореакторам – это ансамбли из гостевых молекул, атомов, ионов, расположенных в полостях различной природы от “грубых” и малочувствительных к изменяющимся условиям молекул краун- эфиров до каликсаренов, карсеплексов или циклодекстринов, способных избирательно захватывать молекулы гостей и выпускать их на свободу при замене растворителя или изменении рН, совершенно необычные 1D-0D образования под названием пиподы – нанотрубки, заполненные молекулами фуллеренов от С36 до С82 или экзофуллеридов типа Ln@C82, которые могут давать внутри трубки одномерную полимерную цепочку или быть продопированы (в случае фуллеритов) атомами щелочных металлов. В этих удивительных образованиях гостевые молекулы не просто занимают некое геометрическое пространство, но ведут себя довольно «нахально» - крутятся, катаются, сталкиваются.
Цеолитовые пещеры и межслоевые пространства в графите, халькогенидах, глинах, и искусственно созданных двумерных графитоподобных нанореакторов на основе оксофосфатов с изменяемой геометрией межслоевого пространства за счет изменяемой длины гибкоцепных полиметиленовых мостиков, соединяющих слои, и их числа (рис. 56),

Рис. 56. Схема изменения геометрии межслоевого пространства и количества гостей в гибкоцепных слоевых структурах.
кристаллосольваты и клатраты, молекулы фуллерена с дефицитом 2 атомов на поверхности, что открывает доступ молекул-гостей внутрь сферы, и тому подобные еще совсем недавно немыслимые комбинации веществ - все это нанореакторы или наноконтейнеры, в которых происходят реакции невообразимые в макросостоянии, зачастую «навязанные» необычной геометрией ансамбля, изменениями в энергиях активации, механизмах и прочими аномалиями, связанными с наносостоянием взаимодействующих компонентов.
В случае, когда размер определяет функцию, понятия наночастица и нанореактор совпадают. Так, имеются данные, что кластер, содержащий ≤15 атомов железа, обладает обоими свойствами, а при большем числе он остается нанокластером, но теряет свойства нанореактора, т.е. по своим свойствам как бы приближается к металлическому железу. В ансамбле, образованном α-нафтолом и водой первый проявляет себя в обеих ипостасях только при n(Н2О)<20. При больших значениях n химические аномалии исчезают, α-нафтол диссоциирует по кислотному типу и протон присоединяется к воде. Следует все же отметить, что приведенные литературные примеры весьма эффектны и ими можно оперировать, но трудно согласиться. Хотя бы потому, что в кластере из 15 атомов железа только 2 или 3 атома являются внутренними, вся конструкция неравновесна и весьма затруднительно представить, о каком макрометаллическом состоянии здесь можно говорить. Об этой неопределенности говорят и найденные зависимости реакционной способности нанокомпонентов от числа атомов в них. Так, ион одновалентного магния Mg+ реагирует с водой с выделением водорода по реакции Mg+(H2O)n →(MgOH)+(H2O)n-1 + H только при 6≤n≤15. Означает ли это, что при n≤6 кластер воды приобретает макросвойства, в интервале значений 6-15 он становится нонореактором, а потом опять обычной водой? Вряд ли, тем более, что подобные нелинейные зависимости свойств кластеров от числа атомов далеко не единичны и скорее всего характеризуют лишь отношение к данному свойству, в случае кластеров воды - отношение к иону магния+1.
Высокая реакционная способность и микронеравновесность УДЧ делают совершенно неприемлемыми для их получения классические методы измельчения вещества, основанные на механическом диспергировании. К настоящему времени разработано несколько способов получения УДЧ, позволяющих реализовать сильно неравновесное состояние: 1-путем деформации, например при использования давления со сдвигом; 2- облучением твердого тела нейтронами или потоками заряженных частиц; 3- переохлаждением расплавов или наоборот – нагревом с последующей ударной закалкой; 4- разложением молекулярных кластеров, МОС, карбонилов, гидридов и других нестабильных веществ; 5- химическое восстановление солей металлов водородом или комплексными гидридами в растворителях различной природы; 6- фотовосстановление или восстановление жестким γ-излучением.
Наиболее удобный способ, который одновременно является и наиболее общим при получении УДЧ, основан на конденсации паров металла, получаемых самыми разнообразными методами. Непременным условием для их реализации должна являться только высокая скорость нуклеации, при минимальных скоростях агрегации атомов, приводящей к росту частиц. К этим методам относятся методы плазмохимического, термического, лазерного и т.п. испарения металлов, метод взрыва проводника при пропускании через него тока большой мощности. (Последний метод в исполнении «великих» московских физиков с благословения Московского правительства предлагается «использовать» для трансмутации элементов. Видимо бюрократов прельстила разрекламированная этими физиками «возможность» не вывозить отходы на свалку, а сразу на месте превращать их в золото.) Известно, что пары металлов на 99% состоят из атомов. При их совестной конденсации с большим избытком инертного газа на охлаждаемую до 70 К и ниже подложку происходит матричная изоляция отдельных атомов металла, которые при этом становятся доступными для изучения. Следует отметить, что этом метод матричной изоляции используется не только для фиксации атомов, но и отдельных молекул и достаточно широко применяется в спектроскопии. Но, к сожалению, даже в этих условиях происходит довольно интенсивная агрегация атомов. Так, атомарный ванадий существует в виде атомов при отношении концентраций V:Ar=1/104 и температуре ниже 12 К, а при 50 К он уже более чем наполовину агрегирован. Еще выше эти скорости для серебра. Помимо агрегации, если конденсация проведена в другие матрицы, происходит взаимодействие атомов с этими матрицами или просто тривиальное окисление. Так, совместная конденсация паров металла с алифатическими углеводородами или алканами приводит к крекингу последних даже при температурах жидкого азота и образованию МОС с связями М-С или М-Н. Именно поэтому говорить о нано технологиях, нано частицах на основе металлов и ряда других неорганических веществ, да и вообще о прочих вещах с приставкой нано, если, конечно, этот разговор идет в кругу ученых, а не в целях рекламы, следует очень осторожно. Еще нет ни одного примера сохранения металлических частиц атомных размеров in vitro – стоит только вынести их из камеры, поднять температуру, заменить инертный газ или вакуум на атмосферный воздух – большинство свойств, присущих именно наночастицам исчезают. Естественно, что наиболее активны все металлы, стоящие в ряду напряжений до водорода. Металлы, стоящие за ним, более устойчивы к процессам окисления, хотя в наносостоянии и они отнюдь не инертны, как в компактном виде. В то же время для УДЧ серебра установлена идентичность оптических свойств материала в вакууме и в среде аргона при низких температурах.
Химическая активность наночастиц может быть использована для синтеза труднодоступных веществ. Таким способом, например, были получены различные ареновые и циклопентадиенильные комплексы переходных металлов, в частности бис-пентаметилциклопентадиенилсамарий – первый представитель мономерных угловых сэндвичей, не содержащих, как и ферроцен, дополнительных лигандов у атома металла. Лишь только когда была показана реальность существования подобных соединений, были разработаны методы их химического синтеза, например по обменным реакциях. В то же время прошло более 30 лет с того момента, когда было обнаружено резкое увеличение проводимости в композите йодида лития с нанооксидом алюминия. Этот эффект используется в миллиардах микробатарей, например для кардиостимуляторов. Тем не менее, еще никто не смог еще дать химически-обоснованного ответа на простейший вопрос, почему гетерогенная смесь LiI и нанокристаллического Al2O3 проявляет столь высокую проводимость и рабочий ресурс? Мне кажется, что таких загадок нанохимия преподнесет еще очень и очень много.
Кластеры с числом атомов от 3 до 12, в которых каждый атом в плотной упаковке является поверхностным, называются малыми. Получение этих веществ направленным синтезом затруднено. Обычно агрегация моно- и биядерных частиц приводит к получению широкого спектра агрегатов различной нуклеарности. При этом, если n=3, то минимум потенциальной энергии на диаграмме Леннарда-Джонса и Морзе отвечает треугольной конфигурации атомов, при n=4 – тетраэдру, при n=5 тригональной бипирамиде, при n=6 бипирамиде с тетраэдром на одной грани, т.н. «шапка», n=7 пентагональной бипирамиде. Последующее присоединение атомов вплоть до n£13 может происходить по «шапочному» типу. Однако все это расчетные модели, а какова реальность, каково строение возможного изомера, реализующегося в том или ином случае, остается не установленным.
Частицы с числом атомов от 13 до 150 имеют размер 8-20 Å и характеризуются появлением в плотной упаковке внутренних атомов. При этом, если отношение внутренних и внешних атомов для n=13 равно 12 (один атом внутренний), то для n=150 приближается к 1. Эти кластеры относятся к средним и большим. Поскольку поверхностные атомы имеют меньше соседей, чем внутренние, нарушается равновесие и симметрия в распределении сил и масс, что приводит к изменению равновесных межатомных расстояний, к сдвиговым деформациям, образованию конфигураций с осями симметрии пятого порядка и икосаэдрической структурой, невозможными для компактного металла. Последнее понятно, так как при образовании этих конформаций атом металла приобретает к.ч.=5, в то время как в ГПУ и ГЦК решетках компактных металлах оно может быть равно только 4. При стабилизации таких кластеров органическими или карбонильными лигандами удалось выделить в индивидуальном состоянии и изучить методом РСтА не слишком большое число соединений, но уже исследованные, в целом подтверждают выводы о строении этих соединений, сделанные на основании общих соображений и модельных представлений. Так, известен скелетный кластерный анион состава [Ni38Pt6 (CO)48]4-, в котором октаэдр из атомов платины окружен 38 атомами никеля. Кластер состава [Cu140Se73(PPh3)30] не относится к скелетным. Он построен из фрагментов селенида одновалентной меди Сu2Se, окруженных фосфиновыми лигандами. Этот пример является уникальным, поскольку других примеров получения монокристаллов кластеров с таким числом атомов пригодных для структурного эксперимента в научной литературе неизвестно. Эта проблема типична для всех многоатомных соединений и до настоящего времени не имеет всеобъемлющего решения. Так, строение другого крупного кластера состава Au55(PPh3)12Cl6 определено только косвенными методами.
Кластеры с размером частиц от 20 до 100 Å называются гигантскими. В них число внутренних и внешних атомов соизмеримо. Считается, что именно к частицам подобного размера приложима приставка нано и они же наиболее интересны для материаловедения. Это объясняется тем, что именно для них наблюдается наибольшее количество аномалий в физических свойствах, именно эти вещества изучаются наиболее интенсивно и именно для них имеется наибольший массив информации (возможно, именно поэтому они и представляются наиболее интересными, чем все прочие кластеры).
Обычно эти вещества получают при нуклеации паров металлов на охлаждаемые поверхности или путем стабилизации в полимерных матрицах или различными лигандами, в качестве которых обычно выступают молекулы растворителя и которые почему-то зачастую не рассматриваются как лиганды.
Строение этих веществ исследовано крайне недостаточно. Известно, что формирование ядра кластера, как и формирование компактного металла, подчиняется правилам, сформулированным в рамках концепции плотной упаковки. Число атомов металлов в плотноупакованном ядре, построенном в виде правильного 12-вершинного многогранника (кубооктаэдра, икосаэдра, антикубооктаэдра) вычисляется по формуле
N=1/3(10n3+15n2+11n+3),
где n – число слоев вокруг центрального атома. Отсюда следует, что минимальное плотноупакованное ядро содержит 13 атомов (1 атом внутренний), затем 55, 147, 309, 561, 923, 1415, 2057, 2869 и т.д. Монослойные молекулярные кластеры, рассмотренные ниже, с 13 атомами металла, например [Rh13(CO)24H3]2- с ядром в виде кубооктаэдра, хорошо известны и многочисленны. С ростом числа атомов их может и не становится меньше, но существенно, затрудняется определение их состава и строения. Так, помимо уже упомянутого двухслойного Au55(PPh3)12Cl6 с размером ~14 Å известен ряд 55 атомных кластеров металлов платиновой подгруппы. В четырехслойном кластере Pt309Phen36O30±10 уже и состав определен с некоторой долей достоверности.
Совершенно уникальный случай связан с гигантским пятислойным кластером состава Pd560Phen60(OAc)180 и диаметром около 20 Å. Его удалось не только выделить в индивидуальном состоянии, но даже изучить его структуру, правда, учитывая вышесказанное, только косвенными методами, но достоверность предложенной структуры весьма велика. Атомы палладия в нем кристаллизуются в 12-ти вершинном полиэдре в виде икосаэдра или кубооктаэдра, молекулы фенантролина располагаются по всем вершинам и ребрам полиэдра, покрывая всю его поверхность, ацетатные группы являются внешнесферными (рис. 57). В настоящее время имеются сведения о получении еще более крупных кластеров – семислойного состава Pd1415phen60O~1100 и восьмислойного Pd2057phen84O~1600.
Радикальное отличие свойств кластерных молекул от свойств компактных металлов убедительно доказано различиями в их электропроводности, теплоемкости и магнитных характеристиках. Так, для кластеров Au55 и Pd561 уже типичным является локализация электронов, формирующих в отличие от металла дискретные энергетические уровни и соответственно не обобществленные молекулярные орбитали. Далее, с уменьшением размера кластера для него становится возможным и легко осуществимым одноэлектронный перенос, поскольку электростатическая энергия электрона становится больше кинетической

Рис. 57. Модель структуры гигантского кластера Pd560Phen60(OAc)180.
энергии. Как следствие, на вольтамперной кривой U=(I) проявляются ступеньки и плато, тогда как на массивном металле эта зависимость строго линейна.
Частицы с размером от 100 до 300 Å характерны для черней, коллоидных металлов, оксидов, сульфидов и т.п. веществ. Число внутренних атомов в этих частицах уже велико и, например упаковка металлических нанокластеров уже начинает напоминать структуру компактного металла. Растет энергия упругой деформации, которая в некоторый момент может превысить поверхностную энергию и в частицах будут реализовываться два типа упаковки: внутренняя – металлическая и внешняя – икосаэдрическая или ей подобная с осью пятого порядка. Отсюда и из других данных следует, что структура металлической коллоидной частицы, видимо, очень близка хотя бы по «идеологии» строения с структурой вышерассмотренного гигантского кластера Pd560Phen60(OAc)180, размер которого приближается к размеру мельчайших коллоидных частиц: внешние и внутренние слои металлов, ось пятого порядка, двойной электрический слой. К сожалению, структуры коллоидных частиц не установлены так детально, как структура некоторых гигантских кластеров, поэтому прямое их сравнение остается невозможным. Тем не менее исследование первых дает ключ к пониманию особенностей строения и некоторых свойств вторых и указывает на возможные методы их изучения и получения. Среди таких методов хорошо изучены и уже имеют широкое практическое применение методы «золь-гель» технологии, о которых более подробно мы поговорим ниже. Сейчас лишь стоит отметить, что использование в этих технологиях алкоксидов циркония, титана, алюминия, железа и ряда других позволяет получать нанокластерные системы-катализаторы FeO/ZrO2, FeO/TiO2 и другие с различным размером частиц. В то же время он (метод) из-за очень широкого распределения частиц по размерам не дает возможности получать организованные наноструктуры.
В этом отношении более перспективны методы синтеза нанокластеров, использующие прямые и обратные (обращенные) мицеллы (мицеллы – самоорганизующиеся частицы дисперсной фазы золя вместе с окружающей их сольватной оболочкой из молекул (ионов) дисперсионной среды (обычно ПАВ). В прямых мицеллах – обычно наблюдаемых в полярных средах, например в воде, ядро образовано гидрофобными радикалами, а гидрофильные группы ориентированы наружу; в обратных мицеллах -,обычно наблюдаемых в сильно неполярных средах, гидрофильные или полярные группы ориентированы внутрь ядра). В этом отношении наибольший интерес представляют обратные микроэмульсии, обладающие большой подвижностью и большой поверхностью раздела фаз. Это свойство при постоянном столкновении частиц микроэмульсий приводит к непрерывному обмену содержимого их ядер. Так, взаимодействие обратных мицелл на основе Na2S и серебра приводит к получению мицелл Ag2S с узким распределением по размерам. После освобождения от ПАВ-оболочки, обычно достигаемой обработкой тиолами, отделением от растворителя и высушиванием получают нанокластеры размером до 10 нм, но с достаточно узким распределением по размерам. Аналогичным образом получены полупроводниковые нанокластеры, кластеры металлических кобальта, серебра и золота. Однако, здесь необходимо подчеркнуть, что все эти вещества пассивированы тиолами, фосфинами или дитиолами, т.е. опять же избыточная энергия этих образований, как и в молекулярных кластерах, понижается за счет донорно-акцепторного (ковалентного) взаимодействия с внешнесферными молекулами лигандов. Хотя апологеты нанохимии этот факт как-то забывают отметить, рассматривая только ядро кластера. Но в данном вопросе не это главное. Используя специальные приемы, на подложках различного типа из этих равноразмерных нанокластеров удается сформировать как духмерные 2D-структуры, представляющие собой плотноупакованные монослои, в которых, как и в настоящих молекулярных или атомных двухмерных пленках, можно наблюдать дислокации и дефекты, так и трехмерные 3D наноструктуры с свойствами «кристалла», образующими, например, ОЦК-решетку. Таким образом, нанокластеры при строительстве наносистемы, как бы выступают в роли «больших атомов», но, конечно, взаимодействие между ними осуществляется за счет ван-дер-ваальсовых сил.
В настоящее время не установлено, когда в металлических кластерах исчезает икосаэдрическая и остается только типично металлическая упаковка. Возможно, что этот переход затруднен еще и кинетически. Во всяком случае наблюдались частицы металлов размером более 400 Å с осями пятого порядка. Но именно этот переход окончательно стирает грань между кластером и компактным металлом и является той верхней, хотя и очень размытой, границей существования кластерного состояния вещества. Судя по имеющимся данным, вряд ли число атомов, определяющее эту грань, будет одинаковым для различных металлов.
Отсутствие детальных данных по структуре многих металлических кластеров и УДЧ или по современной терминологии наночастиц, особенно в начале ряда и в его конце – в первом случае прежде всего из-за крайне высокой реакционной способности, а во втором из-за отсутствия возможности применения прямых методов исследования структуры вещества, крайне затрудняют определение корреляций «структура-свойство». Тем не менее, имеется довольно много примеров использования этих веществ в практических целях иногда даже без осознания их природы. Например, выше мы уже говорили о «золь-гель технологиях», в которых фигурантами являются коллоидные частицы оксидов металлов. Далее, магнитные жидкости – лиозоли ультрадисперсных магнитных частиц. С уменьшением размера ферромагнитной частицы до величины порядка 100 Å их магнитные свойства начинают существенно отличаться от свойств компактного металла (именно в этих отличиях и заключается уникальность истинных наноматериалов), поскольку частица ниже некоторой критической размерности из многодоменной становится однодоменной. Это приводит к тому, что все они намагничиваются однородно и при этом начинают проявлять супермагнитные свойства. Видимо образование подобных частиц является и причиной уникальных свойств магнитов на основе сплава Nd-Fe-B. Лиозоли с подобными свойствами применяются при изготовлении устройств, герметизирующих выходные валы, кабели или другие детали в стенке основного корпуса.
Особенно впечатляющая демонстрация размерных эффектов наблюдается в полупроводниковых нанокристаллах (обычно называемых квантовыми точками) с размером меньшим размера боровского радиуса экситона (квазичастица, соответствующая электронному возбуждению в кристалле диэлектрика или полупроводника, мигрирующему по кристаллу в виде волны, но не связанному с переносом электрического заряда и массы). По мере уменьшения размера кластера происходит увеличение ширины запрещенной зоны, определяемой задержкой электронно-дырочной пары, генерируемой фото- или радиационно-химическими способами, в ограниченном объеме пространства. Это приводит к тому, что в некоторых полупроводниках, относящихся к классу оптических преобразователей, рекомбинационная люминесценция сдвигается в область более высоких энергий (голубая область). Например, нанокристаллы CdSe покрытые одим-двумя слоями ZnS при дискретном увеличении размера с 23 до 55 Å меняют цвет с голубого через зеленый и оранжевый до ярко-красного.
Определенные и вполне обоснованные надежды и прямые успехи связаны с применением кластерных частиц металлов в катализе. На это указывают многочисленные успешного применения УДЧ носители благородных металлов, нанесенных на минеральные носители, черней и т.п. Конечно, в каталитической реакции «работают» уже не отдельные изолированные кластеры, а продукты их реакции с подложкой, субстратом, растворителем, если он применяется, в конце концов с примесями, избавиться от которых на 100 % просто невозможно. Однако исходный материал для получения реально работающего катализатора – кластер и размерный и структурный факторы в гетерогенном катализе вещь еще непознанная, но явно имеющая место. Сейчас методом молекулярных пучков можно направленно получать кластеры любой нуклеарности, а иногда определять и их структуры, а затем изучать зависимости реакционной способности в той или иной реакции от числа атомов в нем. Так, установлено, что атом Re не реагирует с метаном, в то время как Re3 весьма активен. Линейные Cu3 и Ni3 не реагируют с водородом и метаном, а треугольные и Ni13 высокоактивны. Кластеры Соn с n=3-5 и 10-18 реагируют с водородом с диссоциацией последнего, а с n=6-9 абсолютно инертны. В кластерном состоянии даже золото теряет свое «благородство» и в реакции СО+О2 → СО2 высокоактивны кластеры с n=8,11,15, 18. Таких примеров сейчас известно множество, хотя понять еще не значит создать - это задача другого порядка, но отправная точка существует и следует уже искать пути преобразования знания в конкретный катализатор.
Другой пример – металлические стекла, получаемые при сверхбыстрой закалке расплава металла. Многие их уникальные свойства, прежде всего магнитные, теплофизические, механические, связывают с кластерной природой их структуры.
Как уже неоднократно упоминалось, безлигандные металлические кластеры особенно малой нуклеарности - крайне реакционноспособные вещества. Метастабильное энергонасыщенное состояние частиц приводит к тому, что они энергично взаимодействуют с любыми функциональными веществами, содержащимися в среде, в которой их получают – следами кислорода и влаги, молекулярным и органическим азотом, всеми органическими веществами и даже с инертными газами. Если же такого взаимодействия по каким-то причинам все же нет, то они уже при обычных условиях в процессе хранения агрегируют и образуют обычные металлические порошки. Так, коллоидные металлы с размером частиц <100 Å без специальных мер стабилизации агрегируют и выпадают из раствора. Порошки УДЧ после удаления матрицы агрегируют с сильным разогреванием. Равномерно нанесенные на подложку УДЧ «ползут» по поверхности носителя друг к другу и образуют островковые структуры. В этих процессах естественным образом теряются все или многие уникальные свойства УДЧ и материалов на их основе. Вследствие этого проблема стабилизации и хранения УДЧ является наиболее актуальной и не решена сколько-нибудь удовлетворительным образом по настоящее время. Казалось бы самый простой и естественный способ стабилизации УДЧ создание покрытия на их поверхности. Образующаяся при этом шуба должна защитить частицы от слипания и ненужных реакций. Для такой защиты используют небольшие молекулы n и π-доноров типа CO, NH3, ацетилена, этилена, фосфинов, аминов и т.п. В зависимости от типа лиганда и способа его взаимодействия с металлическим остовом образуются или молекулярные кластерные соединения или кластерные материалы. Однако такое действие не проходит бесследно для УДЧ – при сохранении металлоостова, как правило, теряются многие привлекательные для их использования свойства, такие как высокая энергонасыщенность, уникальный магнетизм и каталитическая активность. Только в исключительных случаях, например при стабилизации некоторых золей УДЧ размером 20-100 Å поливиниловым спиртом удается сохранить их магнитные свойства, хотя и в этом случае они становятся более слабыми, чем в нативном состоянии. Естественно также, что с увеличением ядерности кластера, т.е. с увеличением доли внутренних атомов, роль стабилизирующих веществ, взаимодействующих только с поверхностными атомами металлов, уменьшается и на частицы >300 Å они уже оказывают небольшое влияние.
К настоящему времени известны несколько типов кластерных материалов, хотя все они «сконструированы» по одинаковому типу – путем внедрения кластера в матрицу из органического полимера (обычно проводят совместную конденсацию паров металла и мономера, например ди-п-ксилилена или метилметакрилат, полимеризующихся при низкой температуре, на охлажденную поверхность реактора), в поры цеолита, в межслоевое пространство неорганической матрицы, например графита или глин и в другие вещества или смеси веществ. Таким образом, кластеры как бы запечатываются внутри этих структур, но, конечно, и в этом случае происходит их взаимодействие с матрицей. Материалам, полученным в результате высокоскоростного термораспада соединений металлов в расплаве полимеров, присвоено название «класпол» - кластерный полимер. Размер металлических частиц в них изменяется в пределах 20-30 Å и распределены они в полимере по островковому типу, но в целом изотропно. По авторским данным подобное наполнение полимерной матрицы металлом приводит к повышению термической устойчивости, улучшению физико-механических свойств, необычным магнитным и электрофизическим свойствам. Однако, учитывая все вышесказанное относительно высокой химической активности больших кластеров, мы критически относимся к подобным рекламным заявлениям авторов и имеем большие сомнения как относительно размеров получаемых частиц, так и их сохранности от реакций окисления. Тем не менее, действительно следует признать некоторые отличия свойств материалов получаемых вышеописанным способом от свойств материалов, получаемых простым смешением металлических порошков с полимером. Например, чувствительность класпола свинца с поли-ди-п-ксилиленом на 4-5 порядков выше простых смесей этих же веществ.
Весьма интересен способ получения высокопористых металлов путем терморазложения их гидридов. Например, разложение гидрида бериллия приводит к получению пенобериллия с плотностью <0.1 г/см3. Формально это вовсе не кластерный материал, но его ажурная структура построена из спекшихся ультрадисперсных частиц бериллия. Если прокатать эту «пену» при нагревании, то будет получена бериллиевая фольга очень высокого качества, которое лишь с трудом достигается при использовании обычного порошка бериллия.
Материал, состоящий из УДЧ частиц металла и эпоксидной или полиэфирной смолы, носит торговое название «холодная сварка», что очень образно отражает его основное свойство – склеивать так прочно треснувшие или разбившиеся детали из самых различных материалов, в том числе и чугуна и сталей, что они могут работать длительное время как будто их сварили или спаяли. Например, треснувший корпус дизеля может быть склеен этим клеем и находится в рабочем состоянии десятки часов – времени более чем достаточным, чтобы добраться до ремонтной базы.
УДЧ железа, внедренные в поры цеолитов или других минеральных носителей, являются хорошими катализаторами реакции Фишера-Тропша (реакция каталитического гидрирования СО), устойчивы в работе и хорошо регенерируются. Образование нанокластеров в порах минеральных или органических «инертных» носителей (цеолиты, угли, полисорбы (сополимеры стирола и дивинилбензола), глины и пр.) – один из наиболее эффективных методов получения и стабилизации этих материалов. Обычно их выращивают в поре кристаллизацией из растворов, хотя известны и газофазные методы, но для первого способа лучше развит аппарат описания процесса. Ограниченная концентрация растворенного вещества внутри поры и отсутствие эффективного массообмена приводит и к ограничению размера или объема кластера в поре значением nmax, которое всегда меньше значения n0, характеризующего число атомов растворенного вещества, и меньше размера (диаметра) поры. Кроме того, поскольку рост зародыша кластера скорее всего происходит при контакте с стенкой поры, снижается энергетический барьер зародышеобразования, т.е. происходит стабилизация и рост большей части зародышей, а не их растворение, как это обычно наблюдается в растворе.
Некоторые типы соединений внедрения металлов в межслоевое пространство графита, фуллеренов и нанотрубок также можно отнести в кластерным соединениям, но уже находящимся в двумерном состоянии. Однако, если цеолиты, полимерные материалы, в первом приближении, можно рассматривать как инертные контейнеры (что, конечно, далеко не так), то графитовые слои, в которых каждый атом углерода имеет свободный π-электрон, по сути дела является полидентатным ароматическим π-лигандом и его взаимодействие с атомами металлов уже следует рассматривать как взаимодействие химическое. С другой стороны, атомы металла располагаются между углеродными слоями скорее всего не островками или группами, а изотропно с образованием одномерной плоской сетки, состоящей из одного (щелочные металлы) или двух (железо) слоев (хотя имеется и иная точка зрения на строение этих материалов). В этих слоях прямых межатомных контактов может и не быть, но при полном обобществлении электронов характерном для графитовой матрицы, наверное, не имеет смысла делать из этого факта какие-либо выводы нацело отрицающие возможность кластерообразования, хотя бы на уровне обменных кластеров. В то же время в СВГ тяжелых щелочных металлов, как отмечалось выше, такой контакт неизбежен просто в силу геометрических причин, вытекающих из кристаллохимических закономерностей, а в фуллеридах легких щелочных металлов факт кластерообразования зафиксирован экспериментально на примере соединения внедрения состава Na11C60 или Li25C60.
СВГ, помимо использования их для изготовления конструкционных, прокладочных, сорбционных и огнезащитных материалов, интересны и в ряде химических процессов, в катализе, электрохимии и вообще в реакциях с многоэлектронными переносами (например при 6-ти электронном переносе в ходе каталитического синтеза аммиака из азота и водорода). Действительно, СВГ ряда переходных металлов были использованы в таких каталитических процессах, как гидрирование и полимеризация ненасыщенных углеводородов, в окислении водорода, аммиака и парафинов, дегидрировании спиртов и ряде других. Как правило, эти вещества проявляют лучшие каталитические свойства по сравнению с другими известными гетерогенными катализаторами этих же металлов для данной реакции. Они более устойчивы в работе, дают возможность глубокого модифицирования. В то же время пространственные затруднения, создаваемые сетками углерода, уменьшают скорость реакции полимеризации по сравнению с открытыми системами.
Близкими по своей природе к некоторым СВГ стоят и такие кластерные материалы, в которых имеются плотно упакованные металлические цепи или слои, обрамленные лигандами. Эти цепи слабо взаимодействуют с соседями и образуют низкоразмерную кристаллическую решетку. Это приводит к ярко выраженной анизотропии в химических и некоторых физических свойствах: внутри отдельных цепей или слоев имеется сильное взаимодействие, а между собой они связаны слабыми вандерваальсовыми силами. Соединения цепочечного типа относятся к одномерным, а слоистые к двумерным системам, точнее квазиодномерным и квазидвумерным, поскольку в любой системе имеется трехмерное взаимодействие, но меньшей энергии, чем в первых двух. К таким соединениям относятся бинарные и тройные халькогениды и халькогалогениды, переходных металлов, некоторые соли благородных металлов и другие. Например, NbTe4, M6X8, MxMo6X8 (фазы Шевреля), Pt(NH3)4PtCl4, CoCl2·2H2O и др. Все они могут быть матрицами для интеркаляции различных веществ, а некоторые, например фазы Шевреля, представляют и самостоятельный интерес, поскольку обладают хотя и слабыми, но сверхпроводящими свойствами.
Примеров кластерных или наноматериалов еще не достаточно много, на даже на примере того, что имеется, можно сделать вывод о перспективности их использования в практических целях (для тех, кто специально интересуется вопросами перспектив применения нономатериалов, могу порекомендовать обзоры А.Л. Бучаченко и Г.Б. Сергеева, опубликованные в журнале Успехи химии за 2003 г.). Этот вывод, учитывая большое число возникших за последние годы программ по нанотехнологиям и наноматериалам, не кажется оторванным от жизни, но пока является все еще в значительной степени делом будущего. В то же время научные работы в другой области химии кластеров – химии молекулярных кластеров, стабилизированных различными лигандами, это дело настоящего. Исследования в этой области оставили глубокие следы практически во всех разделах современной химии. И это понятно, поскольку следы в науке остаются тогда, когда теоретические представления, существовавшие до начала работ в новой области входят в противоречие с их результатами или не могут их объяснить: структуру, электронное строение и реакционную способность кластеров оказалось невозможным описать и понять с использованием положений координационной химии, развитых Вернером, нельзя применить к ним и теорию кристаллического поля и метода МО в его классическом варианте, широко используемых в координационной химии.
Молекулярные кластеры
Мы уже отмечали, что голые или безлигандные кластеры, видимо, могут существовать только в момент получения в глубоком вакууме. В «обычных» условиях (если можно назвать обычным, например условия матричного синтеза) они в той или иной степени окружены молекулами различных веществ, которые только в исключительных случаях остаются инертными по отношению к металлическому кластеру, а в подавляющем большинстве реагируют с ним и окисляют его. В кластерах, окруженных лигандами, большая часть энергии исходного, «голого» кластера уже израсходована на реакцию с этими лигандами, а возникающая при этом оболочка предотвращает взаимодействие между частицами и проникновение реагентов вглубь металлического ядра, которое могло бы окончательно разрушить металлический остов. Таким образом, лиганды должны удовлетворять нескольким противоречивым требованиям: с одной стороны, они должны взаимодействовать с поверхностными атомами металлов, а иногда и внутренними, а, с другой, не разрушать довольно слабые связи М-М. Как ни странно, таких лигандов известно достаточно много.
В кластерных соединениях лиганды могут иметь вершинную (μ), реберную (μ2), граневую (μ3, μ4) или внутриполостную (μnвн) координацию. Наиболее простой для описания лиганд – атом водорода. Однако несмотря на то, что электронные возможности этого атома ограничены одним электроном, он способен образовывать далеко не простые соединения со всеми возможными типами координации лигандов, хотя наиболее распространены μ3 и μ4 –типы. В случае атома водорода понятие «простота» ограничивается только тем, что при любом типе координации число донируемых этим атомов электронов не меняется и не превышает 1. Но это атомарный водород, который еще нужно генерировать из молекулярного, не прибегая к высокоэнергетическим средствам, т.е. каталитически. Этот процесс длительное время оставался неисследованным экспериментально, хотя правдоподобные гипотезы, особенно из области катализа, существовали уже давно, в частности предполагались стадии координации (хемосорбция), активации, диссоциации, образования связи М-Н. Среди них наиболее загадочной оставались стадии активации и диссоциации. И только в 1984 году был выделен молекулярный комплекс состава M(CO)3(η2-H2)(PR3)2, (M-W, Mo) на примере которого было показано, что молекулярный водород координирует к металлического типу по η2-типу. При этом расстояние Н-Н возрастает до 1.20-1.33 Å против 0.74 Å в индивидуальной молекуле. Сейчас уже имеется довольно много других примеров диводородных комплексов, в том числе и таких в которых показано, как они превращаются в гидридные комплексы и обратно. Так, совсем недавно были исследована целая группа однотипных комплексов осмия, стабилизированных фосфиновыми лигандами с диводородом и гидридными лигандами и промежуточными между ними формами, названными комплексами с «растянутым» водородом.
Наиболее просты для понимания координационных возможностей лиганды n-типа – простые эфиры, амины, фосфины и т.п. – это всегда двухэлектронные доноры.
Ряд других лигандов при взаимодействии с кластерами может менять число донируемых электронов в очень широких пределах. Так, атом хлора при вершинной координации является одноэлектронным донором, при реберной трех-, а при граневой пятиэлектронным.
Сера при вершинной и реберной координации донирует 2 электрона, при граневой 4. Но даже при μ3 координации у нее остается неподеленная пара электронов, способная координировать еще один атом металла.
Очень сложный и неоднозначный лиганд СО. В моноядерных комплексах это двухэлектронный лиганд, остается им же и при реберной координации в кластерах, если располагается перпендикулярно ребру или грани. В противном случае в образование связи включаются электроны кратной связи и неподеленные пары электронов атома кислорода, поэтому при параллельном расположении относительно ребра или грани он может донировать 6 электронов.
Олефины в моноядрных комплексах являются двухэлектронными донорами (от двойной связи). В трехъядерных кластерах они уже доноры четырех электронов – два электрона от двойной связи и по одному от атомов углерода. При этом разрываются связи С-Н и образуется гидридный кластер.
Ацетилены также довольно нестандартные лиганды. Их координация по вершинам, в которых они выступают как двухэлектронные лиганды экспериментально не доказана, хотя такая возможность обоснованно предполагается. В граневой координации ацетилен донор четырех электронов. При этом он резко меняет свою геометрию и становится этиленоподобным. Известны случаи, когда он является донором шести электронов, но при этом, как и этилен теряет свои протоны и образует гидридные кластеры. Близкие с ним свойства проявляют и нитрильные лиганды.
В химии кластеров известны и такие необычные соединения как кластеры с внутриполостным расположением лиганда, обычно являющимся одноатомным атомом водорода, углерода, азота, серы, фосфора, мышьяка, бора, сурьмы, кремния.
Возникает вопрос сколько и какие по своей природе лиганды координирует тот или иной металлический кластер? На вопрос сколько достаточно правильный ответ дает решение чисто геометрической задачи, в которой внешняя часть остова кластера задается идеализированной поверхностью – цилиндром для цепи, тором для цикла, шаром для полиэдра, с радиусами равными ковалентным радиусам металлов, вокруг которой размещаются лиганды с вандерваальсовыми контактами между ними.
Существенно хуже обстоят дела с прогнозом какие лиганды будут координированы к данному кластеру. Ранние правила относительно этого прогноза, говорившие, что кластеры из металлов VIII группы предпочитают СО-лиганды, а кластеры из металлов IV-VI галоидные лиганды (концепции π-акцепторной и π-донорной предпочтительности) при получении больших объемов информации оказалась заблуждением. В настоящее время от них осталось только вполне очевидное и тривиальное обобщение, говорящее о том, что кластеры, образованные металлами в низковалентном состоянии, присоединяют акцепторные лиганды, а в высоковалентном – донорные.
Связь в кластерах
В обыденной химии при описании химической связи в моноядерных молекулах мы обычно оперируем понятиями валентных электронных пар, s, p и spd –атомными орбиталями. При описании соединений, содержащих связи металл-металл, остаются те же понятия и описывающие их элементы, но их взаимные комбинации существенно усложняются и дополняются новыми. При этом основную роль в образовании связи М-М отводится d атомным орбиталям металла, хотя в низковалентных кластерах с лигандами сильного поля типа СО (π-акцепторы) энергетическая разность между s, p и d орбиталями невелика и поэтому вклады s и p-орбиталей в энергию связей довольно значительны. В то же время в высоковалентных кластерах с лигандами слабого поля, например галогенидами (π-доноры), эта разность более существенна и основной энергетический вклад в связь М-М дают d-орбитали, а s и p –орбитали преимущественно используются для образования связей с лигандами. Эти различия отражаются и на характеристиках связей М-М: в низковалентных комплексах и кластерах связи М-М по преимуществу одинарные, имеют σ-характер с малым вкладом π-составляющей. Поскольку энергия этих связей сравнительно невелика межатомные расстояния превышают некие средние значения. В высоковалентных комплексах и кластерах в образование связи М-М основной вклад дают π и δ электронные плотности, расстояния М-М в них существенно сокращены и связи часто бывают кратными. Мы знаем, что, например, в ненасыщенных углеводородах кратные связи образуют s и p электроны за счет σ и π перекрывания гибридизованных АО (sp2 или sp гибридизация). При этом сама связь приобретает вполне определенные химические (например, типичную для ненасыщенных соединений реакцию присоединения) и энергетические свойства (сравнимые величины энергии составляющих ее компонент). В случае межметаллических связей все не так однозначно и сам термин «кратность» скорее имеет качественную характеристику и говорит лишь об общем числе электронов, участвующих в ее образовании (см. выше). При этом компоненты ее составляющие существенно отличаются по энергиям и, в целом, порядок связи М-М или ее кратность никоим образом не характеризуют ее прочность.
Большая часть соединений с кратными связями относится к биядерным комплексам, выдающуюся роль в исследовании которых внес Ф.Коттон. В то же время истинные кластеры с кратными связями даже с числом атомов металлов равным 3 довольно редки и кратность связи в них не превышает 3. Так, в кластере Mo4Cl8(PR3)4 две связи Мо-Мо имеют кратность равную 1, а две равную 3. В кластерах высокой нуклеарности кратные связи неизвестны. Еще раз можно подчеркнуть, что кратные связи М-М обнаружены только в комплексах с π-донорными лигандами и атомами, находящимися в высоких степенях окисления. Введение в состав таких соединений π-акцепторов, например СО, приводит к разрушению не только кратной связи, возможно из-за использования части d-электронной плотности на π-акцепторные орбитали лиганда, но и одинарной связи М-М. Таким образом, соединения с кратными связями в химии кластеров скорее исключение, чем правило и обычно связь в истинно кластерных соединениях описывается как одинарная.
Характерной особенностью молекулярных кластеров являются так называемые магические числа валентных электронов, равные общему числу валентных электронов, принимающих участие в образовании кластера, и которые специфичны для определенной его геометрической формы и симметрии. Они одинаковы для кластеров, построенных из различных металлов, но имеющих однотипное строение. Адекватная структурная модель кластера должна правильно предсказывать значения магического числа, и наоборот, магическое число, рассчитанное из состава кластера, должно дать представление о его структуре (хотя и не всегда).
Существует два подхода для подсчета числа кластерных валентных электронов (КВЭ). Первый из них основан на правиле Сэджвика (Сиджвика) или правиле эффективного атомного номера, согласно которому каждый атом металла стремится дополнить свою электронную оболочку до конфигурации следующего за ним инертного газа ([n-1)d10ns2np6). Это становится возможным только в случае, если внутри данного класса кластеров действует постулат о локализованной двухцентровой и двухэлектронной связи М-М (принцип «2е+2с»). В ряде случаев это позволяет не только объяснять строение комплексов, но и прогнозировать их химические свойства. Например, рассмотрим ряд моноядерных бис-циклопентадиенильных комплексов переходных металлов IV-VII групп, взятых в одинаковой степени окисления III. В Cp2TiCl атом титана с учетом, что циклопентадиен является пяти электронным донором, имеет 15-ти электронное окружение (рис). У него имеется одна вакантная орбиталь и одна полузаполненная, т.е. комплекс парамагнитен, обладает кислыми (по Льюису) свойствами и должен координировать нуклеофилы. Действительно, все известные комплексы титаноцена III димерны или в общем случае координируют анион, атом, группу Х-. У аналогичного соединения ванадия на фронтальных орбиталях уже два электрона и атом ванадия имеет 16-ти электронное окружение. Соединение «амфотерно» - с одной стороны, оно проявляет кислые свойства, но уже только по отношению к сильным нуклеофилам, а с другой, за счет своей пары электронов в реакции с сильными кислотами может проявлять и основные свойства. В парамагнитном Cp2MoX атом молибдена имеет 17-ти электронное окружение и комплекс проявляет только основные свойства. В Cp2ReX атом рения имеет 18-ти электронное окружение с двумя парами неподеленных электронов, и комплекс проявляет сильно основные свойства. Таким образом, все соединения, имеющие неподеленные пары электронов могут достаточно легко протонироваться, давая ионные комплексы, а цены с вакантными орбиталями любыми способами присоединять нуклеофильные частицы, в том числе и внутримолекулярные атомы, образуя, например комплексы с агостической связью <М←Н-δ-С>.
Это правило оказывается выполнимым и для большого числа кластерных соединений. В этом случае общее число КВЭ в кластере MmLn подсчитывается как сумма валентных электронов (к) всех атомов (m) металлов плюс число электронов (l), донируемых всеми лигандами (n), и заряда, взятого с обратным знаком (±е), т.е. Σ=km+ln±е. Это число может быть подсчитано и другим способом, но для этого необходимо знать структуру вещества. Из числа валентных электронов, получаемого умножением 18 на число атомов в кластере (заполненная электронная оболочка каждого атома), т.е. 18m, вычитается число т.н. скелетных электронов, обеспечивающих связи М-М, каждой из которых отвечает одна разрыхляющая орбиталь. Таким образом, фактически мы получаем разницу между числом электронов на связывающих орбиталях и числом виртуальных электронов на разрыхляющих. Тогда, например для Rh6C(CO)15-2, образующего тригональную призму, мы имеем по первой схеме 9х6+2х15+4+2=90, а по второй 18х6-2х9=90 (где 9- число связей М-М). Это и есть магическое число кластера для данного типа многогранника, о которых уже говорилось выше. Для тетраэдра оно будет равно 18х4-6х2=60, для квадрата 18х4-4х2=64, треугольника 18х3-3х2=48 и т.д. Присоединение дополнительных электронов к кластеру, которые могут разместиться только на его разрыхляющих орбиталях, приводит к разрушению связи М-М. Так, при добавлении двух электронов к 60 е тетраэдрическому кластеру рвется одна связь и он превращается в 62 е «бабочку» или ромб, а при добавлении следующих 2 электронов в 64 е квадрат.
При повышении нуклеарности кластера и в случае образования многогранников, в вершинах которых сходится более трех ребер, принцип «2е+2с» нарушается, что говорит о более сложном характере связи в этих веществах, чем это можно описать, используя правило ЭАН. Так, согласно этому правилу октаэдрический кластер должен содержать 84 е, а в большинстве известных наблюдается 86 е и это число принято называть магическим для кластеров данного строения. Для подсчета КВЭ в кластерах с произвольным, но небольшим числом вершин Уэйдом (Wade) предложено правило 2n+2, которое применимо и для подсчета электронов в полиэдрических бороводородах. Предполагается, что в полиэдрической молекуле электронная оболочка разделена на две независимые подсистемы – экзополиэдрическую (внешнюю) и эндополиэдрическую или скелетную (внутреннюю). Первая отвечает за связывание с внешними лигандами или содержит неподеленные пары электронов, вторая за образование связей М-М. Согласно этому правилу каждый клозо -n-вершинник (замкнутый полиэдр) имеет n+1 связывающих скелетных (эндо) МО, на которых могут разместиться 2n+2 электрона. В случае октаэдра это число равно 14. Экзополиэдрическая подсистема включает n орбиталей в случае непереходных металлов, например бора, и 6n для переходных или суммарно 2n+1 и 7n+1, соответственно, связывающих МО. Заполненная электронная оболочка таких молекул должна содержать 4n+2 (бораны) и 14n+2 (металлокластеры) электронов. Отсюда магическое число для октаэдрического кластера равно 86 и 170 для икосаэдрического.
При наличии открытой грани в октаэдре (тетрагональная пирамида или нидо- n-вершинник)число скелетных орбиталей увеличивается на единицу, т.е. будет равным n+2, при этом число скелетных электронов не меняется и также будет равно 2n+4=14, а число КВЭ уменьшается до 74. В случае двух открытых граней (в данном примере квадрат или арахно- n-вершинник, хотя это неправильный пример, так как это уже не полиэдрическая молекула) число скелетных орбиталей увеличивается еще на единицу и составляет n+3, но число скелетных электронов по-прежнему сохраняется равным 14. В гифо- n-вершиннике с тремя открытыми гранями число скелетных орбиталей становится равным n+4 при числе электронов 14. Таким образом, исчезновение одной или нескольких вершин в многограннике не изменяет общего числа скелетных электронов. Не изменяет
 2018-02-13
2018-02-13 2144
2144








