Теплота Q и работа A не являются функциями состояния системы, это – способы обмена энергией. Эти величины зависят от пути перехода, в отличие от изменения внутренней энергии; поэтому эти величины на бесконечно малом участке процесса не будут с точки зрения математики полными дифференциалами, и для них используются обозначения 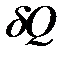 и
и 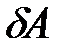 .
.
Работа идеального газа при изменении объёма.
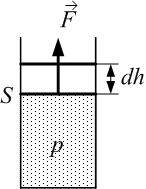
Рассмотрим идеальный газ в сосуде под поршнем площадью S. Давление газа равно p (рис.8.1).
При подъёме поршня на малую высоту dh сила давления газа
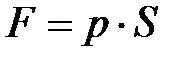 (8.7)
(8.7)
совершит работу
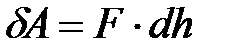 . (8.8)
. (8.8)
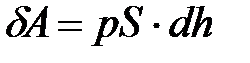 ,
,
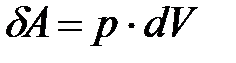 , (8.9)
, (8.9)
так как 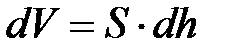 – увеличение объёма газа.
– увеличение объёма газа.
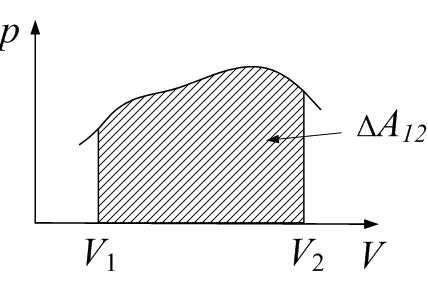
Работа газа при переходе между состояниями 1 и 2 работа равна
| Рис.8.1 |
| Рис.8.2 |
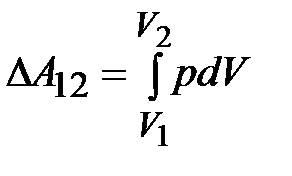 . (8.10)
. (8.10)
Работа равна площади под графиком 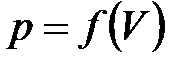 (рис.8.2).
(рис.8.2).
Работа газа в изопроцессах
1) Изохорический процесс
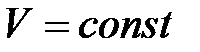 , следовательно,
, следовательно, 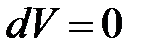 , работа не совершается:
, работа не совершается: 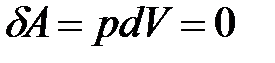 ,
, 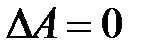 .
.
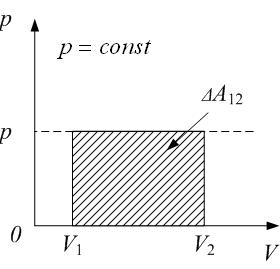
2) Изобарический процесс
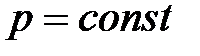
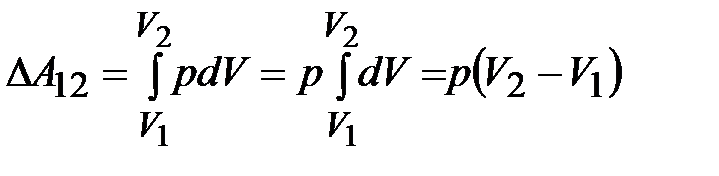
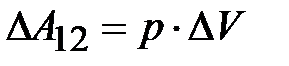 . (8.11)
. (8.11)
То же самое получим из графика рис.8.3 как площадь прямоугольника.
Из уравнения Менделеева-Клапейрона
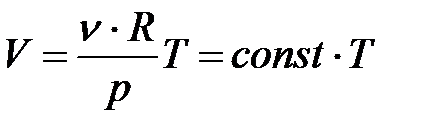
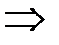
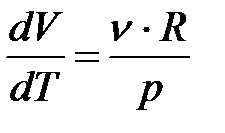
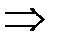
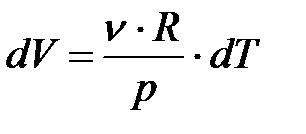
Отсюда работа из (8.9):
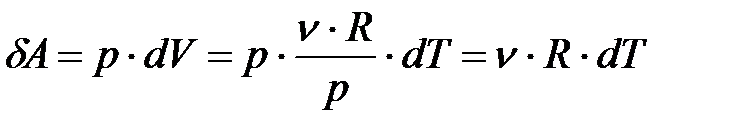
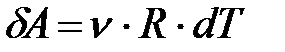 . (8.12)
. (8.12)
То же самое можно получить в интегральном виде:
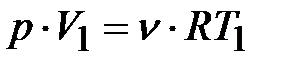
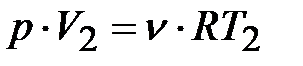
Тогда
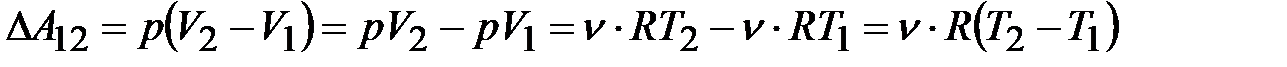
Или:
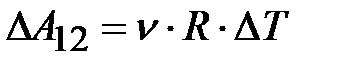 . (8.12а)
. (8.12а)
Соотношение (8.12) проясняет смысл универсальной газовой постоянной R:
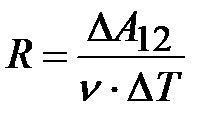 ;
; 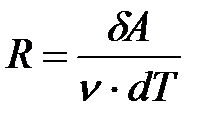
универсальная газовая постоянная численно равна работе одного моля идеального газа при изобарном нагревании на 1 кельвин.
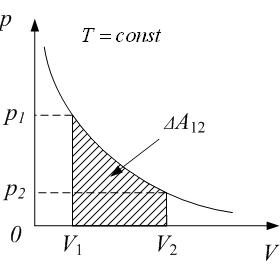
Изотермический процесс
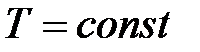
Из уравнения Менделеева-Клапейрона выразим давление и подставим в (8.10):
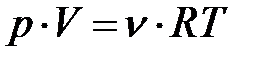
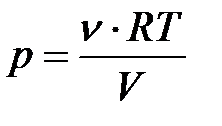
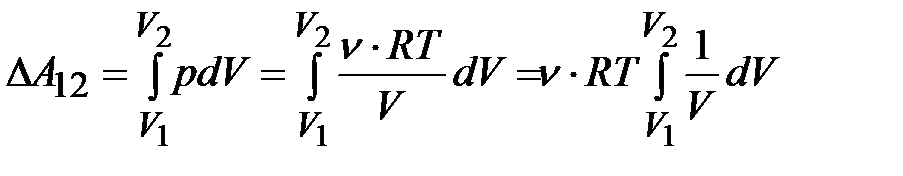 ,
,
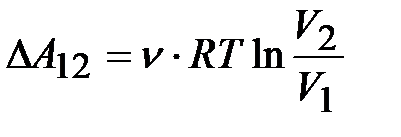 (8.13)
(8.13)
| Рис.8.4 |
| Рис.8.3 |
Уравнение процесса: 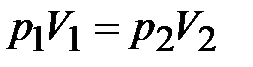
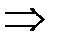
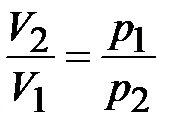 ; тогда
; тогда
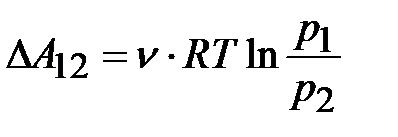 (8.14)
(8.14)
Билет
 2018-02-14
2018-02-14 318
318








