Микроэлементами А П Виноградов называет такие элементы, среднее содержание которых в водах обычно составляет менее 10 мг/л. В отдельных случаях содержание микроэлементов в водах может намного превышать указанную цифру. К числу микроэлементов относят бром, иод, фтор, бор, литии, рубидий, стронций, барий, мышьяк, молибден, медь, кобальт, никель, цинк, радиоактивные элементы, золото и др.. Современные исследования показывают что в обогащении подземных вод микрокомпонентами главную роль играют соли морского генезиса и процессы, протекающие в коре выветривания Наибольшее разнообразие микрокомпонентов обнаруживается в водах связанных с корой выветривания гранитов.
Микроэлементы в водах исследуются при поисках месторождении нефти, газа, солеи и полиметаллов. Изучаются они и сбальнеологической точки зрения, так какнекоторые микрокомпоненты придают водам лечебные свойства. И, наконец, особый интерес микрокомпоненты представляют в санитарно гигиеническом отношении. Несмотря на малое содержание, роль микроэлементов в жизненных процессах очень велика. Многие микроэлементы являются биологически активными. Недостаток или избыток их в природных водах вызывает появление среди людей и животных местных заболеваний, называемых эпидемиями. Эндемический зоб возникает в тех местах, где в воде, почве, воздухе и растениях мало или совсем нет йода. Отсутствие или недостаток микроэлементов в водах и почвах обусловливает отсутствие или недостаток их в растениях и овощах.
При недостатке в питьевых водах фтора наблюдается заболевание зобов — кариес, а при избытке этого элемента другое заболевание — флюороз. Распространение подагры связано с высоким содержанием молибдена в водах. Известны провинции с избытком редких элементов. В районах никелевых месторождении в Казахстане скот слепнет от избыточного содержания никеля в кормах. Повышенное содержание бора в почвах (а. следовательно, и в водах) некоторых районов Прикаспийской низменности вызывает тяжелые желудочно-кишечные заболевания у овец, повышенное содержание селена в травах вызывает разрушение рогов, копыт и другие болезненные явления. Домашние животные болеют в районах, обогащенных молибденом, стронцием и другими редкими элементами.
О.А.Алекин делит условно группу микроэлементов на пять подгрупп:
1). типичные катионы (Li+, Rb+, Be++, Cs+, Ba++ и др),
2) ионы тяжелых металлов (Cu++, Ag+, Au+, Pb++, Fe++, Ni++, Co++ и др.),
3) амфотерные комплексообразователи (Cr, Mo, V, Mn);
4) типичные анионы (Вг-, I-, F-, B-);
5) радиоактивные элементы.
Формы нахождения микроэлементов в растворе многообразны. Они могут присутствовать в природных водах в виде взвесей коллоидов (гидроокислы металлов), в форме комплексов образуемых с гумусовыми и другими органическими кислотами, в виде недиссоциированных молекул (СuSO4), полудиссоциированных (СuСl2+) и свободного иона (Сu++) и т.д.
Содержание микроэлементов в природных водах в большинстве случаев очень низкое, намного ниже 1 мг/л. Поэтому для удобства их концентрацию иногда выражают в мкг/л (1мкг=0,001 мг).
Общей причиной ничтожных содержании микроэлементов в водах является не их малая распространенность в природе, так как существуют микроэлементы (Fe+++, Al+++), содержащиеся в земной коре в больших количествах, а их очень слабая миграционная способность. Ряд факторов препятствует накоплению и миграции микрокомпонентов в водной среде. К числу их относятся присутствующие в водах анионы OH-, CO3--, реже H2PO4- и HS-. Катионы тяжелых металлов с этими анионами образуют слаборастворнмые соединения. Особенно большое лимитирующее значение имеют ионы ОН-, так как большинство гидроокисей металлов трудно растворимы.
Другими факторами, ограничивающими подвижность микроэлементов являются адсорбция глинистым веществом и извлечение их из водных растворов живыми организмами. Наибольшей адсорбционной способностью обладают глинистые минералы, гидроокись железа (особенно для Mn, Ni, Co) и органические вещества различной степени дисперсности.
Бром. Бром, йод и фтор принадлежат к числу элементов, встречающихся в земной коре в рассеянном состоянии и большей частью в незначительных количествах. Содержание их в природных водах во много раз меньше содержания ионов хлора. Пресные воды отличаются, как правило, наинизшими количествами брома, колеблющимися от 0,001 до 0.2 мг/л. Сравнительно много брома в водах минеральных источников — до 10—50 мг/л и в водах некоторых соляных озер — до 900 мг/л. Максимальные количества брома обнаружены в рассолах нефтяных месторождений. Воды с высоким содержанием брома относятся к категории промышленных.
При повышении минерализации воды концентрация ионов брома так же, как и хлора, беспрерывно растет. Однако, в процессе садки солей (галогенеза) при наступлении галитовой стадии седиментации происходит разделение ионов хлора и брома. Ионы хлора переходят в твердую фазу, а ионы брома преимущественно остаются в водной фазе, что объясняется более высокой растворимостью бромидов по сравнению с хлоридами. В естественных условиях бром скопляется в больших количествах в остаточной (маточнике) рапе после садки солей. Минералы, содержащие бром, встречаются в природе как исключительная редкость.
Бром, в отличие от хлора, ассимилируется в каком-то количестве некоторыми организмами моря и сорбируется органическим веществом илов, почв н особенно торфами. Главным источником ионов брома в подземных водах являются горные породы, в которых он присутствует в рассеянном состоянии, а также океаны и моря.
Йод. Содержание йода в природных водах еще меньше, чем брома. В пресных подземных водах его концентрация выражается всего лишь в сотых и тысячных долях миллиграмма на литр. В морской воде йода 0,05 мг/л. В рапе соляных озер йод, как правило, отсутствует. Аналогично брому, йод в большом количестве скапливается в водах нефтяных месторождении. Солончаки, образующиеся в пустынях на нефтеносных структурах, нередко обогащены йодом, что может быть использовано для поисков нефти.
С недостаточностью йода в пище связано тяжелое заболевание щитовидной железы у человека и животных (зоб). Главная причина заболеваемости заключается в недостаточности йода в растительной пище, а не в питьевой воде. Одной из особенностей геохимии йода является связь его с живым веществом, выраженная гораздо более ярко, чем у брома. Поэтому йод концентрируется в почвах и илах, в образовании которых участвуют организмы. Много йода содержится в тонкодисперсных породах, богатых органическим веществом. Установлено, что абсолютное содержание йода в нефтяных водах не зависит ни от химического типа вод, ни от величины их минерализации и. очевидно, исключительно обусловлено наличием органического вещества в недрах. Органическое вещество, и горные породы могут быть источниками поступления йода в природные воды. Важным источником йода в почвах и водах являются дождевые осадки, захватывающие йод из атмосферы, в которую он приносится ветром со стороны моря.
Фтор. Этот компонент оказывает большое влияние на питьевые качества воды. Слишком малое (менее 0,01 мг/л) содержание фтора в питьевых водах, а также повышенные количества его (более 1,5 мг/л) вызывают заболевания зубов. Содержание ионов фтора в воде рек, озер и артезианских скважин колеблется в сравнительно узких пределах от 0,04 до 0,3 мг/л. В морской воде фтора содержится около 1 мг/л. В некоторых минеральных источниках его концентрация достигает большой величины от 23 до 38 мг/л.
Одним из источников повышенного содержания ионов фтора в подземных водах являются фторсодержащие минералы. Еще более высокое содержание фтора (6—9 мг/л) установлено в водах некоторых источников Центрального Казахстана, вытекающих из щелочных гранитов, а также в термальных источниках северных цепей Тянь-Шаня. Факторами, способствующими здесь накоплению ионов фтора в водах, являются, с одной стороны, щелочной тип вод (первый тпп по О.Л.Алекину, в которых лучше мигрирует фтор, а с другой — породы с повышенным содержанием фтора). Породы же гранитной магмы как раз более богаты фтором, и в них же формируются воды с высокими значениями рН.
Важным источником ионов фтора в природных водах служат продукты разрушения горных пород, в состав которых входит апатит (Са5(РО4)3F, турмалин, слюды и другие минералы. Подвижность ионов фтора весьма ограничена ввиду его способности давать с Са ++ труднорастворимое соединение Са F2. Исследования показали, что фтор, подобно йоду и брому, аккумулируется живым веществом. Повышенное содержание фтора, в нефтяных водах, по-видимому, связано с аккумуляцией его живыми организмами. В районах современной вулканической деятельности фтор может иметь ювенильное происхождение. Так, некоторые источники Камчатки содержат 70—80 мг/л фтора.
Бор. Бор принадлежит к числу рассеянных элементов. Он присутствует в природных водах повсеместнов незначительных количествах. В пресных подземных водах содержание бора составляет тысячные и десятитысячные доли миллиграмма на литр. В морской воде количество бора равно 1,5-4,4 мг/л. Высокие содержания этого иона (порядка 100—150 мг/л) установлены в рапе соляных озер.
Много бора в водах нефтяных месторождений, причем особенно много в щелочных водах, где его содержание составляет иногда сотни миллиграммов на литр.
Бор в подземных водах имеет различное происхождение, Он может поступать в воду при выщелачивании морских осадков. В последних иногда присутствуют борсодержащие минералы, выпадающие из морской воды при некоторых стадиях ее сгущения. Кроме того, растительные н животные организмы ассимилируют бор из морской воды, переводят его в морские илы и, тем самым, обогащают бором осадочные породы. Особенно богаты бором подземные воды, непосредственно омывающие экзогенные месторождения боратов. Бораты подобного генезиса обладают сравнительно хорошей растворимостью.
Эндогенные месторождения бора представлены боросиликатами (датолит, данбурнт) и алюмоборосиликатами (турмалин, аксинит). Эти минералы труднорастворимы, но воды, соприкасающиеся с продуктами их выветривания, содержат повышенные концентрации ионов бора. Поставщиком бора служат вулканы. При вулканической и поствулканической деятельности соединения бора выносятся на поверхность земли вместе с парами воды и другими продуктами извержения. Воды с высоким содержанием бора имеют лечебное значение.
Молибден. Молибден распространен в природе в виде эндогенного молибденита МоS2 который близ земной поверхности, в зоне окисления, отдает серу и превращается в ряд экзогенных минералов. Миграция молибдена в водах происходит наиболее часто в виде иона (МоО4--). Не исключена возможность переноса этого элемента и в виде коллоидов, т. к. продукты окисления молибденита представляют рыхлые тонксдисперсные вещества Спектральным анализом молибден был обнаружен во всех исследованных водах Заилийского и Джунгарского Алатау. Среднее содержание этого элемента в водах термальных источников составляет 15 мкг/л, для холодных источников и рек оно уменьшается в десять и более раз.
Ж. Сыдыков приводит следующие средние данные о содержании молибдена в трещинно-грунтовых водах: Уралтау-Сакмарская зона — 0,2 мкг/л, Зеленокаменная зона — 1,3 мкг/л и Урало-Тобольская зона — 2,7 мы/л. Повышенные концентрации (до 17 мкг/л) молибдена связаны с водами, залегающими в основных изверженных породах.
В природных водах Джунгаро-Балхашской металлогенической провинции содержание молибдена, независимо от величины рН, изменяется в широких пределах—от 0 до 10 мг/л. Наиболее высокие его содержания в целом по названному региону приходятся на воды нейтральные и слабощелочные {рН от 7 до 7,6). В области кислых (рн<7) и щелочных (рН —8,5) растворов содержание молибдена снижается.
На миграцию молибдена в водной среде оказывают влияние процессы сорбции его из водных растворов различными породамится. Источником молибдена в водах являются сульфидные руды и разнообразные горные породы. Из изверженных пород наиболее богаты молибденом основные и кислые породы (базальты, габбро, граниты), меньше всего молибдена в ультра-основных породах. Осадочные породы содержат больше молибдена, чем изверженные, особенно им богаты глины, глинистые сланцы, покровные ивалунные суглинки; мало молибдена в песчаных и супесчаных породах. Аномально высокие концентрации молибдена в водах связаны с продуктами окисления сульфидных молибденовых руд, образующихся в условиях окисления под воздействием кислородосодержащих грунтовых вод.
Медь. Законы миграции меди довольно сложны. Разная валентность меди (Cu+ и Cu++) определяет большое влияние окислительно-восстановительных условий на миграцию этого элемента. Соединения одновалентной меди нерастворимы, а среди солей двухвалентной меди имеются как легкорастворимые (CuSO4), так и трукднорастворимые. Важнейшими осадителями иона Сu++ являются СО3--, РО4--, VO4---, H2S, SiO2. Медь легко сорбируется отрицательно заряженными коллоидами, что также ограничивает миграцию этого элемента. Важнейшими рудными минералами меди являются халькопирит (СuFeS2), ковелин (СuS), борнит (Сu5FeS4) и другие сульфиды.
Количество меди в водах лимитируется величиной рН. Медь становится неустойчивой и выпадает из растворов уже при рН = 5,3. Поэтому в водах, имеющих нейтральную или близкую к нейтральной реакцию, содержание меди выражается весьма малыми величинами (1 —100 мкг/л).Повышенные и высокие ее содержания наблюдаются лишь в непосредственной близости от медно-рудных месторождений. В кислых рудничных водах количество меди может составлять десятки и сотни миллиграммов на лето. При удалении от рудного тела, благодаря взаимодействию вод с вмещающими породами, происходит резкое уменьшение кислотности воды, что приводит к выпадению меди из раствора.
Источником меди в подземных водах являются горные породы. Высокие концентрации этого компонента связаны с интенсивно окисляющимися рудными телами (медноколчеданными и др.). Наибольшие количества меди наблюдаются в основных изверженных породах, прочие типы пород содержат близкие, относительно невысокие количества меди.
Из осадочных пород больше всего меди в покровных и лессовидных суглинках, меньше ее в моренных суглинках и карбонатных породах, еще меньше — в песчаных породах.
Почвы, лежащие на продуктах выветривания основных изверженных пород, на покровных и лессовидных суглинках, могут быть обогащены медью.
Основная литература: ОЛ 1 [58-74], 3 [45-58].
Дополнительная литература: ДЛ 1 [28-32].
Контрольные вопросы:
1. Какие элементы относятся к микроэлементам?
2. В каком количестве микроэлементы бывают в воде?
3. Как подразделяются микроэлемента по Алекину?
9 – лекция: ПОИСХОЖДЕНИЯ МИКРОЭЛЕМЕНТОВ В ПОДЗЕМНЫХ ВОДАХ.
Свинец. Широкому распространению ионов свинца в природных водах способствует то, что этот элемент в форме двух валентного иона может находиться при весьма высоких значениях рН (до 10,5). Однако концентрация свинца при прочих равных условиях резко снижается в нейтральных и слабощелочных растворах (при рН>7). Максимальные количества свинца обычно обнаруживаются в водах кислых, с рН<5,5. Миграционная способность свинца усиливается в присутствии ионов хлора (растворимость РЬС12—14,9 мг/л), а также в гидрокарбонатных водах с высоким содержанием СО-2.
Горные породы по отношению к свинцу проявляют большую сорбционную способность, чем к меди и цинкуЖ. Сыдыков приводит следующие средние значения содержания свинца по Западному Казахстану в трещинно грунтовых водах. Зеленокаменная зона — 13 мкг/л, Урало-Тобольская зона —7,6 мкг/л. В повышенных концентрациях (20—90 мкг/л) свинец установлен в подземных водах гранитойдов.
Исследования в Центральном Казахстане показали, что на месторождениях с хорошо развитой зоной окисления содержание свинца в водах рудных тел колеблется от 40 до 400 мкг/л, а на месторождениях со слабо развитой зоной окисления — от 40 до 100 мкг/л. Как в том, так и в другом случае свинец обнаружен во всех отобранных пробах. Содержание свинца в водах, циркулирующих во вмещающих породах, изменяется соответственно от 2 до 20 мкг/л и от 2 до 7 мкг/л при встречаемости 60—80%.
Свинец рассеян в земной коре в большей степени, чем медь. Источниками свинца в водах являются как эндогенные минералы — галенит (РbS), — так и экзогенные — англезит (PbSО4), церуссит (РbСО3) и ряд других. Растворимость природных соединений свинца очень низкая. Наиболее растворимы PbSО4 (42 мг/л) и РbСО3 (1,1 мг/л). Слабая растворимость вторичных минералов способствует устойчивости сульфидов свинца в зоне окисления.
Цинк. Эндогенный минерал цинка — сфалерит (ZnS) — в воде растворяется лучше, чем другие сульфиды. В зоне окисления сфалерит сравнительно быстро разлагается с образованием сульфатов и карбонатов. Почти все соединения цинка, кррме фтористого цинка (ZnF)относительно хорошо растворимы в воде. Вследствие этого, в отличие от меди и свинца, цинк широко распространен в водах нередко в высоких концентрациях. В сероводородной восстановительной среде цинк образует практически нерастворимый сульфид. Миграционная способность у цинка более высокая, чем у меди и свинца.
На месторождениях Центрального Казахстана с хорошо развитой зоной окисления цинк обнаруживается во всех водных пробах; количество этого элемента в водах рудных тел 300 — 1400 мкг/л. до 500 мкг/л в зависимости от размеров зоны окисления, близости рудных тел и условий, подземного стока вод.
По данным Ж. Сыдыкова, в трещинно-грунтовых водах Уралтау-Мугоджарской горноскладчатой области содержание цинка колеблется от единиц до 3000 мкг/л. При прочих равных условиях содержание цинка увеличивается с ростом минерализации подземных вод. Из изверженных пород наиболее богаты цинком основные породы. Меньше цинка содержится в кислых, и, особенно, в ультраосновных породах. Относительно богаты цинком глинистые породы, особенно покровные и лессовидные суглинки, мало цинка в песчаных и супесчаных породах.
Фосфор. Фосфор присутствует в водах главным образом в виде Н2РО+-- и НРО4--, причем первая форма преобладает в кислых водах, а вторая — в нейтральных и щелочных. Основным источником фосфора являются различные формы фосфата кальция (апатита) Са5(РО4)3С1 и Са5(РО4)3F которые распространены широко как в изверженных, так и в осадочных породах. В природных водах фосфор содержится в ничтожных количествах вследствие низкой растворимости его соединений и поглощения их живыми органнзмами. Содержание различных соединений фосфора составляет обычно сотые и десятые доли миллиграмма на литр и лишь в некоторых минеральных водах достигает единиц и даже десяткой миллиграммов на литр. Повышенное количество фосфора в водах ииогда указывает на их загрязнение, так как соединения фосфора относятся к числу продуктов разложения сложных органических веществ.
Мышьяк. Мышьяк в природных водах распространен незначительно, что объясняется низким средним содержанием его в горных породах. Миграция мышьяка в водах происходит, наиболее вероятно, в форме ионов НАsО3-- и НАsО3-. Максимальные из зафиксированных количеств мышьяка доходят до 40 мг/л (минеральные источники Южного Тироля). По данным Г.А.Голевой, распространение мышьяковистых вод в западных областях Украины совладает с районами мышьяковистого оруденения и связано с палеогеновыми осадочными песчано-глинистыми отложениями. Воды здесь обычно углекислые, минерализация их не превышает 3,0 г/л, содержание мышьяка составляет 1,0—1,6 мг/л.
Литий. Литий в природных водах присутствует обычно в малых концентрациях. В морской воде содержится около 0,1 мг/л лития. В подземных водах палеозойских отложений Московского артезианского бассейна содержание лития достигало значительных величин (44 мг/л), особенно в водах с повышенной минерализацией
За рубежом известны источники с содержанием лития 122 мг/л. В некоторых соляных озерах земного шара содержание лития достигает промышленных концентраций (оз. Сирлс в Калифорнии).
Источниками обогащения природных вод ионами лития могут быть изверженные породы. В процессе образования магматических пород литий концентрируется в кислых их разновидностях, особенно в последних стадиях кристаллизации магмы, образуя при этом литиевые минералы сподумен, лепидолит и другие. Одновременно с этим концентрируются щелочные металлы и особенно калии Подобные концентрации лития в породах развиты локально.
Стронций Низкая обычно концентрация стронция в природных водах объясняется слабой растворимостью его сернокислых соединений, в 1 л воды при 18°С растворяется 114 мг SrSO4. Главные минералы стронция — целестин (SrSO4) и стронцианит (SrСО3) - обладают ничтожной растворимостью (десятые доли миллиграмма на литр). Стронций называют «спутником» кальция по водной миграции, по для него характерна меньшая биологическая аккумуляция.
На миграцию стронция оказывает влияние химический состав вод. Стронций лучше мигрирует в хлоридных и гидрокарбонатных водах. В пресных водах содержание стронция обычно намного ниже 1мг/л и выражается в мкг/л. Однако встречаются районы с повышенной концентрацией этого иона в водах. Так, в Прикаспийской низменности, в речных водах содержание. Sr++ колеблется от 0,5 до 2,5 мг/л (среднее содержание 1.0 мг/л), в пресных и солоноватых грунтовых водах оно достигает 4,5 мг/л (среднее 1,2 мг/л), увеличиваясь вместе с ростом минерализации воды.
Источниками стронция в природных водах являются горные породы. В изверженных породах наиболее высокие количества связаны с образованиями остаточной магмы: прежде всего со щелочными породами (сиенитами), затем гранитами. Из осадочных отложений наибольшие количества стронция содержат гипсоносные породы высоко его содержание и в глинисто-карбонатных породах, а в глинах меньше. В доломитах содержание стронция очень мало, вероятно, в результате выноса стронция при доломитизации магнезиальными растворами.
Стронций обогащает осадки, выпадающие при испарения насыщенных рассолов замкнутых водоемов в условиях жаркого и сухого климата. Вхождение стронция в эти осадки регулируется, по-видимому, содержанием кальция.
Изучение распределения стронция в природных водах представляет специальный интерес для бальнеологии, биогеохимии, для выяснения фациальных условий осадконакопления, корреляции геологических разрезов и других целей.
Барий. Содержание бария в природных водах еще ниже, чем стронция. Растворимость ВаSО4 в воде при нормальных условиях всего 2,3 мг/л. Основные минералы бария — барит (ВаSO4, и витерит (ВаСО3) — очень слабо растворимы.
Среднее содержание бария в реках и грунтовых водах бассейна р. Вухтармы (Алтай) соответственно 24 — 107 мкг/л и 55—83 мкг/л. Такие концентрации бария в пресных водах являются значительно повышенными, что объясняется развитием горнорудной промышленности в Зыряновском районе.
По данным П.А.Удодова с соавторами, распространенность в природных водах Сибири бария сравнительно высокая. Максимальное содержание его — 2,64 мг/л — отмечено в Змеиногорском месторождении Рудного Алтая, минимальное — 0,1 мкг/л и среднее содержание бария — 5 мкг/л.
Никель. В кислых и слабокислых водах никель может мигрировать в форме Ni++. Согласно А. И. Перельману (1966), рН выпадения гидроокиси никеля Ni (ОН)2 равен 6,7. Согласно же П. А. Удодовву с соавторами [58], выпадение гидроокиси никеля при содержании 1,0 мкг/л наблюдается при рН=12. Никель легко адсорбируется глинами и образует растворимые комплексы с органическими соединениями. Сульфид никеля практически нерастворим, с чем связано выпадение никеля из раствора в восстановительной обстановке.
'Никель широко распространен в природных водах. В речных водах в среднем никеля содержится 3 мкг/л. В подземных водах, связанных с ультраосновными породами, содержание никеля, также как и кобальта и хрома, увеличивается, достигая 300 мкг/л. Согласно Ж.Сыдыкову. [53], содержание никеля в тре-щинпо-грунтовых водах Уралтауской зоны (Казахстан) изменяется от следов до 1100 мкг/л, аномальной считается величина более 60 мкг/л,
Кобальт. В природных водах кобальт обнаруживается реже, чем никель, что можно объяснить меньшой его миграционной способностью и низким содержанием кобальта в горных породах.
Вследствие способности кобальта менять валентность (Со++ и Со+++), его подвижность зависит от окислительно-восстановительных условии среды. По имеющимся данным, содержание ионов кобальта в водах рек СНГ выражается в мкг/л и долях микрограмма в литре. В трещинно-грунтовых водах основных и ультраосновных пород Уралтауской зоны содержание кобальта колеблется от следов до 25 мкг/л
Кобальт распространен в тех же породах и месторождениях, что и никель, и встречается с ним, всегда в парагенетчической ассоциации. Из изверженных пород максимальное количество кобальта содержат ультраосновные и основные породы, наиболее бедны им кислые породы. Осадочные породы — глины, сланцы — по содержанию кобальта занимают промежуточное положение между основными и кислыми изверженными породами. Очень мало его в песчаных породах, известняках и доломитах. Более обогащены кобальтом осадочные породы, образовавшиеся в восстановительных условиях в присутствии Н2S, в таких породах кобальт находится в форме малорастворимого сульфида.
Кобальт относится к числу биологически активных элементов. С недостаточным содержанием его в почвах связано недостаточное содержание кобальта в растениях, что способствует развитию малокровия у животных. Таежно-лесная нечерноземная зона как раз характеризуется как зона с недостаточном содержанием общего и подвижною кобальта в почвах.
Уран. Уран — редкий металл, относится к числу радиоактивных элементов. По распространенности он стоит в той же группе, что свинец, медь и молибден. Уран хорошо мигрирует в окислительной обстановке. В верхних частях земной коры под действием свободного кислорода происходит переход урана из первичных и частично вторичных минералов в подземные воды. В результате этого около урановых месторождений и рудопроявлении, омываемых подземными водами, образуются водные ореолы рассеяния, обогащенные ураном, а также радоном, радием и другими спутниками урана. В подземных водах в зонах интенсивного обмена, не встречающих на своем пути урановых руд, содержание урана составляет 0,1-1 мкг/л, реже 10 мкг/л и лишь в исключительных случаях 100 мкг/л. В ореолах рассеяния количество урана поднимается до 0,1-1 мг/л и очень редко до 50 — 100 мг/л.
Как установлено, на содержание урана в водах в значительной мере влияет климат. Его концентрация в водах возрастает в направлении от областей с влажным климатом к областям с более сухим климатом.
Основная литература: ОЛ 3 [58-74], 3 [45-58].
Дополнительная литература: ДЛ 1 [28-32].
Контрольные вопросы:
1. Как представляется растворимость микроэлементов?
2. Как микроэлементы перемещаются в воде?
3. Уран принадлежит к какому элементу?
Лекция 10. Оценка качества подземных вод для питьевого назначения.
Содержание: Разновидностиподземных вод характеризуются минерализацией и химическим составом.
В зависимости от степени их полезности используются по разному в производстве и в других целях. Они не во всех случаях могут отвечать на предъявляемые желания, в некоторых случаях они могут быть пригодными после «водоподготовки». С этим связано трудности нормирования воды. Только за последние десять лет с трудностями нормирования стали заниматься наука и производственные предприятия.
При формировании нормативов хозяйственно-питьевой воды учитываются степень минерализации (сухой остаток), состав макро-, и микрокомпонентов, физические качества и главное учитывается санитарные состояние.
Основные требования к питьевой воде:
1) вода должна быть прозрачная, несоленая, без запаха и освежающего вкуса;
2) в подземных водах обычно не должно превышать определенных пределов по минерализации и наличию растворенных веществ;
3) для состава с вредными веществами (медь, цинк, мышьяк и др.) для здоровья человека не должно превышать принятых пределов;
4) болезнетворных бактерий не должно быть.
Для оценки качества воды в основном производятся химические и бактериологические анализы. Нормативы питьевой воды формируются с участием авторитетных гигиенистами, конгрессменами и другими
ведущими предприятиями. Однако, еще и сегодня не существуют универсальные нормативы, характеризующие оптимальные физиологические качества воды. Для обеспечения центров водой качество воды определяется принятой нормой ГОСТ 2874- 73. Этот стандарт не распространяется на воды, потребляемых без трубопроводных сетей непосредственно из местных источников.
Основные поставленные требования к физическим свойствам воды – неприемлемая повышенная температура и отсутствие вкуса. Для подземных вод обеспечения городов, если цвет и наличие в них органических и механических примесей окажутся более 30 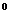 (по платиново-кобальтовой шкале), следует их очищать внесением в значительных размерах серной кислоты, алюминия и извести. Однако в северных районах, в целях питьевого применения, используются воды повышенной цветностью и наличием болотного запаха. Вкусовые свойства воды определяется концентрацией в ней растворенных солей (Таблица 12).
(по платиново-кобальтовой шкале), следует их очищать внесением в значительных размерах серной кислоты, алюминия и извести. Однако в северных районах, в целях питьевого применения, используются воды повышенной цветностью и наличием болотного запаха. Вкусовые свойства воды определяется концентрацией в ней растворенных солей (Таблица 12).
Пределы концентраций солей, определяющих вкус воды (мг/дм  ).
).
Таблица 12
| Соли | Едва ощущаемый вкус | Ощущаемый вкус | Неприятный вкус |
NaCl MgCl  NaSO NaSO 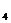 CaSO CaSO 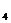 MgSO MgSO 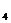 FeSO FeSO 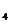 NaNO NaNO   NaHCO NaHCO  | 165 135 150 70 250 1.6 70 415 | 495 400 450 140 625 4.8 205 450 | 660 535 - - 750 - 345 - |
Основным критерием в качестве использования питьевой воды считается показатель степень минерализации. В соответствии стандарта СНГ степень минерализации не должна превышать 1 г/дм  .
.
Но при всех условиях население не возможно обеспечить водой такой минерализации. В некоторых районах используются воды с повышенной минерализацией не вредных для здоровья. По О.А.Алекину
для засушливых районов можно рассчитать граничные нормы согласно нижеприведенной градации:
хорошие 1.0 г/дм  ;
;
удовлетворительные 1.0 – 2.0 г/дм  ;
;
возможные 2.0 – 2.5 г/дм 
предельный 2.5 – 3.0 г/дм 
Тем не менее очень низкая минерализация (до100 мг/дм  ) понижает качество питьевой воды., а совсем без солей считаются вредными, потому что понижает внутриклеточное осматическое давление..
) понижает качество питьевой воды., а совсем без солей считаются вредными, потому что понижает внутриклеточное осматическое давление..
В общем это является гигиенической проблемой для Северных регионов, где используются очень
маломинерализованные растопленные воды льда. Так, к примеру на Кольском полуострове жесткость питьевой воды не превышает 0,36 мг-экв/л (1 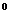 ), а по неприятному вкусу вода приближается к дистиллированной воде и поэтому для местных жителей возникает необходимость производства обеспечения повышения вкусовых качеств и минерального чередования. Для вод использования водопоя животных ставятся такие же вышеуказанные требования, хотя некоторые животные потребляют воду с повышенной минерализацией: верблюды и овцы пьют воду с преобладающими ионов Сl
), а по неприятному вкусу вода приближается к дистиллированной воде и поэтому для местных жителей возникает необходимость производства обеспечения повышения вкусовых качеств и минерального чередования. Для вод использования водопоя животных ставятся такие же вышеуказанные требования, хотя некоторые животные потребляют воду с повышенной минерализацией: верблюды и овцы пьют воду с преобладающими ионов Сl 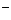 и Na
и Na 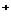 с минерализацией до 9.0 г/дм
с минерализацией до 9.0 г/дм  . Однако до сих пор не исследовано воздействие такой минерализации воды на организм животных.
. Однако до сих пор не исследовано воздействие такой минерализации воды на организм животных.
Таблица сравнений стандартов качества питьевой воды (по химическому составу) различных государств.
Таблица 13
| Вещество | Стандарты питьевой воды, мг/дм | |||
| СНГ ГОСТ 2874 - 73 | Международный 1963 | Европейский 1963 | США 1962 | |
| Бериллий Свинец Молибден Мышьяк Стронций Селен Хром Цианиды Кадмий Фтор Нитраты Барий Медь Цинк Фенольные вещества Железо Марганец Хлориды Сульфаты Остаток алюминия Гексаметофосфат Триполифосфат Поликриламид Уран Радий-226 Ки/л Стронций-90 Ки/л | 0,0002 0,1 0,5 0,05 2,0 0,001 - - - 0,7 – 1,5 10,0 - 1,0 5,0 отсутствие запаха 0,3 0,1 350,0 500,0 1000,0 0,5 3,5 2,0 1,7 1.2.10 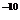 4.0.10 4.0.10 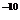 | - 0,05 - 0,05 - 0,01 0,05 0,2 0,01 1,0 – 1,5 45,0 1,0 1,5 15,0 0,002 1,0 0,5 600,0 400,0 1500,0 | - 0,1 - 0,2 - 0,05 0,05 0,01 0,05 1,5 50,0 - 3,0 5,0 0,001 0,1 0,1 350,0 250,0 - | - 0,05 - 0,05 - 0,01 0,05 0,2 0,01 0,7 – 1,7 45,0 1,0 1,0 5,0 0,001 0,3 0,05 250,0 250,0 500,0 |
При оценке качества хозяйственно-питьевой воды важен показатель жесткости, определяемая наличием в воде содержания ионов кальция и магния. Центры обеспечиваются водой, согласно ГОСТа с жесткостью не более 7,0 мг-экв/л (19.6 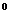 ). Использование воды с высокой жесткостью вызывают нежелательные процессы. При кипетении воды в посудах происходит выпадение кальция и магния в виде осадка. В жесткой воде трудно свариваются овощи и мясо, слабо заваривается заварка чая и больше расходуется мыло.
). Использование воды с высокой жесткостью вызывают нежелательные процессы. При кипетении воды в посудах происходит выпадение кальция и магния в виде осадка. В жесткой воде трудно свариваются овощи и мясо, слабо заваривается заварка чая и больше расходуется мыло.
В таблице 13 показаны нормативы для различных видов микрокомпонент. Обычно в природе у подземных пресных вод величины их состава не достигают цифыр, указанных в таблице. Проявление указанных концентраций – считается следствием загрязнения. Только в кислых водах состав микрокомпонентов может немного превышать величин стандарта. Интенсивность реакции для питьевой воды не ложна превышать пределов (рН) 6,5-9.5. При необходимых обстоятельствах для устранения в воде вредных веществ очищают от их окислением, осаждением и адсорбцией.
В санитарно экономическом отношении обращается большое внимание на два микрокомпонента – фтор и йод.
Фтор поступает в человеческий организм в основном с водой. Но в природной воде его очень мало. Высоко концентрированные фтором подземные воды – артезианские и грунтовые воды. Кариес
зубов порождается нехваткой фтора. На земном шаре эта болезнь одна из широко распространенная. Излишек фтора вызывает заболевание флюороз, разрушая зубы. Выяснено, что фтор улучшает физиологические процессы. Он влияет на рост человека и развитию формирования костей и выполняет
важную роль в обмене фосфором. Исходя из этого, возникает вопрос. Какая величина фтора полезна человеку?
В таблице стандарта питьевой воды йод не включен, так как сейчас в йодном балансе человека он занимает несущественное место. Но в человеческом организме нужное количество йода значительно больше поступающего водой. Так называемый эндемический зоб, разрушающий в общем организм человека, происходит от недостатка в пище йода. Однако, низкая концентрация йода в воде происходит из-за малой величины его в почве и местной пищевой продукции.
Оценка химического состава воды, обеспечиваемой питьевой водой, не ограничивается только важностью значений концентраций растворимых в ней компонентов, а значимостью комбинаций анионов с катионами, т.е. соединений солей. Приведем несколько сведений о значений натрия с хлором, употребляемых человеком с пищей. Уровень натрия с хлором в организме превышает по сравнению с другими минеральными соединениями. NaCl в плазме крови составляет 0,85%. Осмосное давление крови плазмы 7,6 – 8.1 атм, оно проникает с посредством растворенных солей. С помощью осмосного давления соль удерживает воду. Когда в организме повышается содержание слей увеличивается объем жидкости и плазмы. Эти два фактора обуславливают возможному подъему артериального давления. И наоборот, уменьшение солевой плотности приводит к консолидации жидкости и к снижению артериального давления. Поступление в организм с пищей лишней соли приводит к повышению кровяного давления.
Наблюдается связь между уровнем жесткости воды и смертью больных сердцем. Эта проблема изучалась шведскими врачами. Результаты этого исследования показали только одну зависимость между концентрацией ионов кальция в воде и сердечно- сосудистой системой. Эта причина еще не выяснена полностью, но замечены, что с умягчением воды уменьшается сердечно-сосудистое заболевание. Нижний предел концентрации кальция в воде соответствует содовому типу.
В оценке питьевой воды по химическому составу основное место занимает ее микробиологическое состояние. Опасным для питьевой воды является фекальное загрязнение. Для установления возможно загрязнения, исследуемых вод, производственными водами используются микробиологические показатели. Для централизованного водоснабжения вода поставляется с качеством по нормированному ГОСТу не более 3 –х колли индекс (1000 мл – число кишечных палочек), а колли титр (наличие в составе 1-ой кишечной палочки в малом объеме мл.) не менее 300. Если норма превышается, тогда вода на водостанциях хлорируется, озонируется и обезвреживаются соответственными путями.
Подземные воды играют большую роль в водоснабжении. Их, по сравнению с поверхностными водами, больше, поскольку обладают постоянством химического состава и низким уровнем загрязнения. Подземные воды считаются хорошими источниками для водоснабжения, закрыты водонепроницаемыми покровами и надежно сохранены от загрязнения. Они обычно выгодно отличаются прозрачностью и отсутствием микробов. При широком распространении подземных вод они широко используются в водоснабжении.
Основная литература: ОЛ 1 [38 - 58], 3 [27 - 44].
Дополнительная литература: 1 [28 - 32].
Контрольные вопросы:
1) Какие требования к питьевой воде?
2) Что называется агрессивностью воды?
3) Требования к физическим качествам воды?
Лекция-11. Оценка качества подземных вод для использования в технических и ирригационных целях.
В промышленных районах пользуются различными водами. Вода в технологии пищевой промышленности изготовления продукции используется прямо в качестве сырья. Для этих целей к воде предъявляются промышленные требования: в сахарном производстве- маломинерализованной, потому что излишние соли затрудняют процесс сахароварения; в пивоварении не должно быть СаSO 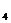 , в виноделии должны отсутствовать СаСl и MgCl, т. к. замедляют созревания закваски. Вода, используемая в системах охлаждения, чтобы не повлиять жесткостью на функционирования аппаратур
, в виноделии должны отсутствовать СаСl и MgCl, т. к. замедляют созревания закваски. Вода, используемая в системах охлаждения, чтобы не повлиять жесткостью на функционирования аппаратур
должна быть с низкой температурой. В фото, бумажном и текстильном производствах вода не должна содержать железо, марганец, серную кислоту, особенно радиактивные вещества. В производстве искусственного волокна требуется вода с слабой окисляемостью (кислород менее 2 мг/дм  ), низкая жесткость (до 0,64 мг-экв/дм
), низкая жесткость (до 0,64 мг-экв/дм  ).
).
Самые высокие требования к химическому составу воды предъявляются для использования в паровых котлах. В этих случаях вредны все компоненты воды, особенно жесткость.
При оценке технической воды, по сравнению с питьевой, главное принимается во внимание степень жесткости. Карбонатная жесткость определяется наличием кальция, магния и гидрокарбонатов, общая жесткость – концентрацией соединений катионов Са и Мg. Жесткость воды в соответствии введенного стандарта показывается соединениями Са 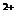 и Mg
и Mg 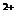 в 1 дм
в 1 дм  воды. Жесткость одного мг-экв. соответствует Ca
воды. Жесткость одного мг-экв. соответствует Ca 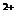 – 20.04 мг/дм
– 20.04 мг/дм  или Мg
или Мg 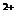 - 12.6 мг/дм
- 12.6 мг/дм  .
.
Значения жесткости воды следующие:
очень мягкая - 1.5 мг-экв/дм  ;
;
мягкая - 1.5 – 3.0 мг-экв/дм  ;
;
средняя - 3.0 – 6.0 мг-экв/дм  ;
;
жесткая - 6.0 – 10.0 мг-экв/дм 
очень жесткая - 10.0 мг-экв/дм 
В производстве и ряде технических процессов использовать жесткую воду неэффективно. Образование накипи понижает тепловую проводимость в производственных котлах и происходит высокий расход топлива. При 1 мм толщины накипи сжигание топлива превышает на 5%.
Образование накипи - сложный физико-химический процесс. В воде в процессе беспрерывного парообразования увеличивается концентрация растворенных солей и при достижении определенной предельной температуры соли выпадают в осадок. Обычно в осадок выпадают соли, отличающиеся малой растворимостью (СаСО  , МgСО
, МgСО  , СаSO
, СаSO 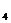 , СаSiO
, СаSiO  , МgSiO
, МgSiO  ). Сильно растворимые соли (NaCl, MgCl
). Сильно растворимые соли (NaCl, MgCl  , MgSO
, MgSO 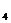 и др) не осаждаютя, потому что в котле предел их растворимости не хватает.
и др) не осаждаютя, потому что в котле предел их растворимости не хватает.
Химический состав накипи связан какие соли состоят в воде. При кипячении воды углекислый газ может полностью улетучится, и тогда гидрокарбонаты кальция и магния превращаются в слаборастворимые карбонаты:
Са(НСО  )
)  ↔ СаСО
↔ СаСО  +
+  Н
Н  О + СО
О + СО 

Мg(HCO  )
)  ↔ MgCO
↔ MgCO  + Н
+ Н  О + СО
О + СО 

потом карбонат кальция подвергается гидролизу:
Mg(HCO  )
)  + H
+ H  O ↔ MgOH
O ↔ MgOH  + CO
+ CO 

В этих условиях твердые осадки могут иметь различное физическое строение – от аморфного тверже порошка до правильных кристаллов. Если в воде большое количество кальция сульфата, тогда образуются гипсы. При наличии в составе воды окисла натрий кремния и также соли окисла кремния, тогда в котле происходит взаимодействия кальция и магния между сульфатами, в результате чего формируются слаборастворимые силикаты, например:
СаСО  + Na
+ Na  SiO
SiO  = CaSiO
= CaSiO  + Na
+ Na  SO
SO 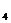 /
/
Накипи формируются солями кальция и силикатами магния, окислами кремния или силикатами. Особенности этих солей, как малорастворимые, с повышением температуры совсем не растворяются. Накипи окислов кремния для паровых котлов очень опасные, потому что нагревание котла может привести к взрыву. Неподходящие воды для питания паровых котлов, требуются смягчивать. Этот процесс понижения жесткости воды может называться как уменьшение в воде концентрации кальция и магния.
Для смягчении воды имеются различные методы: термические, химические с помощью катионов (содовая-известковая) и др.
Подземные воды бывают агрессивными к бетону, железобетону и металлам. Агрессивность воды в основном определяется ионами водорода (кислые воды), сульфатами с магнием при свободной углекислоты. ГОСТ 4796-49 подразделяет агрессивность на пять вида.
Щелочная агрессивность воды определяется степенью карбонатной агрессивности. Вода в сильно водопроводящих породах считаются агрессивными с карбонатной жесткостью до 2.14 мг-экв/дм  (6
(6 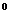 ) для портландцемента и до 1.07 мг-экв/дм
) для портландцемента и до 1.07 мг-экв/дм  (3
(3 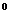 ) для шлакопортландцемента.
) для шлакопортландцемента.
Общая кислотная агрессивность воды определяется величиной содержания ионов водорода (по степени рН). Для вышесказанных цементов воды с карбонатной жесткостью в сильно вдопроводимых породах считаются агрессивными когда: а) карбонатная жесткость < 8.6 мг-экв/дм  и рН <7; б) карбонатная агрессивность > 8.6 мг-экв/дм
и рН <7; б) карбонатная агрессивность > 8.6 мг-экв/дм  при рН < 6.7. В слабо водопроводимых породах вода агрессивная при рН < 5.0.
при рН < 6.7. В слабо водопроводимых породах вода агрессивная при рН < 5.0.
Углекислая агрессивность воды определяется наличием в воде углекислого газа. Вода в сильноводороводимых породах считается для многих цементов агрессивной, если в составе уравнения а [Са 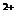 ] + в, много свободной углекислоты (а и в – установленные коэффициенты по таблице в МЕСТ – 4796-49 в зависимости от количества ионов Сl
] + в, много свободной углекислоты (а и в – установленные коэффициенты по таблице в МЕСТ – 4796-49 в зависимости от количества ионов Сl 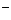 + SO
+ SO 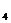 и степени карбонатной жесткости). Агрессивная СО
и степени карбонатной жесткости). Агрессивная СО  опасная при 3 мг/дм
опасная при 3 мг/дм  , малоопасной при 8.3 мг/дм
, малоопасной при 8.3 мг/дм  . В слабопроводимых породах агрессивные свойства не нормируются.
. В слабопроводимых породах агрессивные свойства не нормируются.
Сульфатная агрессивность воды определяется по МЕСТ 4796-49 в зависимости от состава бетона. В высоко водопроводимых породах воды считаются агрессивными для портланцемента, если в составе воды иеются ионы (мг/дм  ):
):
Cl 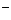 SO
SO 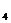

0-3000 250-500
3001-5000 501-500
более 5000 более 1000
В слабо водопроводимых породах вода считается агрессивной для портландцемента при содержании в ней иона SO 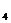
 более 1000 мг/дм
более 1000 мг/дм  .
.
Магнезиальная агрессивность воды связана с наличиеминов Mg 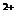 . В высоко водопроводимых
. В высоко водопроводимых
породах вода оказывается агрессивной к портандцементу при содержании иона Мg 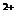 более 5000 мг/дм
более 5000 мг/дм  ; ниже приведены значения (мг/дм
; ниже приведены значения (мг/дм  ) ионов агрессивные для портландцемента:
) ионов агрессивные для портландцемента:
SO 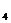
 Mg
Mg 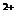

0-1000 > 5000
1000-2000 3000-5000
2000-3000 2000-3000
3000-4000 1000-2000
Воды в слабо водопроводимых породах на агрессивность не нормируется.
Интенсивность углекислой, сульфатной и другой агрессивности зависит от скорости течения агрессивной воды.
Основная литература: ОЛ 1 [38-58], 3 [27-44]..
Дополнительная литература: ДЛ 1[28-32].
Контрольные вопросы:
1) Что называют накипью?
2) Что называют агрессивностью?
3) Какие требования для производственных вод?
12 - лекция. ИЗОТОПНЫЙ СОСТАВ ВОДОРОДА, КИСЛОРОДА И СЕРЫ
Изотопный состав воды. Под термином «изотопный состав вод» понимают изотопные составы водорода и кислорода, входящих в состав молекулы воды.
При изотопном анализе воды физические константы исследуемой воды сравниваются с константами пресной речной воды, принимаемой за эталон. При оценке суммарного изотопного состава той или иной воды поступают так: если исследуемая вода тяжелее стандартной, то перед разностью плотностей, выражаемой вставят плюс, если легче — минус. Гамма же определяется в единицах плотности: 1γ равна 0,000001 единиц плотности и эквивалентна 9,3 -10-4 мол % дейтерия или избыточному его содержанию сверх стандартного на 6,1%.
Согласно данным различных авторов, суммарная изотопная плотность природных вод испытывает колебания от минус 23 до плюс 21γ. Значения плотности от 0 до минус 3,5γ свойственны подземным водам вблизи области питания и на небольших глубинах. Утяжеление подземных вод в зоне свободного водообмена невелико и близко к речному стандарту. С увеличением закрытости недр количество тяжелых изотопов в воде при прочих равных условиях обычно возрастает, достигая + 7 -8γ. Большое уплотнение свойственно поровым водам (горным растворам) и капельно-жидким включениям в минералах. У них отмечается плотность + 8γ, иногда -14,4γ.
По суммарному изотопному составу различают следующие типы природных вод: 1) легкие воды, снеговые и ледниковые (минус 3, минус 23 гаммы); 2) нулевые воды больших рек Русской равнины ( 0); 3) тяжелые воды озер и морей (плюс 2, плюс 3); 4) собственно тяжелые воды нефтяных месторождений (плюс 3, плюс 16 и выше); 5) смешанные воды сложного генезиса (0,
0); 3) тяжелые воды озер и морей (плюс 2, плюс 3); 4) собственно тяжелые воды нефтяных месторождений (плюс 3, плюс 16 и выше); 5) смешанные воды сложного генезиса (0,  1,
1,  2 гаммы).
2 гаммы).
Воды Антарктиды (снег и фирн) относятся, по-видимому, к самым легким водам на Земле. Суммарный изотопный состав большинства их проб оказался ниже минус 13 и достигает минус 23,1 гамм. Предполагают, что льды Антарктиды образовались в результате многократных фракционных перегонок атмосферных осадков, сформировавшихся над океаном, которые проникли вглубь Антарктиды на значительных высотах. Большая плотность холодного воздуха нижних горизонтов препятствовала проникновению паров воды непосредственно из океана.
Л. И. Бродский указывает, что большинство элементов в природных условиях существует в виде механических смесей изотопов. Соответственно этому атомный вес таких элементов является арифметическим средним из атомных весов их изотопов. Эти средние атомные веса отличаются большей частью замечательным постоянством. Казалось бы в геологическом масштабе времени подобное постоянство не должно сохраняться, но изменению изотопного состава противодействуют природные фракционирующие процессы. Последние недостаточно односторонне направлены для того, чтобы вызывать значительное разделение изотопов.
Нарушения постоянства атомных весов наблюдаются в двух случаях: 1) если тот или иной изотоп является продуктом, радиоактивного распада; 2) если элементы в природных условиях подвержены интенсивному направленному круговороту или односторонней миграции, как например: водород и кислород воды, углерод органического мира, сера и т. д. В первом случае наблюдаются резкие различия в изотопном составе, во втором — незначительные. Какие же природные процессы вызывают фракционирование изотопов? К числу их относятся повторяющиеся процессы растворения и кристаллизации, испарения и конденсации, диффузия, различные реакции химического взаимодействия, в частности реакции изотопного обмена, и ряд других. Особая роль в разделении изотопов принадлежит процессам, происходящим при участии живых организмов — фотосинтезу. Дыханию и прочее. Поэтому испарению отводится главная роль в разделении изотопов. Другие факторы имеют второстепенное значение.
Изотоп водорода. В последнее время особое внимание уделяется изучению изотопного состава водорода с целью использования его для решения некоторых теоретических и практических вопросов гидрогеологии. Результаты определения изотопов водорода выражаются по-разному: в мол % D2O, ат.% D, в гаммах. (1γ эквивалентна 0,000927 ат.%), в виде относительной величины, причем за стандарт, приравненный 1, принимается обычно вода Московского водопровода, абсолютная концентрация дейтерия" в которой составляет 0,0147  0,0005 мол. %,
0,0005 мол. %,
По данным многочисленных определений, воды рек средней полосы Европейской территории СНГ характеризуются содержанием дейтерия, близким к 1. Меньше дейтерия в поверхностных водах Сибири: р. Иртыш 0,96; оз. Байкал 0,95:. р. Слюдянка 0,94; р. Енисей 0,93, — что объясняется, по всей вероятности, уменьшением эффекта фракционирования при испарении с понижением температуры. В водах морей и бессточных озер аридных областей концентрация дейтерия намного превышает принятый стандарт: Каспийское море от 1,08 до 1.09, Японское море 1,10, Черное море 1,11, Красное море 1,13.
Вариации изотопного состава водорода подземных вод из водоносных горизонтов различного возраста неодинаковых по геологическому строению артезианских бассейнов не выходят за пределы изменений дейтерия в поверхностных водах. Лишь в некоторых пробах найдено содержание дейтерия, более свойственное морским водам. Воды артезианских бассейнов Средней Азии характеризуются низкими концентрациями дейтерия, что можно поставить в связь с питанием их талыми водами высокогорных снегов, тоже содержащих относительно мало дейтерия (0,91—0,93). В водах артезианских бассейнов Азербайджана, Поволжья, Краснодарского края больше дейтерия, поскольку в области питания развиты воды с концентрацией дейтерия, близкой к 1.
В действительности наблюдается закономерное изменение концентрации дейтерии в водах артезианских бассейнов в зависимости от не в интенсивности водообмена, а в генезисе воды. В нижних непромытых горизонтах обычно сохраняются седиментационные воды морского генезиса. В зоне замедленного водообмена еще сохраняется примесь морских вод. Брезгунов с соавторами по содержанию дейтерия произвели ориентировочный подсчет пропорций седиментационных и инфильтрационных вод. При благоприятных условиях морские воды иногда проникают в верхнюю зону, свободного водообмена и тогда здесь будут фиксироваться повышенные концентрации дейтерия.
Надо иметь в виду, что минерализованные воды континентального засоления, образовавшиеся путем испарительного концентрирования, будут всегда обогащены дейтерием, независимо от того, в какой гидродинамической зоне они будут находиться.
Изотоп кислорода. Обогащение вод тяжелыми изотопами кислорода приписывается одному изотопу О18, хотя в значительно меньших количествах существует еще один тяжелый стабильный изотоп О17. Найдено, что изотопный состав кислорода в природных водах может значительно отличаться. Например, разность плотностей воды. Мертвого моря и одного из глетчеров Канады за счет различия концентрации О18 достиг
 2018-02-14
2018-02-14 4295
4295
