Равновесное состояние системы при постоянной температуре и объеме можно
охарактеризовать минимумом свободной энергии Гельмгольца  где
где
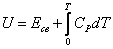 − внутренняя энергия, равная сумме энергии связи частиц
− внутренняя энергия, равная сумме энергии связи частиц  и тепловой энергии, определяемой температурой T и теплоемкостью
и тепловой энергии, определяемой температурой T и теплоемкостью  .
.  – энтропия системы.
– энтропия системы.
Внутренняя энергия U и энтропия S с повышением температуры растут и при температуре плавления  ,испытывают скачки, обусловленные теплотой плавления Q. Ее наличие показывает, что речь идет о фазовом переходе I рода.
,испытывают скачки, обусловленные теплотой плавления Q. Ее наличие показывает, что речь идет о фазовом переходе I рода.
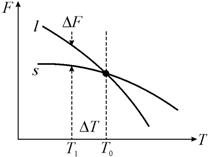
Кривые солидуса s и ликвидуса l (рис. 13.12) для свободной энергии твердого тела и жидкой фазы убывают из-за влияния энтропийного члена. Для жидкой фазы скорость убывания больше, чем для твердой, за счет того, что степень неупорядоченности жидкости больше, чем у твердого тела. Поэтому ниже точки пересечения кривых s и l устойчива твердая фаза, а выше – жидкая. Точка пересечения не является особой точкой, поэтому возможны переохлаждение расплава и перегрев кристалла.
|
| Рис. 13.12. Вид зависимости свободной энергии от температуры для твердой – S и жидкой – l фаз |
При температуре  в равновесии находятся две фазы: расплав и кристалл. При температуре
в равновесии находятся две фазы: расплав и кристалл. При температуре 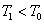 идет фазовое превращение расплава в кристалл. Переохлаждение на величину
идет фазовое превращение расплава в кристалл. Переохлаждение на величину  (степень переохлаждения) приводит к тому, что расплав (или фаза β) становится метастабильной по отношению к кристаллу (фаза α). Для начала спонтанного процесса кристаллизации необходимо возникновение центра кристаллизации, или кристаллического зародыша.
(степень переохлаждения) приводит к тому, что расплав (или фаза β) становится метастабильной по отношению к кристаллу (фаза α). Для начала спонтанного процесса кристаллизации необходимо возникновение центра кристаллизации, или кристаллического зародыша.
Пусть Δ F – увеличение свободной энергии при образовании новой фазы (твердой). При этом полное превращение энергии системы определяется двумя факторами: уменьшением свободной энергии при росте объема, занимаемого новой фазой  (V – объем новой фазы, Δ f – свободная энергия единицы объема), и
(V – объем новой фазы, Δ f – свободная энергия единицы объема), и 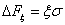 – доля, обусловленная ростом поверхности раздела двух фаз (s – свободная энергия единицы поверхности;
– доля, обусловленная ростом поверхности раздела двух фаз (s – свободная энергия единицы поверхности;  – площадь этой поверхности)
– площадь этой поверхности)
 . .
| (13.45) |
Площадь поверхности и объем вновь образовавшегося кристаллического зародыша соответственно  и
и  , где R – радиус зародыша. Тогда для зародыша радиусом R находим
, где R – радиус зародыша. Тогда для зародыша радиусом R находим
 . .
| (13.46) |
Первый член в уравнении (13.46) равен уменьшению внутренней объемной энергии зародыша за счет выделения теплоты кристаллизации q, приходящейся на один зародыш, второй − обусловлен работой образования поверхности зародыша площадью  , совершаемой за счет внутренней энергии системы. Второй член в уравнении (13.46) пропорционален поверхностному натяжению s на границе раздела фаз. Объем зародыша v мал по сравнению с объемом всего расплава V. Это позволяет пренебречь изменением объема системы при образовании зародыша. В этом случае процесс кристаллизации является изотермическим и изохорным, и равновесие системы определяется минимумом свободной энергии. Изменение свободной энергии Гельмгольца при образовании зародыша
, совершаемой за счет внутренней энергии системы. Второй член в уравнении (13.46) пропорционален поверхностному натяжению s на границе раздела фаз. Объем зародыша v мал по сравнению с объемом всего расплава V. Это позволяет пренебречь изменением объема системы при образовании зародыша. В этом случае процесс кристаллизации является изотермическим и изохорным, и равновесие системы определяется минимумом свободной энергии. Изменение свободной энергии Гельмгольца при образовании зародыша
 . .
| (13.47) |
Для зародыша радиуса R находим
 . .
| (13.48) |
Формула (13.48) показывает, что равновесие «кристалл–расплав» является неустойчивым.
Зависимость изменения свободной энергии зародыша от его радиуса Δ F (R) имеет максимум при критическом значении радиуса зародыша  (рис. 13.13), который определяется равенством
(рис. 13.13), который определяется равенством
 , ,
| (13.49) |
где  – критический размер зародыша.
– критический размер зародыша.

|
| Рис. 13.13. Изменение свободной энергии при возникновении кристаллического зародыша имеет максимум, отвечающий критическому размеру зародыша |
Все центры кристаллизации с размерами меньше критического  неустойчивы, т. к. при их росте свободная энергия должна увеличиваться. Все кристаллические зародыши с размерами больше
неустойчивы, т. к. при их росте свободная энергия должна увеличиваться. Все кристаллические зародыши с размерами больше  будут расти, поскольку при этом свободная энергия системы уменьшается.
будут расти, поскольку при этом свободная энергия системы уменьшается.
Максимум кривой определяет работу образования зародыша
 . .
| (13.50) |
Она равна 1/3 поверхностной энергии зародыша.
Работа образования зародышей новой фазы значительно уменьшается при их возникновении на стенках сосуда или поверхностях частичек примесей.
Рассмотрим образование из пара (фаза I) сферического зародыша жидкости АВС (фаза II) на плоской поверхности фазы III, граничащей с фазой I (рис. 13.14).

|
| Рис. 13.14. Образование сферического зародыша жидкой фазы на границе раздела двух сред [55] |
Работа образования зародыша в случае его возникновения на стенке равна 
 , ,
| (13.51) |
где  – поверхностное натяжение на границе «зародыш – питающая фаза I»,
– поверхностное натяжение на границе «зародыш – питающая фаза I»,  – поверхностное натяжение на границе «зародыш – стенка»,
– поверхностное натяжение на границе «зародыш – стенка»,  – то же на границе «стенка – питающая фаза I». В условиях равновесия силы поверхностного натяжения уравновешивают друг друга, т. е.
– то же на границе «стенка – питающая фаза I». В условиях равновесия силы поверхностного натяжения уравновешивают друг друга, т. е.
 , ,
| (13.52) |
где  – краевой угол.
– краевой угол.
Площадь  сферического сегмента АВС и
сферического сегмента АВС и  – площадь основания сегмента, соответственно равны
– площадь основания сегмента, соответственно равны
 ; ;
 . .
| (13.53) |
Отсюда работа образования зародыша
 . .
| (13.54) |
При отсутствии смачивания угол  равен p (ртуть на поверхности стекла) и работа по образованию свободного сферического зародыша
равен p (ртуть на поверхности стекла) и работа по образованию свободного сферического зародыша  , т. е. равна 1/3 поверхностной энергии капли. При частичном смачивании (
, т. е. равна 1/3 поверхностной энергии капли. При частичном смачивании (  ) работа уменьшается, а при полном смачивании (
) работа уменьшается, а при полном смачивании (  ) равна нулю. Последние два фактора в сравнении с первым говорят о том, что работа образования зародыша на поверхности раздела меньше работы образования свободного зародыша. Эти выводы справедливы и для случая образования кристаллических зародышей, что объясняет большую роль стенок и частичек примесей в ускорении процесса кристаллизации.
) равна нулю. Последние два фактора в сравнении с первым говорят о том, что работа образования зародыша на поверхности раздела меньше работы образования свободного зародыша. Эти выводы справедливы и для случая образования кристаллических зародышей, что объясняет большую роль стенок и частичек примесей в ускорении процесса кристаллизации.
Работа образования зародыша особенно сильно снижается в присутствии частиц изоморфных примесей или кристаллов, имеющих с образующимся сходное строение по каким-либо граням. Это используется, например, при выращивании кристаллических пленок на подложках из тех же или сходных по структуре кристаллов.
 2018-02-20
2018-02-20 1316
1316
