Наблюдения показывают, что при охлаждении расплава до температуры кристаллизации переход в твердое состояние происходит не мгновенно и не одновременно во всем объеме. Кристаллизация развивается из одного или нескольких центров и распространяется с конечной скоростью, захватывая постепенно весь объем неустойчивой фазы. Кинетика процесса кристаллизации описывается двумя величинами:
• скоростью образования центров кристаллизации С в единице объема за единицу времени;
• линейной скоростью роста 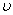 кристалла, равной скорости перемещения растущей грани кристалла по нормали к этой грани.
кристалла, равной скорости перемещения растущей грани кристалла по нормали к этой грани.
Кривые 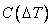 и
и 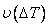 имеют максимумы, что объясняется тем, что при малых степенях переохлаждения D Т наблюдается возрастание скорости ростакристалла
имеют максимумы, что объясняется тем, что при малых степенях переохлаждения D Т наблюдается возрастание скорости ростакристалла 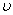 и скорости образования центров кристаллизации С, а при больших степенях переохлаждения D Т, в результате роста вязкости, – их падение.
и скорости образования центров кристаллизации С, а при больших степенях переохлаждения D Т, в результате роста вязкости, – их падение.
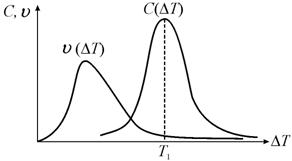
Часто максимумы 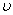 и С довольно сильно сдвинуты относительно друг друга по шкале температур (рис. 13.15). При этом центры кристаллизации в области максимума скорости роста еще не образуются, а в области максимума скорости образования центров кристаллизации линейная скорость роста уже мала. Это тормозит суммарную скорость кристаллизации, и полное время этого процесса растет. Кристаллизация идет только за счет пересечения ветвей. Ее можно ускорить, если, охладив расплав до температуры максимума кривой С (D Т), выждать некоторое время, пока не образуются центры кристаллизации, а затем, нагрев систему, вернуть ее в область максимума скорости роста.
и С довольно сильно сдвинуты относительно друг друга по шкале температур (рис. 13.15). При этом центры кристаллизации в области максимума скорости роста еще не образуются, а в области максимума скорости образования центров кристаллизации линейная скорость роста уже мала. Это тормозит суммарную скорость кристаллизации, и полное время этого процесса растет. Кристаллизация идет только за счет пересечения ветвей. Ее можно ускорить, если, охладив расплав до температуры максимума кривой С (D Т), выждать некоторое время, пока не образуются центры кристаллизации, а затем, нагрев систему, вернуть ее в область максимума скорости роста.
|
| Рис. 13.15. Кривые линейной скорости роста и скорости образования центров кристаллизации |
Инверсия в химии, 1) изменение конформации циклической молекулы, в результате чего меняется ориентация заместителя относительно кольца. Например, метилциклогексан существует в виде равновесной смеси двух конформаций с преобладанием формы II:
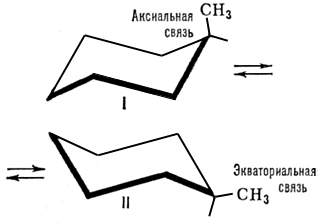
Частота инверсии зависит от характера заместителей и температуры. См. Стереохимия, Конформационный анализ.
2) Переход конфигурации молекулы, содержащей трёхвалентный «пирамидальный» атом (например, азота или мышьяка), в зеркально противоположную. Так, для молекулы с трёхвалентным азотом формы I и II — антиподы оптические:
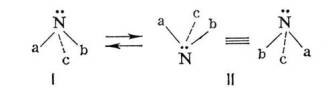
где а, b, с — различные атомы или группы атомов. Энергетический барьер инверсии обычно невысок и зависит от температуры и характера а, b, с. По отношению к атому углерода («тетраэдрический» атом) обычно употребляется термин «обращение конфигурации» (см. Изомерия).
3) Инверсия сахаров — гидролиз сахарозы (например, свекловичного сахара), сопровождающийся изменением направления вращения плоскости поляризованного луча света раствором сахара. См. Сахара.
Б. Л. Дяткин.
ПИРАМИДАЛЬНАЯ ИНВЕРСИЯ,
внутримол. переход конфигурации
молекулы, содержащей. трехкоординац. пирамидальный атом, напр. N, P,
As, С-, Si-, из одной энантиомерной формы в другую. Осуществляется
через промежут. форму с плоской конфигурацией (т.е. путем политопной перегруппировки):
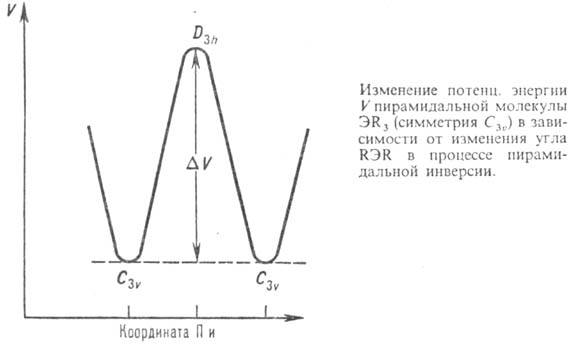
Высота энергетич. барьера
П. и D V (см. рис.) зависит от природы пирамидального атома и заместителей.
Так, энергетич. барьер П. и. NH3 ~ 24,7 кДж/моль (время жизни пирамидальной
конфигурации т = 2,5· 10 -11 с). Он мало меняется при замещении
атомов H на группы с близкой электроотрицательностью [ ~ 9,6 кДж/моль для CH3NH2,
18,4 кДж/моль для (CH3)2NH], резко уменьшается в случае
более электроположит. лигандов (напр., LiNH2) и повышается в случае
более электроотрицат. заместителей (-251,4 кДж/моль для NF3).
С увеличением порядкового
номера элемента в одной подгруппе барьеры П. и. однотипных соед. (а следовательно,
и устойчивость пирамидальной конфигурации) резко возрастают, что позволяет препаративно
разделять энантиомеры, напр. в случае CH3(C3H7)PC6H5.
Для пирамидальной конфигурации PH3 t = 2,3·10-6 с, для
(СН3)3Р-2 ч, для AsH3-1,4 ч. Синтезированы
также оптически активные соед. As(III), сульфониевые соли, сульфоксиды, эфиры
суль-финовой к-ты и сульфиниламины.
Электронные факторы, стабилизирующие
переходное состояние 11. и., могут изменить геометрию молекулы от пирамидальной
до плоской. Напр., барьер П. и. H2NCHO (плоская конфигурация) ~4,6
кДж/моль, что объясняется p-p -сопряжением в плоском переходном состоянии.
Этот эффе-кт обусловливает также плоскую геометрию пиррол лов и соед., содержащих
связи Si—N или P-N.
При включении атома Э в
малый цикл (азиридины) или пятичленный цикл (пирролидины) барьер П. и. повышается
из-за дестабилизирующих плоское переходное состояние угловых напряжений (напр.,
в N-метилазириди-не барьер П. и. ~89,2 кДж/моль). Тот же эффект отмечен для
изопропилоксираниевого иона и циклопропилид-аниона.
Впервые соед. с пирамидальной
конфигурацией молекул в оптически активной форме - основание Трегера (ф-ла I)-получил
В. Прелог в 1944.
Лит.. Вейлстеке
А., Основы теории квантовых усилителей и генераторов, пер. с англ., M., 1963;
Зефиров H. С., "Ж. Всес. хим. об-ва им. Д. И. Менделеева" 1977,
т 22, № 3, с. 261-74; Потапов В. M., Стереохимия, 2 изд., M., 1988. М.Е.Клецкий.
Эвтектика этононвариантная (при постоянном давлении) точка в системе из n компонентов, в которой находятся в равновесии n твердых фаз и жидкая фаза. Эвтектическая композиция представляет собой мелкодисперсную механическую смесь фаз, плавящихся и кристаллизующихся одновременно при минимальной температуре существования жидкой фазы для данной системы.
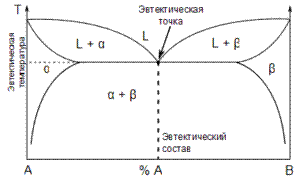
Рис.. Бинарная фазовая диаграмма с эвтектическим превращением
Добавляя или отводя тепло, можно изменить пропорцию между кристаллическими фазами и расплавом в эвтектической точке без изменения температуры. После кристаллизации эвтектика становится механической смесью фаз — твёрдой эвтектикой.
Эвтектика является пересечением поверхностей насыщения участвующих кристаллических фаз, находящихся в равновесии с расплавом при минимальной температуре плавления. Если отводится соответствующее количество тепла, то расплав эвтектического состава при кристаллизации в равновесных условиях в точке эвтектики даст все кристаллические фазы, участвующие в системе. Если же при сохранении эвтектической температуры в достаточном количестве подводится тепло, то смесь фаз, отвечающая эвтектическому составу, в равновесных условиях полностью расплавится.
 2018-02-20
2018-02-20 401
401








