В инженерной практике часто приходится иметь дело с газообразными веществами, близкими по свойствам к идеальным газам и представляющими собой механическую смесь отдельных компонентов различных газов, химически не реагирующих между собой. Это так называемые газовые смеси. В качестве примера можно назвать воздух, продукты сгорания топлива в двигателях внутреннего сгорания, топках печей и паровых котлов, влажный воздух в сушильных установках и т. п.
Все зависимости, полученные выше для идеальных газов, справедливы и для их смесей, если в них подставлять газовую постоянную, молекулярную массу и теплоемкость смеси.
Закон Дальтона. Основным законом, определяющим поведение газовой смеси, является закон Дальтона: полное давление смеси идеальных газов p равно сумме парциальных давлений всех входящих в нее компонентов:
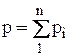
Парциальное давление рi, — давление, которое имел бы газ, если бы он один при той же температуре занимал весь объем смеси.
Способы задания смеси. Состав газовой смеси может быть задан массовыми, объемными или мольными долями.
Массовой долей gi называется отношение массы отдельного компонента Mi к массе смеси М:
gi = Mi / M.
Очевидно, что M = Σ Mi
и Σ gi = 1.
Массовые доли – безразмерные величины и часто задаются в процентах. Например, для сухого воздуха доля азота составляет 77%, а кислорода – 23%.
Объемная доля ri представляет собой отношение приведенного объема газа Vi к полному объему смеси V:
ri=Vi / V.
Приведенным называется объем, который занимал бы компонент газа, если бы его давление и температура равнялись давлению и температуре смеси.
Вычисление приведённого объема определяется из уравнения:
Vi / V = рi / р.
Просуммировав все компоненты смеси, получим с учетом закона Дальтона
Σ Vi = V, откуда Σ ri = 1.
Объемные доли также часто задаются в процентах. Для воздуха r O2 = 21 %, r N2 = 79%.
Иногда бывает удобнее задать состав смеси мольными долями. Мольной долей называется отношение количества молей Ni рассматриваемого компонента к общему количеству молей смеси N.
Мольная доля компонента будет равна Ni /N, а число молей смеси N = Σ Ni
Задание смеси идеальных газов мольными долями равнозначно заданию её объемными долями
Ni /N = Vi/V.
Газовая постоянная смеси газов. Просуммировав уравнения для всех компонентов смеси, получимгазовую постоянную смеси газов
RCM = Σ giRi = 8314 Σ (gi / μ i).
Смесь идеальных газов также подчиняется уравнению Клапейрона
pV = MRCMT.
Кажущаяся молекулярная масса смеси. Кажущаяся молекулярная масса смеси, заданная объемными долями, равна:
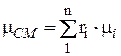 .
.
Теплоемкость смесей идеальных газов. Если смесь газов задана массовыми долями, то ее массовая теплоемкость с определяется как сумма произведений массовых долей на массовую теплоемкость каждого компонента, т. е.
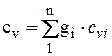 ,
, 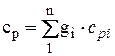 .
.
При задании смеси объемными долями объемная теплоемкость смеси
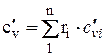 ,
, 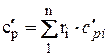 .
.
Аналогично мольная теплоемкость смеси равна произведению объемных долей на мольные теплоемкости составляющих смесь газов:
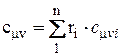 ,
, 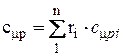 .
.
В сушильной технике в качестве рабочего тела широко используют влажный воздух, представляющий собой смесь сухого воздуха и водяного пара. Содержание водяного пара в атмосферном воздухе зависит от метеорологических условиях, а также от наличия источников испарения воды и колеблется в широких пределах: от малых долей до 4% по массе.
Обычно к влажному воздуху, пренебрегая незначительной погрешностью, применяют уравнение состояния для идеальных газовых смесей.
21. Массовая, объемная и мольная теплоемкость смеси газов.
22. Массовая, объемная и мольная теплоемкости.
23. Истинная и средняя теплоемкость.
24. Теплоемкость при постоянном объеме и постоянном давлении.
25. Уравнение Майера.
 2014-02-09
2014-02-09 4059
4059
