Из выражения (63) термического КПД следует, что
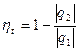 . (73)
. (73)
Но для обратимого цикла Карно термический КПД еще выражается через температуры источников теплоты:
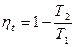 . (74)
. (74)
Из сравнения выражений (73) и (74) следует, что для цикла Карно
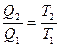 или
или 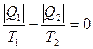 .
.
Но, учитывая, что отводимая теплота отрицательна, имеем:
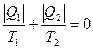 .
.
Или
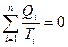 . (75)
. (75)
Выражение (75) служит для определения приведенной теплоты.
Таким образом, для каждого элементарного цикла Карно справедливо выражение (75), а для всего произвольного цикла:
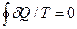 . (76)
. (76)
Уравнение (76), выведенное Клаузиусом в 1854 г., представляет собой математическое выражение второго закона термодинамики для произвольного обратимого цикла и называется первым интегралом Клаузиуса.
Если сопоставить уравнение (76) и выражение (60) получим:
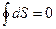 . (77)
. (77)
Выражение (77) показывает, что изменение энтропии замкнутых процессов или циклов равно нолю.
ИЗМЕНЕНИЕ ЭНТРОПИИ В НЕОБРАТИМЫХ ПРОЦЕССАХ
При прочих равных условиях работа, совершаемая необратимым процессом, меньше, чем обратимым, и, следовательно, 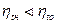 . Поэтому при наличии в цикле необратимых процессов:
. Поэтому при наличии в цикле необратимых процессов:
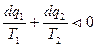 , (78)
, (78)
Или, после интегрирования по замкнутому контуру:
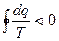 . (79)
. (79)
Пусть, например, в произвольном цикле, изображенном на рисунке 6, процесс 2-4-1 обратимый, а обозначенный пунктирной линией 1-3-2 необратимый.
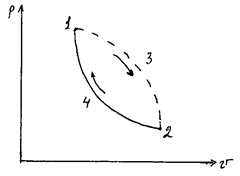
Рисунок 6 – Цикл
Полученный в результате этих процессов цикл будет необратимым, поскольку один из процессов цикла необратим. Тогда интеграл (79) с учетом выражения (78) можно представить в виде суммы интегралов:
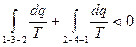 . (80)
. (80)
Так как процесс 2-4-1 обратимый, то второй интеграл, согласно выражению (60), равен разности 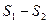 , поэтому неравенство (80) примет вид:
, поэтому неравенство (80) примет вид:
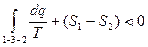 , (81)
, (81)
Или, после преобразования:
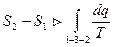 . (82)
. (82)
Знак неравенства (82) указывает на то, что в случае необратимого процесса интеграл в правой части его уже не выражает собой разности энтропий, а меньше нее, т.е.
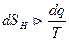 , (83)
, (83)
где 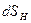 – элементарное изменение энтропии необратимого процесса.
– элементарное изменение энтропии необратимого процесса.
Таким образом, необратимость процесса 1-3-2 приводит к возрастанию энтропии.
ЭКСЭРГИЯ
Эксэргия или техническая работоспособность – максимальная работа совершаемая рабочим телом, если в качестве холодного источника теплоты принимается внешняя среда с температурой 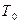 .
.
Различают эксэргию рабочего тела в потоке, эксэргию неподвижного рабочего тела и эксэргию теплоты.
Эксэргией рабочего тела, способной в той или иной мере превращаться в работу, является в случае потока энтальпия, а в случае неподвижного тела – внутренняя энергия.
Рассмотрим необратимый процесс передачи тепла Q от горячего тела с температурой 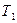 к холодному с температурой
к холодному с температурой 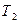 . Считаем, температуры
. Считаем, температуры 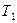 и
и 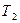 выше
выше 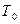 . В результате этого процесса изменение энтропии первого тела составит:
. В результате этого процесса изменение энтропии первого тела составит:
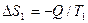 . (84)
. (84)
Знак минус указывает на то, что тепло от первого тела отводится, т.е. энтропия убывает.
Тогда, энтропия второго тела возрастает:
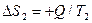 . (85)
. (85)
Суммарное изменение энтропии системы из двух тел:
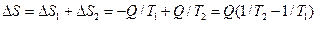 . (86)
. (86)
Из выражения (86) следует, что энтропия данной системы увеличивается.
Максимальное количество работы за счет тепла Q может быть получено при осуществлении в заданном интервале температур цикла Карно. При этом термический КПД в интервале от 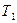 до
до 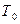 составит:
составит:
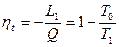 . (87)
. (87)
Следовательно, максимальное количество работы будет равно:
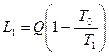 . (88)
. (88)
Максимальное количество работы, которое можно получить от тепла Q после необратимого перехода его второму телу, составит:
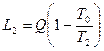 . (89)
. (89)
В результате получается, что рассматриваемый необратимый процесс сопровождается уменьшением работоспособности системы на величину:
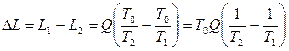 . (90)
. (90)
Сравнивая полученное выражение (90) с уравнением (86) получаем выражение:
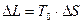 . (91)
. (91)
Формула (91) – это уравнение французского физика Гюи-Стодола. Оно вскрывает физический смысл энтропии и показывает, что необратимые процессы перехода тепла с более высокого на более низкий температурный уровень сопровождаются потерей работоспособности, т.е. деградацией энергии той системы, в которой они происходят, а соответствующее возрастание энтропии пропорционально этой потере работоспособности.
Таким образом, энтропию можно рассматривать как параметр замкнутой системы, увеличение которого является количественной мерой потери работоспособности системы, при протекании в ней необратимых процессов.
Понятие об эксэргии тепла позволяет не только осуществить анализ совершенства тепловых устройств, с позиций первого закона термодинамики, но и оценить потерю работоспособности, обусловленную необратимостью происходящих в них процессов, т.е. оценить работу этих устройств и с позиций второго закона термодинамики.
 2020-01-15
2020-01-15 177
177








