При получении черных металлов с шихтовыми материалами вносится значительное количество серы, ухудшающей качество сплавов. Сера в металле – вредная примесь.
Сера неограниченно растворима в жидком железе.
Растворимость серы в твердом железе очень мала.
Поэтому при затвердевании стали и сплавов происходит выделение избыточной серы в виде сульфидов железа и других элементов по границам зерен поликристаллического металла. При этом могут образовываться и легкоплавкие эвтектики. Сплошность металла нарушается. Этими причинами обусловлены требования на ограничение содержания серы в расплавах менее 0,03…0,001%(мас.).
Формально процесс растворения серы из газовой фазы в разбавленных растворах металлов представляют в виде:
½ S2(газ) = [S]  Дж/моль
Дж/моль
Сера имеет большое химическое сродство к железу. Раствор Fe –S не является идеальным, коэффициент активности f S <1. Поэтому взаимодействие железа с серой нередко представляют реакцией [Fe] + [S] = [FeS]
Растворенные в железе элементы взаимодействуют с серой и изменяют коэффициент активности f S и растворимость серы в железе.
О влиянии каждого из элементов на коэффициент активности серы можно судить по данным о массовых параметрах взаимодействия с серой этих элементов в жидком железе при 16000С, приведенным в таблице.
| Элемент J | Al | P | C | Si | Cr | Cu | Mn | Mo | Ce | S |

| 0,035 | 0,29 | 0,11 | 0,063 | –0,011 | –0,0084 | –0,026 | 0,0027 | –9,1 | –0,028 |
Из таблицы видно, что лишь некоторые элементы (C, Mo, N, Si, P) повышают величину коэффициента активности серы. Другие – Cu, Mn, Cr снижают величину коэффициента активности серы, что должно было бы приводить к повышению растворимости серы в железе из-за усиления связей серы с железом.
Однако для окончательного заключения необходимо иметь в виду, что ряд элементов (Al, Mn, Ce, Zr, Ca, Mg и др.) обладают более высоким сродством к сере, чем железо.
Взаимодействие их с серой при определенных условиях должно приводить к образованию сульфидов, нерастворимых в металле и нередко переходящих в шлак. Это лежит в основе десульфурации железоуглеродистых сплавов.
Пример 4. В расплавленной малоуглеродистой стали, содержащей 0,1%C и 0,5%Mn, и расплавленном чугуне, содержащем 4,0% C, 1,0% Si и 0,6% Mn при 16000С концентрации [S] = 0,04%. Рассчитать активности серы в расплавах.
Решение.
Записываем выражения для расчета коэффициента активности серы по методу Вагнера. Растворы Fe – Mn близки к идеальным, поэтому принимаем 
Тогда расчет активностей серы в сплавах сводится к выражениям:
Для стали: 
Для чугуна:
 Активность серы в чугуне ~ в 3 раза больше, чем в малоуглеродистой стали (при одной и той же концентрации [S].
Активность серы в чугуне ~ в 3 раза больше, чем в малоуглеродистой стали (при одной и той же концентрации [S].
Это значит, что при прочих равных условиях десульфурация чугуна будет идти более успешно, чем стали.
Пример 5. Для расплавленного чугуна, содержащего 4,0% C, 1,0% Si, 0,6% Mn и 0,04% S, рассчитать температуру, при которой термодинамически возможно образование сульфида. Как изменится температура, если содержание марганца в чугуне увеличить вдвое?
Решение.
Уравнение реакции образования сульфида: [Mn] + [S] = MnS(ТВ)
Константа равновесия реакции

Запишем уравнение изотермы реакции и определим, при какой температуре изменение энергии Гиббса реакции становится равным нулю. Это будет температура, ниже которой сера не может находиться в растворе и должна переходить в сульфидную фазу.
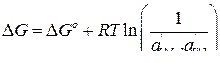
Здесь  и
и  – активности, соответствующие исходным концентрациям Mn и S.
– активности, соответствующие исходным концентрациям Mn и S.
 рассматриваемой реакции выражаем через константу равновесия, температурная зависимость которой по табличным данным имеет вид: lg К = 8470/ Т –5,095.
рассматриваемой реакции выражаем через константу равновесия, температурная зависимость которой по табличным данным имеет вид: lg К = 8470/ Т –5,095.
Тогда уравнение изотермы реакции:

Учитывая условие равновесия  , получим выражение для расчета температуры равновесия сульфида с серой в сплаве
, получим выражение для расчета температуры равновесия сульфида с серой в сплаве

Растворы Fe – Mn близки к идеальным, поэтому принимаем 
Обратим внимание, что состав чугуна соответствует составу сплава примера 4 с вычисленной активностью серы 
Тогда 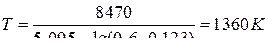
В чугуне с вдвое большим содержанием Mn


С увеличением содержания Mn в чугуне образование сульфидов начинается при охлаждении сплавов при более высоких температурах.
 2020-01-14
2020-01-14 503
503








