Первые попытки создать теорию шлаковых расплавов основывались на результатах исследований минералогического состава затвердевших шлаков и опытных данных о поведении различных элементов в металлургических системах. Так появились различные модификации молекулярных теорий шлаков. Это, по-существу, теории качественные.
Научно обоснованные методы описания термодинамических свойств шлаковых расплавов стали возможны после экспериментального обнаружения и теоретической проработки ионного строения шлаков. Разработано несколько теорий:
– теория совершенных ионных растворов,
– теория регулярных ионных растворов,
– полимеризационная теория,
– теория растворов как фаз с коллективной электронной системой.
Молекулярная теория
Молекулярная модель шлаковых расплавов основывается на предположении, что раствор состоит из “свободных” (FeO, CaO, MnO,...) и “связанных” оксидов (сложных оксидов: CaO×SiO2; 2CaO×SiO2; 2FeO×SiO2;...).
Тогда суммарная концентрация, например, оксида кальция, å(CaO), в основном шлаке складывается из концентраций свободного оксида (CaO)своб. и связанного в сложные оксиды: силикаты –  , фосфаты –
, фосфаты –  , ферриты –
, ферриты –  и др.
и др.
 (3)
(3)
Аналогичные балансовые уравнения можно записать и для других оксидов в шлаке.
Принимается, что
– активность оксида металла определяется концентрацией только “свободного” оксида.
– “свободные” и сложные оксиды находятся в состоянии химического равновесия, описываемого идеальным законом действующих масс.
Трудности:
– в застывших шлаках присутствует достаточно большое число минералов (сложных оксидов), содержащих одни и те же оксиды,
– невозможно объективно оценить “константы” диссоциации сложных оксидов на более простые.
Поэтомув разных вариантах теории ограничивались учетом только “важнейших” и наиболее прочных соединений. Такой выбор был достаточно произвольным.
Так в теории 30-х гг Шенка структурными единицами шлака выбраны молекулы свободных оксидов металлов (CaO, FeO,...) и “важнейшие” соединения: CaO×SiO2, 2FeO×SiO2, 2MnO×SiO2, 3CaO×Fe2O3, 4CaO×P2O5. Используя опытные данные по распределению элементов между металлом и шлаком, Шенк нашел, что предлагаемая молекулярная модель лучше описывает свойства шлака, если предположить, что первые три соединения частично диссоциируют на свободные оксиды:
CaO×SiO2= CaO+SiO2, (4)
2FeO×SiO2= 2FeO+SiO2, (5)
2MnO×SiO2= 2MnO+SiO2, (6)
трехкальциевый феррит 3CaO×Fe2O3 находится в равновесии с металлической фазой
3CaO×Fe2O3 + Fe = 3 CaO + 3FeO, (7)
а соединение 4CaO×P2O5 совсем не диссоциирует. Из опытных данных были получены значения “констант” равновесия реакций (4) – (7), с использованием идеального закона действующих масс. Например, для реакции (4)
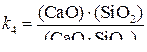 , (8)
, (8)
где  и
и  – концентрации свободных оксидов;
– концентрации свободных оксидов; 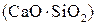 – концентрация соединения в шлаке, или концентрации связанных оксидов.
– концентрация соединения в шлаке, или концентрации связанных оксидов.
Таким образом, задавшись структурными единицами шлакового расплава, используя выражения “констант” равновесия реакций (4) – (7) и балансовые уравнения типа (3), можно определить концентрации структурных составляющих в шлаковых расплавах, а значит и активности компонентов.
Следует отметить, что выбор Г. Шенком сложных оксидов нельзя признать строго обоснованным. Так соединения CaO×SiO2 менее прочно, чем 2CaO×SiO2 , а последнее вообще не входит в перечень принятых Шенком соединений.
При разработке других вариантов молекулярной теории шлаков допускали возможность существования ассоциированных сложных оксидов: 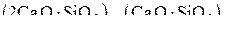 и др. Отсутствие научно обоснованных методов выбора молекулярного состава шлака не позволяет предпочесть какой-либо из вариантов теории.
и др. Отсутствие научно обоснованных методов выбора молекулярного состава шлака не позволяет предпочесть какой-либо из вариантов теории.
Таким образом, основная особенность и недостаток молекулярной теории шлаковых расплавов заключается в отсутствии учета реального строения шлаковых расплавов, что приводит к достаточно произвольному подбору структурных составляющих шлака при расчете распределения элементов между металлургическими фазами.
Однако простота и наглядность исходных положений теории позволяет использовать ее для качественных объяснений процессов и в настоящее время.
 2020-01-14
2020-01-14 284
284








