Основные положения теории состоят в следующем.
1. Раствор состоит только из одноатомных заряженных частиц (катионов – ионов металла Na+, Ca2+, Fe2+, Al3+, Si4+,... и анионов – ионов металлоидов O2-, S2-, F-,...).
2. Ближайшими соседями у каждого иона является только ионы противоположного знака.
3. Энергетическое состояние ионов изменяется при переходе компонента в раствор, поэтому раствор образуется с выделением или поглощением тепла – теплотой смешения  .
.
4. Энергетическая равноценность ионов не приводит к дополнительной упорядоченности в расположении ионов. Катионы, например, распределены по катионным местам структурной матрицы раствора статистически (случайно). Анионы – аналогично. Поэтому энтропия смешения рассчитывается как в теории совершенных растворов.
Наиболее простые соотношения, определяющие энергию и другие термодинамические функции раствора, получаются для ионных растворов с одним общим ионом. Это – оксидные расплавы (шлаки), в которых единственным анионом является ион кислорода.
Для простоты выводов рассмотрим раствор, образованный двумя соединениями CaO и SiO2. Значит, раствор состоит из простейших катионов Ca2+ и Si4+. Анион О2– – общий анион. Тогда состав раствора может быть выражен через ионные доли только катионов Ca2+ и Si4+ Ионная доля кислорода 
Ионные доли катионов совпадают в этом случае с мольными долями компонентов и равны:  (1)
(1)
где n 1 и n 2 – числа молей компонентов CaO и SiO2
Введем модельные схемы размещения частиц в растворе (здесь ионы упрощено даны без знаков зарядов):
Ca—O—Ca Si—O—Si Si—O—Si Ca—O—Ca
| | | | | | | | | | | |
O—Ca— O O—Si—O O—Ca—O O— Si— O
| | | | | | | | | | | |
Ca—O—Ca Si—O—Si Si—O—Si Ca—O—Ca

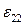

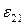
Каждому из возможных размещений частиц в I координационной сфере соответствует определенная энергия связи центрального иона с соседями.
 – энергия связей катиона Ca2+ с окружающими его анионами О2–, когда следующий катионный слой состоит только из катионов Ca2+. По-существу, это энергия связей катиона Ca2+ с анионами О2– в чистом оксиде CaO.
– энергия связей катиона Ca2+ с окружающими его анионами О2–, когда следующий катионный слой состоит только из катионов Ca2+. По-существу, это энергия связей катиона Ca2+ с анионами О2– в чистом оксиде CaO.
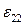 – аналогично, но для Si4+.
– аналогично, но для Si4+.
 – энергия связей катиона Ca2+ с окружающими его анионами О2–, когда следующий катионный слой состоит только из катионов Si4+.
– энергия связей катиона Ca2+ с окружающими его анионами О2–, когда следующий катионный слой состоит только из катионов Si4+.
 – аналогично, но для Si4+.
– аналогично, но для Si4+.
Средняя энергия связей катиона Ca2+с анионами в растворе e1
 (2)
(2)
Здесь z – координационное катионное число – число катионов в ближайшем к данному катиону слою катионов. Из них в растворе  окажутся катионами Ca2+, а
окажутся катионами Ca2+, а  – катионами Si4+.
– катионами Si4+.
Аналогичное выражение для средней энергии связей катиона Si4+ с анионами в растворе e2
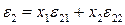 (3)
(3)
Энергия раствора, содержащего 1 моль катионов
 (4)
(4)
где N0 – число Авогадро.
При записи конечного выражения было учтено, что для бинарного раствора

Обозначим
 (5)
(5)
 (6)
(6)
Величины  и
и 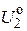 представляют собой энергии чистых соединений CaO и SiO2 , содержащих 1 моль катионов, а величина Q12 – энергия смешения (энергия взаимообмена) компонентов CaO и SiO2 .
представляют собой энергии чистых соединений CaO и SiO2 , содержащих 1 моль катионов, а величина Q12 – энергия смешения (энергия взаимообмена) компонентов CaO и SiO2 .
Поэтому мольная энергия
 (7)
(7)
Энтропия раствора, содержащего 1 моль катионов,
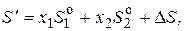 (8)
(8)
где  и
и  – мольные энтропии чистых компонентов CaO и SiO2 .
– мольные энтропии чистых компонентов CaO и SiO2 .
Энтропия смешения
 (9)
(9)
где k – постоянная Больцмана, W – термодинамическая вероятность.
W может быть подсчитана как число всех возможных (различимых) перестановок частиц в системе, приводящих к новым конфигурациям в расположении частиц.
 (10)
(10)
Здесь 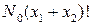 – общее число всех перестановок катионов,
– общее число всех перестановок катионов,  и
и 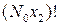 – число перестановок катионов Ca2+и катионов Si4+.
– число перестановок катионов Ca2+и катионов Si4+.
Применяя формулу Стирлинга для 
 (11)
(11)
получим: 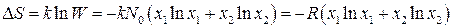
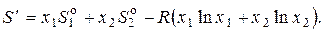 (12)
(12)
Свободная энергия раствора  ,
,
поэтому
 (13)
(13)
Свободная энергия произвольного количества раствора, содержащего  и
и  моль
моль
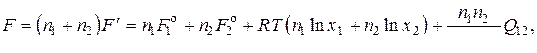 (14)
(14)
а химические потенциалы компонентов
 (15)
(15)
 (16)
(16)
Сравним (15) с уравнением  (17)
(17)
и учтем, что  , получим:
, получим:
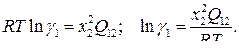 (18)
(18)
Активности компонентов CaO и SiO2 будут равны
 (19)
(19)
Если система содержит k компонентов, то уравнение (13) принимает вид:
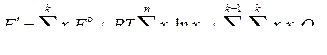 (20)
(20)
Энергия произвольного количества раствора, содержащего  ,
,  …
…  моль
моль
 (21)
(21)
 (22)
(22)
После дифференцирования
 (23)
(23)
Окончательно для коэффициента активности компонента l:
 (24)
(24)
Энергия смешения компонентов Qij находится на основании результатов экспериментальных исследований бинарных растворов из соединений, содержащих катионы i и j. Чаще всего используются диаграммы состояния (диаграммы плавкости) бинарных систем.
Рассмотренное нулевое приближение теории регулярных ионных растворов (теория Кожеурова В.А.) основывается на допущении, что энергия смешения компонентов раствора, образованных с участием катионов сортов i и j,
 (25)
(25)
не зависит от состава раствора и температуры.
В квазирегулярном приближении теории принимается, что энергия смешения зависит от температуры,
 (26)
(26)
а в субрегулярном приближении – зависит от состава
 (27)
(27)
где  и
и  – относительные доли катионов i и j в растворе.
– относительные доли катионов i и j в растворе.
В более сложных вариантах теории принимается, что энергия катионов сорта i, e i, определяется не только ближайшими соседними анионами и катионами, но и более далекими. Учитывается также возможная упорядоченность в расположении частиц, которая обусловлена зависимостью энергии связи катиона i от состава раствора.
 2020-01-14
2020-01-14 700
700








