| HNO3 – одноосновная, кислородсодержащая кислота
|
Получение:
В промышленности
1) Поэтапно аммиачным способом:
1 этап: окисление NH3: 4NH3 + 5О2  4NO↑ + 6 Н2О
2 этап: окисление NO в NO2: 2NO + О2 → 2NO2↑
3 этап: абсорбция бурого газа: 3NO2 + Н2О → 2HNO3 + NO↑
4NO2 + 2H2O + O2 → 4HNO3(конц.)
В лаборатории
2) Из нитратов: NaNO3 + H2SO4(конц.) 4NO↑ + 6 Н2О
2 этап: окисление NO в NO2: 2NO + О2 → 2NO2↑
3 этап: абсорбция бурого газа: 3NO2 + Н2О → 2HNO3 + NO↑
4NO2 + 2H2O + O2 → 4HNO3(конц.)
В лаборатории
2) Из нитратов: NaNO3 + H2SO4(конц.) 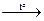 NaHSO4 + HNO3 NaHSO4 + HNO3
|
Физические свойства:
В чистом виде бесцветная маслянистая жидкость c резким запахом, кислая на вкус, отлично растворимая в воде, ядовита.
При длительном хранении или на свету желтеет, вследствие разложения с выделением бурого газа: 4HNO3 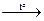 4NO2↑ + 2H2O + O2↑.
Концентрированная азотная кислота обугливает бумагу, мех, кожу, вызывая сильные ожоги. При попадании на кожу образуются жёлтые пятна, вследствие ксантопротеиновой реакции. 4NO2↑ + 2H2O + O2↑.
Концентрированная азотная кислота обугливает бумагу, мех, кожу, вызывая сильные ожоги. При попадании на кожу образуются жёлтые пятна, вследствие ксантопротеиновой реакции.
|
| Химические свойства:
1) Сильный электролит: HNO3⇄ H+ + NO3–.. Изменяет окраску индикаторов: лакмус в красный, а метилоранж в розовый.
2) С металлами: *10HNO3 (8%) + 4Zn → 4Zn (NO3)2 + 3H2O + NН4NO3
*12HNO3 (18%) + 5Zn → 5Zn (NO3)2 + 6H2O + N2↑
8HNO3 (30%) + 3Zn → 3Zn (NO3)2 + 4H2O + 2NO↑
4HNO3 (80%) + Zn → Zn (NO3)2 + 2H2O + 2NO2↑
*3) С неметаллами: 5HNO3 (63%)+ Р → Н3РО4 + H2O + 5NO2↑
5HNO3 (30%)+ 3Р + 2H2O → 3Н3РО4 + 5NO↑
4) С оксидами металлов: 2HNO3 + ZnO→ Zn (NO3)2 + H2O
5) С основаниями: 2HNO3 + Zn(OH)2 → Zn (NO3)2 + 2H2O
6) С солями: 2HNO3 + Na2CO3 → 2NaNO3 + H2O + CO2↑
|
| Применение:
Азотная кислота занимает второе место по применению после H2SO4. Она применяется для получения нитратов, минеральных удобрений, взрывчатых веществ (тол, динамит), нитрокрасок и эмалей, полимеров, лекарственных препаратов, а также как окислитель ракетного топлива.
|
 4NO↑ + 6 Н2О
2 этап: окисление NO в NO2: 2NO + О2 → 2NO2↑
3 этап: абсорбция бурого газа: 3NO2 + Н2О → 2HNO3 + NO↑
4NO2 + 2H2O + O2 → 4HNO3(конц.)
В лаборатории
2) Из нитратов: NaNO3 + H2SO4(конц.)
4NO↑ + 6 Н2О
2 этап: окисление NO в NO2: 2NO + О2 → 2NO2↑
3 этап: абсорбция бурого газа: 3NO2 + Н2О → 2HNO3 + NO↑
4NO2 + 2H2O + O2 → 4HNO3(конц.)
В лаборатории
2) Из нитратов: NaNO3 + H2SO4(конц.) 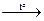 NaHSO4 + HNO3
NaHSO4 + HNO3
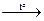 4NO2↑ + 2H2O + O2↑.
Концентрированная азотная кислота обугливает бумагу, мех, кожу, вызывая сильные ожоги. При попадании на кожу образуются жёлтые пятна, вследствие ксантопротеиновой реакции.
4NO2↑ + 2H2O + O2↑.
Концентрированная азотная кислота обугливает бумагу, мех, кожу, вызывая сильные ожоги. При попадании на кожу образуются жёлтые пятна, вследствие ксантопротеиновой реакции.
 2020-05-13
2020-05-13 109
109








