Кровообращение выполняет одну из важнейших функций переноса кислорода от легких к тканям, а углекислого газа — от тканей к легким. Потребление кислорода клетками тканей может изменяться в значительных пределах, например при переходе от состояния покоя к физической нагрузке и наоборот. В связи с этим кровь должна обладать большими резервами, необходимыми для увеличения ее способности переносить кислород от легких к тканям, а углекислый газ в обратном направлении.
10.4.1. Транспорт кислорода
При 37 °C растворимость О2 в жидкости составляет 0,225 мл-л"1-кПа"1 (0,03 мл/л/мм рт. ст.). В условиях нормального парциального давления кислорода в альвеолярном воздухе, т. е. 13,3 кПа или 100 мм рт.ст., 1 л плазмы крови может переносить только 3 мл О2, что недостаточно для жизнедеятельности организма в целом. В покое в организме человека за минуту потребляется примерно 250 мл кислорода. Чтобы тканям получить такое количество кислорода в физически растворенном состоянии, сердце должно перекачивать за минуту огромное количество крови. В эволюции живых существ проблема транспорта кислорода была более эффективно решена за счет обратимой химической реакции с гемоглобином эритроцитов. Кислород переносится кровью от легких к тканям организма молекулами гемоглобина, которые содержатся в эритроцитах. Гемоглобин способен захватывать кислород из альвеолярного воздуха (соединение называется оксигемоглобином) и освобождать необходимое количество кислорода в тканях. Особенностью химической реакции кислорода с гемоглобином является то, что количество связанного кислорода ограничено количеством молекул гемоглобина в эритроцитах крови. Молекула гемоглобина имеет 4 места связывания с кислородом, которые взаимодействуют таким образом, что зависимость между парциальным давлением кислорода и количеством переносимого кислорода с кровью имеет S-образную форму, которая носит название кривой насыщения или диссоциации оксигемоглобина (рис. 10.18). При парциальном давлении кислорода 10 мм рт. ст. насыщение гемоглобина кислородом составляет примерно 10 %, а при РО2 30 мм рт. ст. — 50—60 %. При дальнейшем увеличении парциального давления кислорода от 40 мм рт. ст. до 60 мм рт. ст. происходит уменьшение крутизны кривой диссоциации оксигемоглобина и процент его насыщения ки-
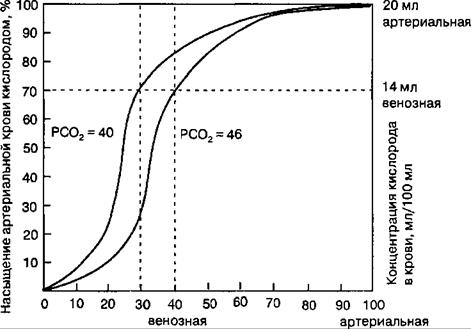
Парциальное давление кислорода, мм рт. ст.
Рис. 10.18. Кривая диссоциации оксигемоглобина. Пределы колебания кривой при РСО2 = 40 мм рт. ст. (артериальная кровь) и РСО2 = 46 мм рт. ст. (венозная кровь) показывают изменение сродства гемоглобина к кислороду (эффект Ходена).
слородом возрастает в диапазоне от 70—75 до 90 % соответственно. Затем кривая диссоциации оксигемоглобина начинает занимать практически горизонтальное положение, поскольку увеличение парциального давления кислорода с 60 до 80 мм рт. ст. вызывает прирост насыщения гемоглобина кислородом на 6 %. В диапазоне от 80 до 100 мм рт. ст. процент образования оксигемоглобина составляет порядка 2. В результате кривая диссоциации оксигемоглобина переходит в горизонтальную линию и процент насыщения гемоглобина кислородом достигает предела, т. е. 100. Насыщение гемоглобина кислородом под влиянием РО2 характеризует своеобразный молекулярный «аппетит» этого соединения к кислороду.
Значительная крутизна кривой насыщения гемоглобина кислородом в диапазоне парциального давления от 20 до 40 мм рт. ст. способствует тому, что в ткани организма значительное количество кислорода может диффундировать из крови в условиях градиента его парциального давления между кровью и клетками тканей (не менее 20 мм рт. ст.). Незначительный процент насыщения гемоглобина кислородом в диапазоне его парциального давления от 80 до 100 мм рт. ст. способствует тому, что человек без риска снижения насыщения артериальной крови кислородом может перемещаться в диапазоне высот над уровнем моря до 2000 м.
Общие запасы кислорода в организме обусловлены его количеством, находящимся в связанном состоянии с ионами Fe2+ в составе органических молекул гемоглобина эритроцитов и миоглобина мышечных клеток.
Один грамм гемоглобина связывает 1,34 мл О2. Поэтому в норме при концентрации гемоглобина 150 г/л каждые 100 мл крови могут переносить 20,0 мл О2.
Количество О2, которое может связаться с гемоглобином эритроцитов крови при насыщении 100 % его количества, называется кислородной емкостью гемоглобина. Другим показателем дыхательной функции крови является содержание О2 в крови (кислородная емкость крови), которое отражает его истинное количество, как связанного с гемоглобином, так и физически растворенного в плазме. Поскольку в норме артериальная кровь насыщена кислородом на 97 %, то в 100 мл артериальной крови содержится примерно 19,4 мл О2.
10.4.1.1. Изменение сродства гемоглобина к кислороду
Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой группой молекулы гемоглобина. При этом чем больше геминовых групп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком РО2, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком РО2 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц.
Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким РО2 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию РО2 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах РО2 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и pH.
Эффект pH и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое pH понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и СО2. Если pH плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном pH 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда pH снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 73 больше, чем при постоянном pH.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани.
Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении РО2 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-
ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей.
10.4.2. Транспорт углекислого газа
СО2 является продуктом метаболизма клеток тканей и поэтому переносится кровью от тканей к легким. Углекислый газ выполняет жизненно важную роль в поддержании во внутренних средах организма уровня pH механизмами кислотно-основного равновесия. Поэтому транспорт углекислого газа кровью тесно взаимосвязан с этими механизмами (см. глава 15).
В плазме крови небольшое количество СО2 находится в растворенном состоянии; при РСО2= 40 мм рт. ст. переносится 2,5 мл/100 мл крови СО2, или 5 %. Количество растворенного в плазме углекислого газа в линейной зависимости возрастает от уровня РСО2.
В плазме крови СО2 реагирует с водой с образованием Н+ и НСО^. Увеличение напряжения углекислого газа в плазме крови вызывает уменьшение величины ее pH. Напряжение СО2 в плазме крови может быть изменено функцией внешнего дыхания, а количество ионов водорода или pH — буферными системами крови и НСО7, например путем их выведения через почки с мочой. Величина pH плазмы крови зависит от соотношения концентрации растворенного в ней СО2 и ионов бикарбоната. В виде бикарбоната плазмой крови, т. е. в химически связанном состоянии, переносится основное количество углекислого газа —порядка 45 мл/100 мл крови, или до 90 %. Эритроцитами в виде карбаминового соединения с белками гемоглобина транспортируется примерно 2,5 мл/100 мл крови СО2, или 5 %. Транспорт углекислого газа кровью от тканей к легким в указанных формах не связан с явлением насыщения, как при транспорте кислорода, т. е. чем больше образуется углекислого газа, тем большее его количество транспортируется от тканей к легким. Однако между парциальным давлением СО2 в крови и количеством переносимого кровью углекислого газа имеется криволинейная зависимость: кривая диссоциации углекислого газа.
10.4.2.1. Роль эритроцитов в транспорте СО2
В крови капилляров тканей организма напряжение СО2 составляет 5,3 кПа (40 мм рт. ст.), а в самих тканях — 8,0—10,7 кПа (60—80 мм рт. ст.). В результате СО2 диффундирует из тканей в плазму крови, а из нее — в эритроциты по градиенту парциального давления СО2. В эритроцитах СО2 образует с водой угольную кислоту, которая диссоциирует на Н+ и НСО^. (СО2 + Н2О = Н2СО3 = Н+ + НСОр. Эта реакция протекает быстро, поскольку СО2 + Н2О = Н2СО3 катализируется ферментом карбоангидразой мембраны эритроцитов, которая содержится в них в высокой концентрации (рис. 10.19). Эта реакция протекает по закону действия масс и в норме выражается в логарифмической форме, известной как уравнение Гендерсо- на—Гассельбаха (см. главу 15).
В эритроцитах диссоциация СО2 продолжается постоянно по мере образования продуктов этой реакции, поскольку молекулы гемоглобина действуют как буферное соединение, связывая положительно заряженные ионы водорода. В эритроцитах по мере освобождения кислорода из гемоглобина его молекулы будут связываться с ионами водорода (СО2 + Н2О = Н2СО3 = = Н+ + НСО7), образуя соединение (НЬ-Н+). В целом это называется эф-
 |
|

|
|
|
► СО2
А. Процессы газообмена СО2 между клетками тканей и плазмой крови. СО2 поступает путем диффузии в плазму крови из тканей и дифференцирует внутрь эритроцитов. В эритроцитах СО2 превращается при участии фермента карбоангидразы мембраны эритроцитов в НСО3 и в виде этого иона вновь активно транспортируется в плазму крови, в которой в составе бикарбонатов (NaHCO3) переносится к капиллярам легких. Водородные ионы, образующиеся при реакции дегидратации Н2СО3, захватываются молекулами гемоглобина и также транспортируются кровью от тканей к легким. При транспорте из эритроцитов НСО3-ионное постоянство внутри эритроцитов поддерживается хлорным сдвигом. Кроме того, СО2 в эритроцитах непосредственно соединяется с Nh2 группами белков гемоглобина.
Б. Процессы газообмена СО2 между плазмой крови и альвеолами легких. В капиллярах легких в эритроцитах под влиянием эффекта Бора происходит диссоциация карбаминовых соединений и СО2 диффундирует через мембрану эритроцитов и альвеолярную мембрану в просвет альвеол легких.
фектом Холдена, который приводит к сдвигу кривой диссоциации оксигемоглобина вправо по оси х, что снижает сродство гемоглобина к кислороду и способствует более интенсивному освобождению его из эритроцитов в ткани. При этом в составе соединения НЬ-Н+ транспортируется примерно 200 мл СО2 в одном литре крови от тканей к легким.
Диссоциация СО2 в эритроцитах может быть лимитирована только буферной емкостью молекул гемоглобина. Образующиеся внутри эритроцитов в результате диссоциации СО2 ионы НСО^ с помощью специального белка-переносчика мембраны эритроцитов выводятся из эритроцитов в плазму, а на их место из плазмы крови закачиваются ионы СГ (феномен «хлорного» сдвига) (рис. 10.19). Основная роль реакции СО2 внутри эритроцитов заключается в обмене ионами СГ и НСО7 между плазмой и внутренней средой эритроцитов. В результате этого обмена продукты диссоциации углекислого газа Н+ и НСО^ будут транспортироваться внутри эритроцитов в виде соединения (НЬ-Н+), а плазмой крови — в виде бикарбонатов.
Эритроциты участвуют в транспорте углекислого газа от тканей к легким, поскольку СО2 образует прямую комбинацию с — НН2-группами белковых субъединиц гемоглобина: СО2 + НЬ НЬСО2 или карбаминовое соединение. Транспорт кровью СО2 в виде карбаминового соединения и ионов водорода гемоглобином зависит от свойств молекул последнего; обе реакции обусловлены величиной парциального давления кислорода в плазме крови на основе эффекта Холдена.
В количественном отношении транспорт СО2 в растворенной форме и в форме карбаминового соединения является незначительным, по сравне
нию с его переносом СО2 кровью в виде бикарбонатов. Однако при газообмене СО2 в легких между кровью и альвеолярным воздухом эти две формы приобретают основное значение.
Когда венозная кровь возвращается от тканей к легким, СО2 диффундирует из крови в альвеолы и РСО2 в крови снижается с 46 мм рт. ст. (венозная кровь) до 40 мм рт.ст. (артериальная кровь). При этом в величине общего количества СО2 (6 мл/100 мл крови), диффундирующего из крови в альвеолы, доля растворенной формы СО2 и карбаминовых соединений становится более значительной относительно бикарбонатной. Так, доля растворенной формы составляет 0,6 мл/100 мл крови, или 10 %, карбаминовых соединений — 1,8 мл/100 мл крови, или 30%, а бикарбонатов — 3,6 мл/100 мл крови, или 60 %.
В эритроцитах капилляров легких по мере насыщения молекул гемоглобина кислородом начинают освобождаться ионы водорода, диссоциировать карбаминовые соединения и НСО^ вновь превращается в СО2 (Н+ + HCOj = = Н2СО3 = СО2 +Н2О), который путем диффузии выводится через легкие по градиенту его парциальных давлений между венозной кровью и альвеолярным пространством. Таким образом, гемоглобин эритроцитов играет основную роль в транспорте кислорода от легких к тканям, и углекислого газа в обратном направлении, поскольку способен связываться с О2 и Н+. В состоянии покоя через легкие из организма человека за минуту удаляется примерно 300 мл СО2: 6 мл/100 мл крови х 5000 мл/мин минутного объема кровообращения.
Регуляция дыхания
Дыхательная система должна обеспечивать полное соответствие между количеством кислорода, поступающего в кровь через легкие, и скоростью его потребления в тканях, а так же соответствие между продукцией в тканях СО2 и количеством удаляемого из организма через легкие СО2. Эта функция дыхательной системы достигается за счет приспособления (регуляции) объема легочной вентиляции к уровню метаболизма в организме. Приспособление легочной вентиляции к процессам метаболически обусловленного газообмена в организме человека осуществляется сложной иерархической системой регуляции дыхания, состоящей из центральных и периферических хеморецепторных рефлексов (общий контроль), а также механо- рецепторных рефлексов (локальный контроль) (рис. 10.20). В этой системе дыхательный центр генерирует дыхательный ритм, интегрирует афферентные сигналы, посылает импульсы к дыхательным мышцам грудной клетки и к гладким мышцам дыхательных путей, обеспечивая приспособление легочной вентиляции к условиям жизнедеятельности организма.
 |

 |
|
10.5.1, Дыхательный центр
Величина легочной вентиляции обусловлена частотой и глубиной дыхательных движений (дыхательного ритма), происхождение которых связано с функцией дыхательного центра центральной нервной системой. Под дыхательным центром понимают ограниченный участок ЦНС, где происходит формирование дыхательного импульса, вызывающего координированную деятельность дыхательных мышц, обеспечивающих для организма необходимую величину газообмена в легких. В центральной нервной системе местом генерации дыхательного ритма, вызывающего ритмические сокращения дыхательных мышц при вдохе и выдохе, является продолговатый мозг, в котором расположен дыхательный центр. Дыхательный центр состоит из нервных клеток (дыхательных нейронов), для которых характерна периодическая электрическая активность в одну из фаз дыхания. Нейроны дыхательного центра локализованы двусторонне в продолговатом мозге в виде двух вытянутых столбов вблизи obex — точки, где центральный канал спинного мозга впадает в четвертый желудочек. Эти два образования дыхательных нейронов в соответствии с их положением относительно дорсальной и вентральной поверхности продолговатого мозга обозначают как дорсальная и вентральная дыхательные группы (рис. 10*21).
Дорсальная дыхательная группа нейронов образует вентролатеральную часть ядра одиночного тракта. Дыхательные нейроны вентральной дыхательной группы расположены в области n. ambiguus каудальнее уровня obex, n. retroambigualis непосредственно ростральнее obex и представлены комплексом Бетзингера, который находится непосредственно вблизи n. retrofa- cialis вентролатеральных отделов продолговатого мозга. В состав дыхательного центра входят нейроны двигательных ядер черепно-мозговых нервов (обоюдное ядро, ядро подъязычного нерва), которые иннервируют мышцы гортани и глотки.
Основным критерием классификации нейронов дыхательного центра является фаза дыхательного цикла, в которую они активны, т. е. инспирация или экспирация. По этому критерию дыхательные нейроны подразделяют на инспираторные и экспираторные. Дорсальная дыхательная группа состоит полностью из инспираторных нейронов. Вентральная дыхательная группа образована инспираторными и экспираторными нейронами, а комплекс Бетзингера образуют только экспираторные нейроны. По паттерну электрической активности нейронов в пределах фаз дыхательного цикла инспираторные и экспираторные нейроны подразделяют на нейроны с нарастающим, постоянным или декрементным типом активности (рис. 10.22).
По проекции аксонов дыхательные нейроны разделяют на премоторные или бульбоспинальные нейроны и проприобульбарные. Аксоны премоторных дыхательных нейронов переходят на противоположную сторону продолговатого мозга, а затем направляются к мотонейронам спинного мозга. Функция инспираторных премоторных дыхательных нейронов заключается
 |
|
|
 LJ.JJJJAB
LJ.JJJJAB
I I
jlliliMl 1 1
: I I HIM

|
 |
|
|
в управлении электрической активностью инспираторных мотонейронов диафрагмы и наружных межреберных мышц во время их сокращения при вдохе. В обычных условиях экспирация осуществляется пассивно, поэтому функция экспираторных премоторных дыхательных нейронов реализуется только при увеличении глубины дыхательных движений. Премоторные нейроны комплекса Бетзингера выполняют уникальную функцию — они тормозят все типы инспираторных нейронов дыхательного центра и диафрагмальные мотонейроны. Поэтому их аксоны распределяются билатерально, т. е. направляются к соответствующим нейронам, расположенным как ипсилатерально, так и контралатерально.
Аксоны проприобульбарных дыхательных нейронов (ранние инспираторные, постинспираторные, поздние инспираторные, экспираторные нейроны комплекса Бетзингера) оканчиваются на мембране нейронов самого дыхательного центра, расположенных в вентральной дыхательной группе. Функция большинства проприробульбарных нейронов заключается в генерации дыхательного ритма.
10.5.1.1. Происхождение дыхательного ритма
У человека дыхательные движения впервые начинаются у плода (в начале III триместра беременности). Эти дыхательные движения носят периодический и нерегулярный характер. Современные исследования свидетельствуют о том, что дыхательные движения плода инициируются проприобуль- барными инспираторными пейсмекерными клетками вентральной дыхательной группы, расположенными вблизи нейронов комплекса Бетзингера (пребетзингерова область). Эти нейроны обладают двумя уникальными свойствами. Мембрана нейронов способна к спонтанной деполяризации и, когда их мембранный потенциал достигает порога возбуждения, нейроны генерируют короткий залп потенциалов действия. Вторым свойством мембраны пейсмекерных нейронов дыхательного центра является механизм аккомодации, т. е. самоограничения электрической активности. Этот механизм представляет собой гиперполяризацию мембранного потенциала нейрона под влиянием нарастающего входящего тока ионов хлора и формирование декрементного паттерна электрической активности. В результате в течение короткого отрезка времени нейроны способны самостоятельно прекращать свою электрическую активность. Разряды электрических импульсов по аксонам дыхательных нейронов распространяется к мотонейронам спинного мозга и вызывают через них сокращение диафрагмы и наружных межреберных мышц у плода. Внутриутробные ритмические сокращения инспираторных мышц у плода способствуют развитию у него аппарата внешнего дыхания к моменту рождения. Первый вдох новорожденного и дыхание в первые сутки после рождения по-прежнему обусловлены спонтанной пейсмекерной активностью проприобульбарных нейронов вентральной дыхательной группы дыхательного центра.
У взрослых млекопитающих животных происхождение дыхательного ритма объясняют двумя теориями, которые основаны на пейсмекерной гипотезе и гипотезе нейронной сети. Согласно первой, дыхательный ритм возникает в пейсмекерных проприобульбарных дыхательных нейронах пребетзингеровой области. Затем залпы нервных импульсов от пейсмекерных нейронов передаются другим типам нейронов дыхательного центра, при участии которых возникает соответствующий ритм дыхательных движений.
Происхождение дыхательного ритма при участии нейронной сети дыхательного центра объясняют функцией синаптических связей между различными типами дыхательных нейронов. Основным проявлением синаптических связей является взаимное торможение между группами нейронов противоположных фаз дыхательного цикла. Вторым свойством ритмгене- рирующей нейронной сети является наличие в ней хотя бы одного типа дыхательных нейронов, возбудимая мембрана которых обладает механизмом аккомодации, т. е. самоограничения электрической активности. В дыхательном центре взрослых животных имеется два типа дыхательных нейронов, обладающих аккомодативным механизмом: ранние инспираторные и постсинспираторные (рис. 10.22). Оба типа нейронов взаимно тормозят друг друга и все другие типы нейронов дыхательного центра в период, когда активны либо ранние инспираторные нейроны, либо постинспираторные нейроны. Ключевая роль в дыхательном ритмогенезе ранних инспираторных нейронов с декрементным типом активности заключается в инициации дыхательного ритма, а именно вдоха. С момента начала разряда этого типа нейронов, благодаря механизму самоограничения активности ранних инспираторных нейронов, прекращается их тормозное действие на другие типы инспираторных нейронов дыхательного центра. В результате происходит активация инспираторных нейронов (полных и поздних) и возникает фаза вдоха. Как только вдох выключается (функция центров моста и ядер блуждающего нерва), активируются постинспираторные нейроны с декрементным типом активности и начинается фаза выдоха. Благодаря механизму самоограничения активности постинспираторные нейроны постепенно прекращают тормозное действие на экспираторные нейроны с нарастающей активностью и на ранние инспираторные нейроны. С момента активации последних прекращается фаза выдоха и начинается очередная фаза вдоха.
10.5.2. Влияние нервных центров варолиева моста на дыхательный ритм
В верхних отделах моста расположены две области — n. parabrachealis medi- alis и n. Kolliker—Fuse, которые влияют на дыхательный центр продолговатого мозга и образуют пневмотаксический центр. Нейроны этого центра ре- ципрокно связаны с инспираторными нейронами дорсальной дыхательной группы. Функцией пневмотаксического центра моста является уменьшение периода активности инспираторных нейронов дыхательного центра путем выключения фазы вдоха и более раннее появление в дыхательном цикле фазы выдоха. В результате пневмотаксический центр вызывает в дыхательном центре генерацию большего числа небольших по длительности инспираций, т. е. увеличивает частоту дыхания.
На уровне нижней трети моста имеется область, определяемая как ап- нейстический центр. В обычных условиях активность этого центра заторможена со стороны пневмотаксического центра. Название центра обусловлено тем, что его отделение от пневмотаксического центра и/или от тормозных афферентных влияний блуждающего нерва (описано ниже), вызывает остановку дыхания на вдохе (апнейзис). Эта область оказывает возбуждающее влияние на нейроны дорсальной дыхательной группы дыхательного центра и ее роль заключается в увеличении времени фазы выдоха, а, следовательно, глубины дыхательных движений.
10.5.3. Функция спинальных дыхательных мотонейронов
При спокойном дыхании в течение фазы вдоха электрические импульсы инспираторных бульбоспинальных нейронов дыхательного центра передаются к мотонейронам сегментов спинного мозга: Сщ—Cv и Тг—ТХ11. Аксоны мотонейронов СП1—■Cv образуют диафрагмальные нервы, a Tj—ТХ11 — межреберные нервы, которые иннервируют соответственно диафрагму и наружные межреберные мышцы. Активация электрической активности этих мотонейронов под влиянием нисходящих команд дыхательного центра вызывает сокращение диафрагмы и наружных межреберных мышц, что определяет уровень вентиляции легких. При глубоком дыхании фаза выдоха также становится активной, и нисходящие команды дыхательного центра начинают включать импульсы к мотонейронам мышц живота и внутренних межреберных мышц (сегменты Т—L). Активация электрической активности мотонейронов, которые иннервируют экспираторные мышцы, обусловливает глубину выдоха.
10.5.4. Рефлекторная регуляция дыхания
10.5.4.1. Хеморецепторный контроль дыхания

|
|
 | |||
 | |||

 |
увеличивает чувствительность пери-
ферических хеморецепторов к [Н+] и СО2. Это состояние называется асфиксией и возникает при прекращении вентиляции легких. Поэтому периферические хеморецепторы называются часто рецепторами асфиксии. Импульсы от периферических хеморецепторов по волокнам синокаротидного нерва (нерв Геринга — часть языкоглоточного нерва) и аортальной ветви блуждающего нерва достигают чувствительных нейронов ядра одиночного тракта продолговатого мозга, а затем переключаются на нейроны дыхательного центра. Возбуждение последнего вызывают прирост вентиляции легких. Вентиляция легких увеличивается линейно в соответствии с величиной [Н+] и РСО2 выше порога (40 мм рт. ст.) в артериальной крови, протекающей через каротидные и аортальные тельца (рис. 10.24). Наклон кривой на рисунке, который отражает чувствительность периферических хеморецепторов к [Н+] и РСО2, варьирует в зависимости от степени гипоксии.
10.5.4.2. Механорецепторный контроль дыхания
Механорецепторный контроль дыхания осуществляется рефлексами, которые возникают при раздражении механорецепторов дыхательных путей легких. В тканях дыхательных путей расположено два основных типа механорецепторов, импульсы от которых поступают к нейронам дыхательного центра: быстро адаптирующиеся, или ирритантные, рецепторы и рецепторы растяжения.
Быстроадаптирующиеся рецепторы расположены в эпителии и субэпителиальном слое, начиная от верхних дыхательных путей вплоть до альвеол. Название рецепторов свидетельствует о том, что они активируются при раздражении не продолжительно и быстро снижают свою активность при сохранении действия стимула. Поэтому быстроадаптирующиеся рецепторы реагируют на изменение силы раздражения. Эти рецепторы инициируют такие сложные рефлексы, как нюхательный или кашлевой. Они возбуждаются при попадании на слизистую оболочку трахеи и бронхов механических или химических раздражителей (пыль, слизь, табачный дым, пары едких веществ — аммиак, эфир). В зависимости от местоположения ирри- тантных рецепторов в дыхательных путях возникают специфические рефлекторные реакции дыхания. Раздражение рецепторов слизистой оболочки носовой полости при участии тройничного нерва вызывает рефлекс чиханья; рецепторов эпифарингеальной области — через волокна языкоглоточного нерва — нюхательный или аспирационный рефлекс; рецепторов слизистой оболочки гортани и трахеи — через волокна блуждающего нерва — рефлекс чиханья; рецепторов слизистой оболочки от уровня трахеи и до бронхиол — при участии блуждающих нервов — парадоксальный рефлекс Геда (при раздувании легких) и рефлекс выдоха и, наконец, рецепторов стенки альвеол в месте их контакта со стенкой легочных капилляров — через волокна блуждающего нерва — вызывает рефлекторную реакцию в виде частого и поверхностного дыхания.
Медленно адаптирующиеся рецепторы растяжения легких локализованы в гладких мышцах главных дыхательных путей бронхиального дерева (бронхи и трахея) и раздражаются в результате увеличения объема легких (раздувание). Рецепторы связаны с нейронами дорсальной дыхательной группы дыхательного центра миелинизированными афферентными волокнами блуждающего нерва. Стимуляция этих рецепторов вызывает рефлекс Геринга—Брейера, который у животных проявляется в том, что раздувание легких вызывает рефлекторное переключение фазы вдоха на фазу выдоха. У человека в состоянии бодрствования этот рефлекторный эффект возникает при величине дыхательного объема, которая превышает примерно в три раза его нормальную величину при спокойном дыхании. Во время сна рефлекторное выключение вдоха с помощью рефлекса Геринга—Брейера обусловливает смену фаз дыхательного цикла.
Легочные J-рецепторы локализованы в пределах стенок альвеол в месте их контакта с капиллярами и способны реагировать на стимулы как со стороны легких, так и со стороны легочного кровообращения. Рецепторы связаны с дыхательным центром немиелинизированными афферентными С-волокнами. Эти рецепторы повышают свою активность при увеличении в плазме крови концентрации ионов водорода, при сдавливании легочной ткани или легочном отеке. Наибольшую активность легочные J-рецепторы имеют во время физической активности большой мощности и при подъеме на большую высоту над уровнем моря. В этих случаях одним из проявлений изменения давления в сосудах малого круга кровообращения может быть отек легких разной выраженности. Возникающее при этом раздражение J-рецепторов вызывает частое, поверхностное дыхание, рефлекторную бронхоконстрикцию и одышку.
Проприорецепторы. Дыхательный центр непрерывно получает афферентные входы от прориорецепторов мышц (мышечные веретена и сухожильные рецепторы Гольджи) по восходящим спинальным трактам. Эти афферентные входы являются как неспецифическими (рецепторы расположены в мышцах и суставах конечностей), так и специфическими (рецепторы расположены в дыхательных мышцах). Импульсация от проприорецепторов распространяется преимущественно к спинальным центрам дыхательных мышц, а также к центрам головного мозга, контролирующим тонус скелетной мускулатуры. Активация проприорецепторов в момент начала физической нагрузки является основной причиной увеличения активности дыхательного центра и повышения вентиляции легких. Проприорецепторы межреберных мышц и диафрагмы рефлекторно регулируют ритмическую активность дыхательного центра продолговатого мозга в зависимости от положения грудной клетки в различные фазы дыхательного цикла, а на сегментарном уровне — тонус и силу сокращения дыхательных мышц.
 2020-05-25
2020-05-25 344
344








