Положительные степени окисления, которые проявляет фосфор в соединении 5, 3, 1.
KH2PO2, P2O3, HPO3
Оксидтетрафосфора, P4O
Диоксидтетрафосфора, P4O2
Оксидфосфора(III), P2O3 (P4O6) кислотаH3PO3
Оксидфосфора(IV), P4O8
Оксидфосфора(V), P2O5 (P4O10) кислотаH3PO4
3) Окислительно-восстановительные свойства диоксида марганца.
При обычных условиях ведет себя довольно инертно. При нагревании с кислотами проявляет окислительные свойства, например, окисляет концентрированную соляную кислоту до хлора:
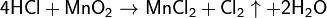
С серной и азотной кислотами MnO2 разлагается с выделением кислорода:
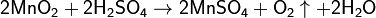
При взаимодействии с сильными окислителями диоксид марганца окисляется до соединений Mn7+ и Mn6+:
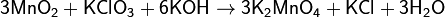
Диоксид марганца проявляет амфотерные свойства. Так, при окислении сернокислого раствора соли MnSO4 перманганатом калия в присутствии серной кислоты образуется чёрный осадок соли Mn(SO4)2.
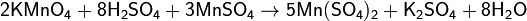
При сплавлении с щелочами и основными оксидами MnO2 выступает в роли кислотного оксида, образуя соли манганиты:
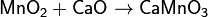
Билет№20. 2) Кислородные кислоты хлора и их соли. Устойчивость, изменение кислотных и окислительно-восстановительных свойств в зависимости от валентного состояния. Хлорная известь.
Кислородные кислоты хлора и их соли являются окислителями.
Кислородные кислоты хлора соответствуют общей формуле НОС1n, в которой n = 1, 2, 3 или 4 в соответствии с различными степенями окисления хлора.
Все кислородные кислоты хлора обладают окислительными свойствами. Особенно сильным окислителем является хлорноватистая кислота, поскольку она очень склонна к распаду с образованием свободного кислорода. Самой прочной из кислородных кислот хлора является хлорная кислота, но и она обладает сильными окислительными свойствами в концентрированных растворах.
Соли кислородных кислот хлора в нейтральной или щелочной средах окислительных свойств не проявляют. Соли кислородных кислот хлора более устойчивы, чем сами кислоты, но при повышенных температурах и они являются сильными окислителями.
Активность кислородных кислот хлора возрастает от хлорноватистой к хлорной кислоте. Окислительная их активность увеличивается в обратном порядке - от хлорной к хлорноватистой, которая является наименее устойчивой.
Соли кислородных кислот хлора обладают весьма разнообразными свойствами. Получение многих из них так или иначе связано с кристаллизацией из растворов. Однако удельный вес процесса кристаллизации в технологии получения того или иного соединения различен.
Из кислородных кислот хлора только хлорная кислота HCIO4 известна в свободном виде.
Хлорноватистая кислота — HClO
Хлористая кислота — HClO2
Хлорноватая кислота — HClO3
Хлорная кислота HClO4
Хлорная известь Ca(Cl)OCl — смесь гипохлорита, хлорида и гидроксида кальция. Относится к так называемым смешанным солям.
Получают взаимодействием хлора с гашеной известью (гидроксидом кальция):
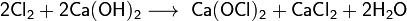 .
.
На воздухе хлорная известь медленно разлагается по схеме:
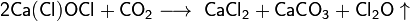 .
.
 , термическое разложение
, термическое разложение
 2020-07-12
2020-07-12 392
392








