Барометрическая формула. Распределение Больцмана. При выводе основного уравнения молекулярно-кинетической теории газов и максвелловского распределения молекул по скоростям предполагалось, что на молекулы газа внешние силы не действуют, поэтому молекулы равномерно распределены по объему.
При рассмотрении закона распределения Максвелла предполагалось, что молекулы равномерно распределяются по всему объему сосуда, что справедливо, если объем сосуда небольшой.
Для больших объемов равномерность распределения молекул по объему нарушается из-за действия силы тяжести, вследствие чего плотность, а следовательно, и число молекул в единице объема будут неодинаковым.
Рассмотрим молекулы газа, находящегося в поле тяготения Земли.
Выясним зависимость давления атмосферы от высоты над поверхностью Земли. Допустим, на поверхности Земли (h = 0) давление атмосферы P0. На высоте h оно равно P. При увеличении высоты на dh давление уменьшится на dP:
dP = - ρgdh
[ρ — плотность воздуха на данной высоте, ρ = mn0, где m — масса молекулы, n0 — концентрация молекул].
Используя соотношение P = n0kТ, получаем
тогда
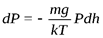
Полагая, что на некоторой высоте h Т = соnst, g = соnst, разделяя переменные, интегрируем это выражение
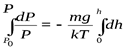 ,
, 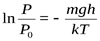
Получаем
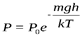 — барометрическая формула.
— барометрическая формула.
Барометрическая формула показывает зависимость давления газа от высоты над поверхностью Земли.
Если учесть, что концентрация молекул воздуха в атмосфере определяет давление, то формулу можно записать в виде
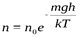
Из формулы следует, что с понижением температуры число частиц на высоте, отличной от нуля, убывает и при Т = 0К обращается в нуль, т. е. при 0К все молекулы расположились бы на земной поверхности.
Так как потенциальная энергия молекул на различной высоте различна и на высоте h определяется по формуле где ЕП = mgh, то [см.
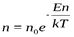
— закон Больцмана, показывающий распределение участвующих в тепловом движении молекул в потенциальном поле сил, в частности в поле силы тяжести.
 2020-07-12
2020-07-12 124
124








