План лекции:
1. Общая классификация, гомологический ряд
2. Номенклатура и изомерия
3. Химические свойства
1. Общая классификация, гомологический ряд
Углеводороды — это органические соединения, состоящие из атомов углерода и водорода, классифицирующиеся следующим образом:
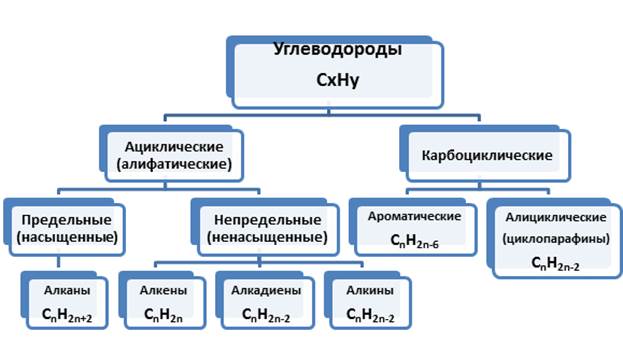
Предельные углеводороды (алканы, насыщенные углеводороды, парафины, алифатические соединения) – это углеводороды линейного или разветвленного строения, содержащие только простые (одинарные) связи. Предельными углеводородами являются алканы, образующие гомологический ряд с общей формулой CnH2n+2. Простейшим представителем класса является метан (CH4).
| Гомологический ряд алканов (первые 10 членов) | ||
| Метан | CH4 | CH4 |
| Этан | CH3—CH3 | C2H6 |
| Пропан | CH3—CH2—CH3 | C3H8 |
| Бутан | CH3—CH2—CH2—CH3 | C4H10 |
| Пентан | CH3—CH2—CH2—CH2—CH3 | C5H12 |
| Гексан | CH3—CH2—CH2—CH2—CH2—CH3 | C6H14 |
| Гептан | CH3—CH2—CH2—CH2—CH2—CH2—CH3 | C7H16 |
| Октан | CH3—CH2—CH2—CH2—CH2—CH2—CH2—CH3 | C8H18 |
| Нонан | CH3—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH3 | C9H20 |
2. Номенклатура и изомерия
Названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. По номенклатуре основой для названия служит одна углеродная цепь, а все другие фрагменты молекулы рассматриваются как заместители. В этом случае выбирают наиболее длинную цепь углеродных атомов и атомы цепи нумеруют с того конца, к которому ближе стоит углеводородный радикал. Затем называют: 1) номер углеродного атома, с которым связан радикал (начиная с простейшего радикала); 2) углеводород, которому соответствует длинная цепь. Если в формуле содержится несколько одинаковых радикалов, то перед их названием указывают число прописью (ди-, три-, тетра- и т. д.), а номера радикалов разделяют запятыми. Вот как по этой номенклатуре следует назвать изомеры гексана:
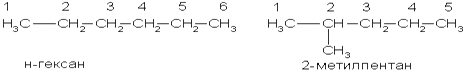
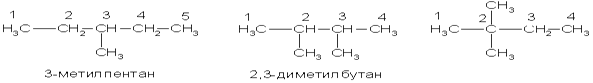
3.Химические свойства
Алканы имеют низкую химическую активность. Это объясняется тем, что единичные C-H и C-C связи относительно прочны и их сложно разрушить. Поскольку углеродные связи неполярны, а связи С — Н малополярны, оба вида связей малополяризуемы, их разрыв наиболее вероятен по гомолитическому механизму то есть с образованием радикалов.
3.1. Реакции радикального замещения
а) галогенирование алканов протекает по радикальному механизму. Для инициирования реакции необходимо смесь алкана и галогена облучить УФ-светом или нагреть. Хлорирование метана не останавливается на стадии получения метилхлорида (если взяты эквимолярные количества хлора и метана), а приводит к образованию всех возможных продуктов замещения, от метилхлорида до тетрахлоруглерода. Хлорирование других алканов приводит к смеси продуктов замещения водорода у разных атомов углерода. Соотношение продуктов хлорирования зависит от температуры, а галогенирование происходит тем легче, чем длиннее углеродная цепь н -алкана. Галогенирование — это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атомы галогенируются в последнюю очередь). Галогенирование алканов проходит поэтапно — за один этап замещается не более одного атома водорода:
1. CH4 + Cl2 → CH3Cl + HCl (хлорметан)
2. CH3Cl + Cl2 → CH2Cl2 + HCl (дихлорметан)
3. CH2Cl2 + Cl2 → CHCl3 + HCl (трихлорметан)
4. CHCl3 + Cl2 → CCl4 + HCl (тетрахлорметан).
б) нитрование – замещение атома водорода нитрогруппой – NO2 c образованием нитроалканов; нитрующий реагент азотная кислота HNO3. Алканы реагируют с 10 % раствором азотной кислоты или оксидом азота NO2 в газовой фазе при температуре 140 °C и небольшом давлении с образованием нитропроизводных.
СH4 + HО-NO2 → СН3NO2 + H2O.
метан азотная нитрометан
кислота
Все имеющиеся данные указывают на свободнорадикальный механизм. В результате реакции образуются смеси продуктов.
в) сульфирование (замещение атомов водорода сульфогруппой -SO3Н с образованием алкансульфокислот RSO3Н). Сульфирующий реагент – серная кислота Н2SO4 (НО─SO3Н). Сульфирование алканов происходит при действии очень концентрированной Н2SO4 при небольшом нагревании. Наиболее легко замещается атом водорода у третичного атома углерода:
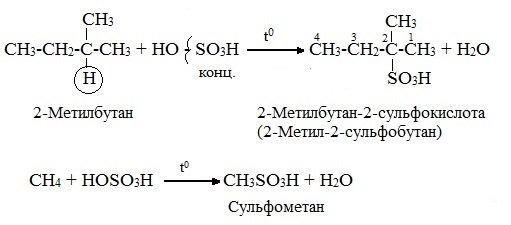
3.2. Реакции окисления
а)окисление кислородом воздуха при высоких температурах(горение)
Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения. Пример:
CH4 + 2O2 → CO2 + 2H2O
В случае нехватки кислорода вместо углекислого газа получается угарный газ или уголь (в зависимости от концентрации кислорода).
2CH4 + 3O2 → 2CO + 4H2O
б) окисление кислородом воздуха при невысоких температурахв присутствии катализаторов. В результате могут образоваться альдегиды, кетоны, спирты, карбоновые кислоты.
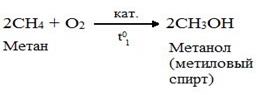
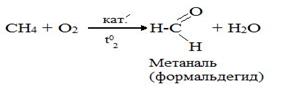
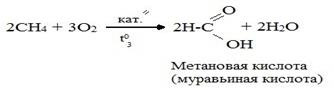
3.3. Термические превращения алканов
а) разложение происходит лишь под влиянием больших температур, что приводит к разрыву углеродной связи и образованию свободных радикалов.
CH4 → C + 2H2 (t > 1000 °C)
C2H6 → 2C + 3H2
СН3 – СН2 – СН2 – СН3 → СН3 – СН3 + СН2 = СН2
СН3 – СН2 – СН2 – СН3 → СН4 + СН2 = СН2– СН3
б) дегидрирование – отщепление водорода; происходит в результате разрыва связей С ─ Н; осуществляется в присутствии катализатора при повышенных температурах с образованием алкена:
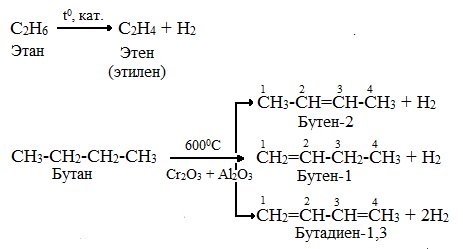
в) дегидроциклизация (ароматизация) - реакция дегидрирования, которая приводит к замыканию цепи в устойчивый цикл. Алканы с шестью или более углеродными атомами в цепи в присутствии катализатора циклизуются с образованием бензола и его производных:
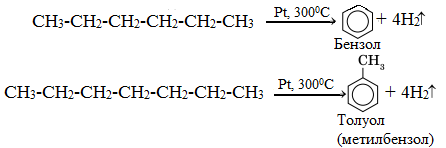
 2020-08-05
2020-08-05 214
214







