Тема 25. Ароматические соединения
К ароматическим соединениям относят все соединения, содержащие бензольное кольцо (одно или несколько). Ароматические соединения, как и остальные органические соединения, классифицируют по функциональным группам.
Ароматические углеводороды (арены)
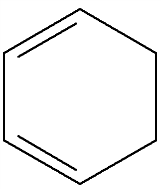
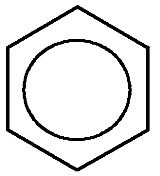
По строению и свойствам, ароматические углеводороды принципиально отличаются от близких внешне циклогексена и циклогексадиена:
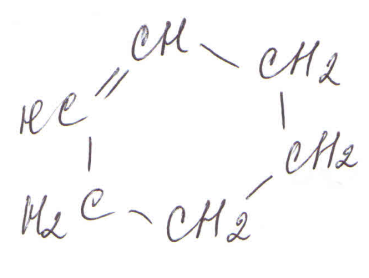
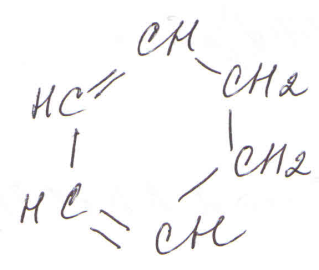
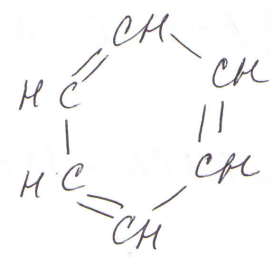
или
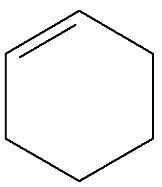
 ,
, 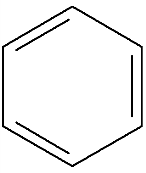
циклогексен циклогексадиен бензол
Напоминаю, что циклоалкены, циклоалкадиены и циклоалкины часто встречаются в цепочках (см. далее разбор задач 33). Свойства этих непредельных циклических соединений схожи со свойствами ациклических непредельных: алкенов, алкадиенов, алкинов. Тут же отметим, что формулы циклических соединений, в том числе и ароматических, предпочтительно записывать в виде геометрических фигур без указания символа углерода. Не допускается некая промежуточная форма – такая формула не будет засчитана на экзамене:
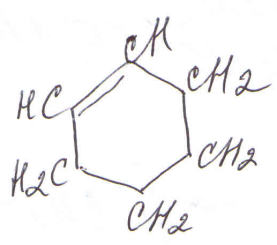
Бензольное кольцо, формально содержащее три двойные связи, отличается аномальной стабильностью. Разберем строение молекулы бензола С6Н6.
Каждый атом углерода в бензоле находится в состоянии sp 2-гибридизации, каждый атом углерода образует три σ-связи (две с атомами углерода и одну – с атомом водорода). Шесть атомов углерода замкнуты в кольцо: обычно рисуют правильный шестиугольник:
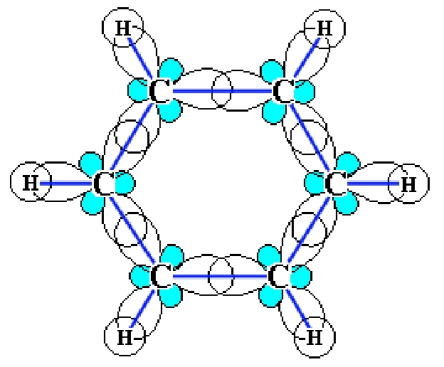
Четвертый p -электрон каждого атома не гибридизован, шесть p -орбиталей располагаются перпендикулярно плоскости кольца. Все шесть р -электронов взаимодействуют между собой, образуют единое π-электронное облако и единую химическую связь для всех атомов углерода.
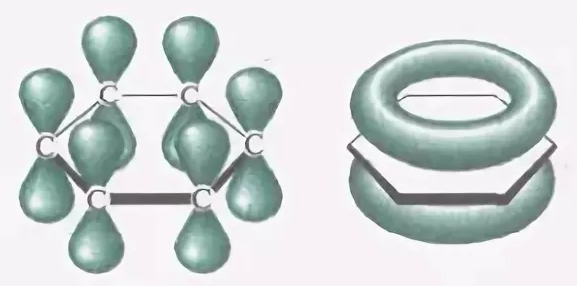
Бензол обычно обозначается или формулой Кекуле – чередованием простых и двойных связей, или шестиугольником с замкнутой линией внутри кольца.
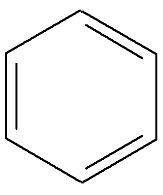 или
или 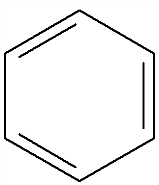
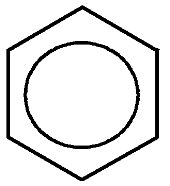
Считается, что сам бензол правильнее обозначать 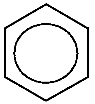 но гомологи и производные бензола – формулой Кекуле
но гомологи и производные бензола – формулой Кекуле 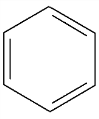 , так как заместители нарушают симметрию делокализованного π-электронного облака.
, так как заместители нарушают симметрию делокализованного π-электронного облака.
Таким образом, в молекуле бензола нет чередования одинарных и двойных связей, а существует делокализованная π-электронная система, за счет которой бензольное кольцо обладает специфическими свойствами.
Бензольное кольцо чрезвычайно устойчиво, несмотря на кажущуюся ненасыщенность – С6Н6 – бензол не вступает в классические реакции присоединения по двойной связи (присоединение возможно, но в очень жестких условиях). Наиболее характерными для бензола являются реакции замещения.
 2020-09-24
2020-09-24 153
153







