Неподеленная электронная пара кислорода вступает в сопряжение с p-электронной системой бензольного кольца, поэтому в фенолах полярность связи –О–Н увеличена:

Фенолы – более сильные кислоты, чем спирты, поэтому раньше фенол называли карболовой кислотой.
1) В растворе фенол диссоциирует с образованием Н+:

В растворе фенола (в отличии от растворов спиртов) индикаторы меняют свой цвет, показывая кислую среду.
Но фенол – слабая кислота, слабее даже угольной. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей.
Но если в бензольное кольцо ввести электронноакцепторный заместитель, полярность связи –О–Н увеличится, например популярное соединение 2,4,6-тринитрофенол (пикриновая кислота) сильнее угольной:
 пикриновая кислота
пикриновая кислота
2) Как и спирты, фенол реагирует со щелочными металлами с образованием фенолятов:
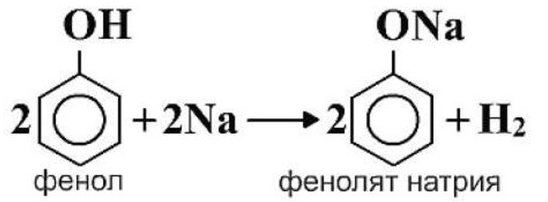
см. опыт:
https://youtu.be/XULMmtL5j7I
Любая кислота, даже раствор СО2, вытесняет фенол из фенолята:
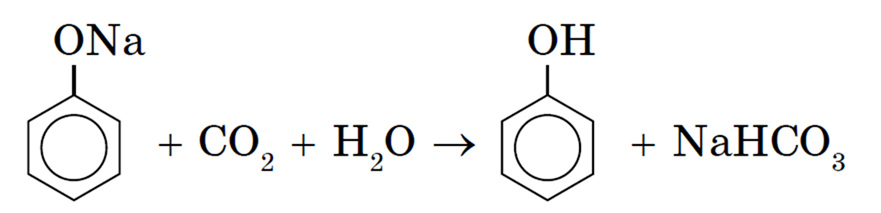
3) В отличии от одноатомных спиртов, фенол, являясь более сильной кислотой, реагируют с растворами щелочей:
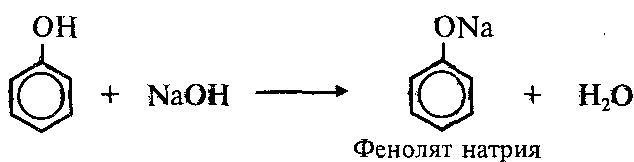
см. опыт:
https://youtu.be/A7kFugtDKR8
4) Качественная реакция на фенол – реакция с солями железа(III): образуется фенолят железа, раствор окрашивается в фиолетовый цвет:
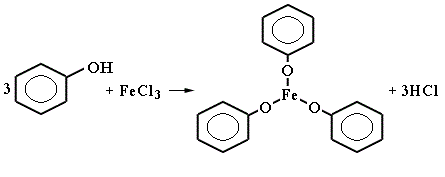
фенолят железа
см. видео:
https://youtu.be/78MleZfhQNE
5) В отличии от спиртов, фенол не реагирует с галогенводородными кислотами (спирты реагируют с НГ).
6)!!! В отличии от спиртов, фенол непосредственно не реагирует с карбоновыми кислотами (спирты реагируют с карбоновыми кислотами с образованием сложных эфиров).
Сложные эфиры фенола можно получить при взаимодействии фенола с ангидридами или галогенангидридами кислот, например:
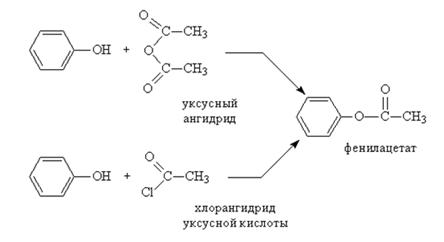
или через фенолят натрия:
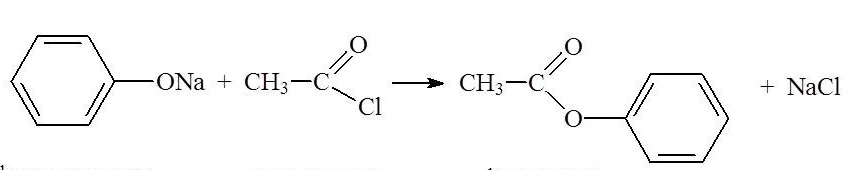
7) Простые эфиры образуются при взаимодействии фенола с галогеналканами, например:

8) Фенолы вступают в реакцию с альдегидами, наиболее известна реакция поликонденсации фенола с формальдегидом – образование фенол-формальдегидных смол (см. свойства альдегидов).
см. видео
https://youtu.be/WlNMzWGqb_U
 2020-09-24
2020-09-24 779
779








