Ароматические альдегиды и кетоны содержат карбонильную группу, связанную с бензольным кольцом:
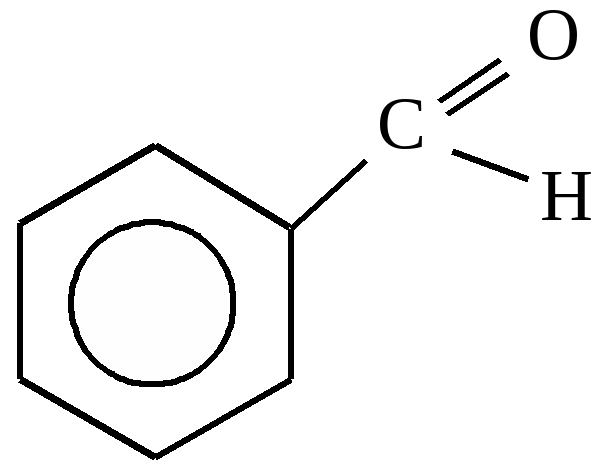 бензойный альдегид (фенилметаналь)
бензойный альдегид (фенилметаналь)
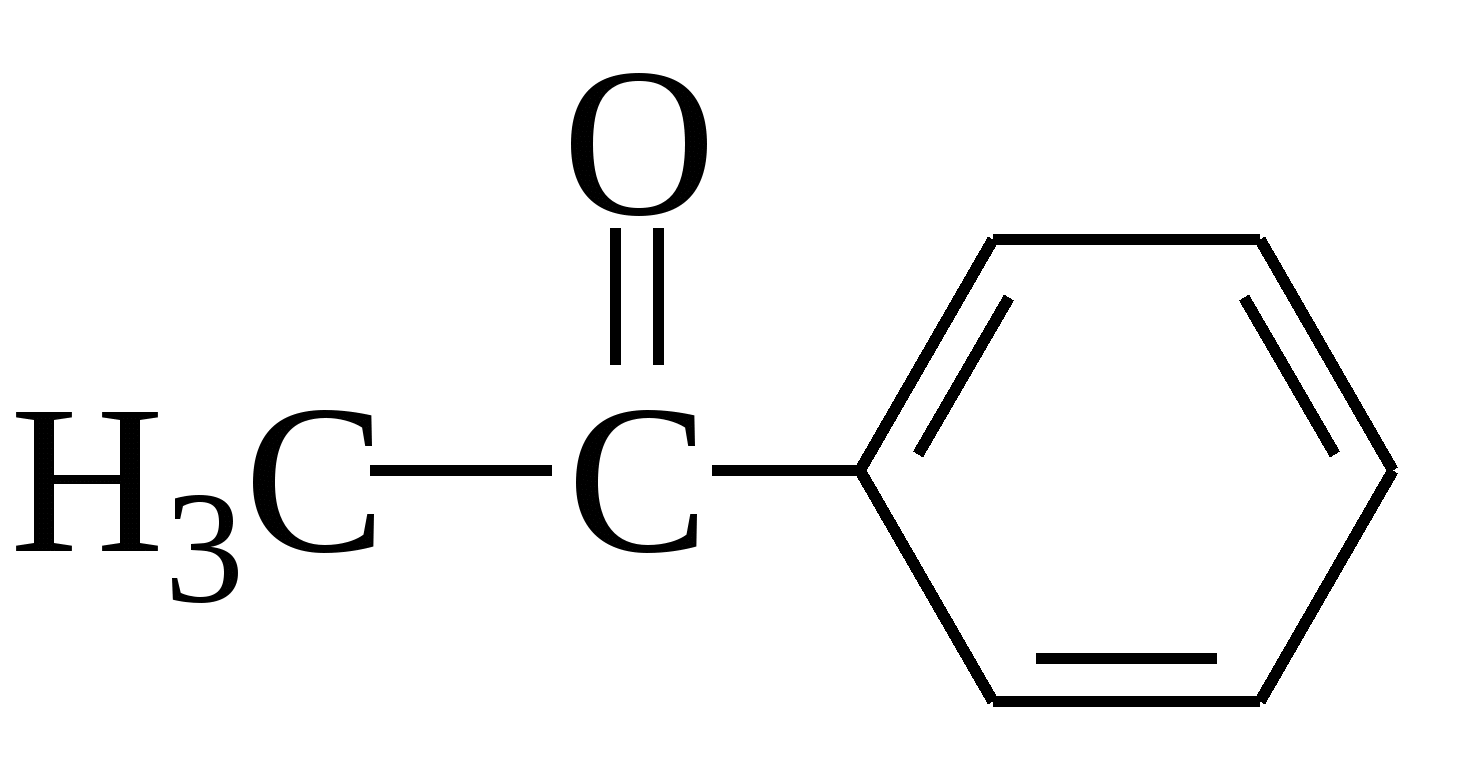 метилфенилкетон (ацетофенон)
метилфенилкетон (ацетофенон)
 дифенилкетон (бензофенон)
дифенилкетон (бензофенон)
Ароматические альдегиды и кетоны отличаются от алифатических несколько меньшей реакционной способностью.
Ароматические кислоты – производные ароматических углеводородов, у которых в бензольном ядре один или несколько атомов водорода замещены карбоксильными группами. Наличие бензольного ядра увеличивает кислотные свойства: они сильнее алифатических.
Надо знать простейшую ароматическую кислоту – бензойную:
 бензойная кислота
бензойная кислота
Также в ЕГЭ встречаются изомерные двухосновные фталевые кислоты:
 фталевая кислота (орто-фталевая кислота)
фталевая кислота (орто-фталевая кислота)
(1,2-бензолдикарбоновая кислота)
 изофталевая кислота (мета-фталевая кислота)
изофталевая кислота (мета-фталевая кислота)
(1,3-бензолдикарбоновая кислота)
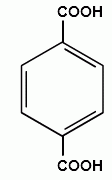 терефталевая кислота (пара-фталевая кислота)
терефталевая кислота (пара-фталевая кислота)
(1,2-бензолдикарбоновая кислота)
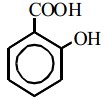
Большое значение имеют и гетерофункциональные соединения, содержащие карбоксильную группу:
(2-гидроксибензойная кислота)
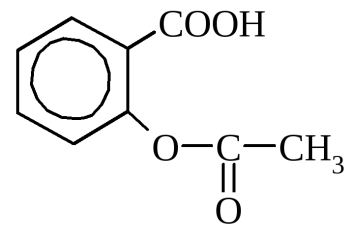 ацетилсалициловая кислота
ацетилсалициловая кислота
(эфиры салициловой кислоты по ОН-группе)
Ароматические кислоты образуют сложные эфиры, например:
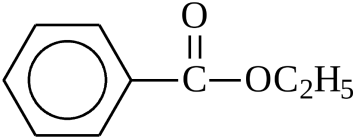 этиловый эфир бензойной кислоты, этилбензоат
этиловый эфир бензойной кислоты, этилбензоат
Терефталевая кислота и ее эфиры – основа многих полимеров. Например, при поликонденсации терефтелевой кислоты с этиленгликолем
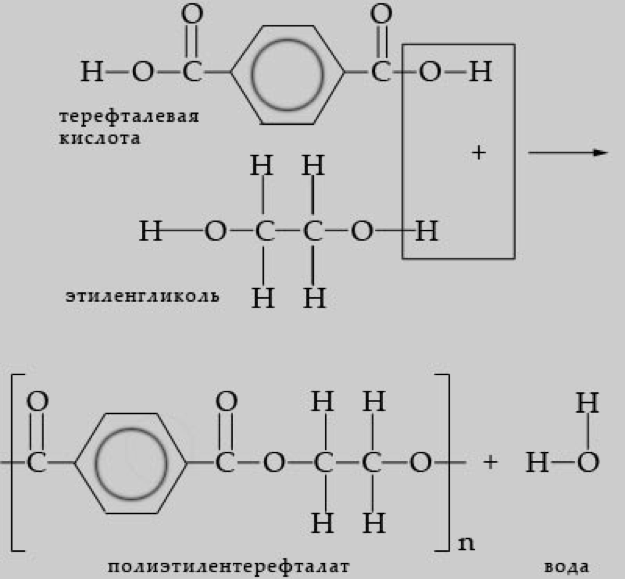
образуется полиэтиленгликольтерефталат (обычно его называют полиэтилентерефталат, ПЭТ), в России этот полимер называют лавсан по аббревиатуре ЛАборатории Высокомолекулярных Соединений Академии Наук, где он был получен в 1949 г. Этот полимер используется для производства пластиковых бутылок, прозрачных прочных нитей, волокон.
Ароматические амины
Рассмотрим только простейший ароматический амин – аминобензол или анилин:
 анилин
анилин
Анилин – маслянистая жидкость с резким запахом, малорастворимая в воде.
см. видео
https://youtu.be/BdP9Xgbe0xg?list=PLnbQh4j9gZkKZDdTU1xVdJZ8FQIvkJCWF
Особенность анилина – взаимное влияние аминогруппы и бензольного кольца.
Главное отличие анилина от аминов предельного ряда – неподеленная электронная пара азота вовлекается в бензольное кольцо:
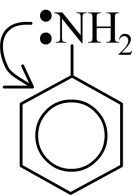
поэтому азот анилина, в отличии азота аммиака и аминов, в меньшей степени способен образовывать донорно-акцепторные связи с Н+.
Анилин более слабое основание, чем предельные амины и аммиак, его раствор не обнаруживает щелочную реакцию.
Анилин не реагирует с водой (не образует гидроксидов) и не изменяет окраску индикаторов.
см. опыт
https://youtu.be/8vsB95fs6Ls
Анилин способен реагировать только с сильными кислотами (соляной, серной) образуя соли фениламмония
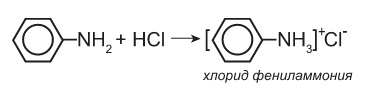
см. опыт
https://youtu.be/NjmJ8YLRoxI
Как соли слабого основания, соли фениламмония реагируют со щелочами с образованием анилина:
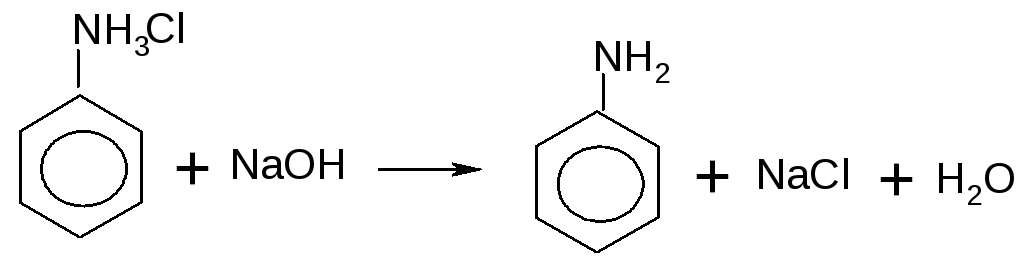
Главное отличие анилина от ароматических углеводородов – анилин обесцвечивает бромную воду. Так как аминогруппа является заместителем I рода и облегчает реакции замещения в бензольном ядре, анилин реагирует с бромной водой с образованием белого осадка 2,4,6-триброманилина:

см. опыт
https://youtu.be/3Kc76xYuetc
В отличие от аминов алифатического ряда, анилин легко окисляется, даже на воздухе он темнеет. Сильными окислителями анилин окисляется до различных хинонов от фиолетового до черного цвета. Например, при взаимодействии анилина с K2Cr2O7 образуется краситель «анилиновый черный». Анилин используется в производстве красителей и лекарств.
см. опыты
https://youtu.be/od3PMioRfRI
https://youtu.be/WHAVBS-k5zs
 2020-09-24
2020-09-24 759
759