Второй закон термодинамики является физическим принципом, накладывающим ограничение на направление процессов передачи тепла меж; телами.
Согласно этому закону невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому (одна из первых формулировок закона; М. В. Ломоносов, 1850 г.).
Существует несколько эквивалентных формулировок второго закона термодинамики, среди которых:
• постулат Клаузиуса: «Невозможно осуществить перенос тепла от более холодного тела к более горячему без затраты работы»;
• постулат Томсона: «Невозможно превратить какое-либо количество теплоты полностью в работу без того, чтобы часть теплоты не оказалась растраченной при более низкой температуре».
Энтропия (S) — важная функция состояния термодинамичесм системы. Энтропию можно охарактеризовать как меру хаотичности или неупорядоченности системы.
S= k∙lnW,
где W — число возможных микросостояний системы; k — постоянная Больцмана, равная отношению R/NA = 1,381•10-23 Дж/К; R — универсальная газовая постоянная, равная 8,315Дж/моль∙К); NA — постоянная Авогадро, равная 6,022•1023 моль-1.
При абсолютном нуле (Т = 0К) энтропия идеального кристалла равна нулю — полная упорядоченность, W = 1 (иногда это положение называется нулевым законом термодинамики).
Изменение энтропии (S) равно теплоте, подведенной к системе в обратимом изотермическом процессе, деленной на абсолютную температуру, при которой осуществляется этот процесс ∆ S = Q/T.
Для необратимого процесса при температуре Т: ∆S > Q/Т
В соответствии с изменением числа возможных микросостояний системы энтропия (S):
· возрастает при превращении жидкости или твердого тела в газ;
· увеличивается при растворении твердого вещества или жидкости в воде или в другом растворителе;
· уменьшается при растворении газа в воде или в другом растворителе;
· возрастает при увеличении числа частиц в системе;
· имеет меньшие значения в ковалентно связанных твердых веществах с прочными, пространственно направленными связями, по сравнению с кристаллами с частично металлической связью;
· повышается по мере ослабления связей между атомами.
На рис. 2.6 приведена типичная кривая изменения значений энтропии для вещества в широком диапазоне температур, в котором это вещество переходит из твердого кристаллического состояния в жидкое и далее из жидкого состояния в газообразное.
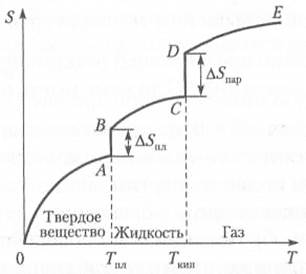
Рис. 2.6. Типичная зависимость энтропии вещества от температуры
Повышение температуры сопровождается ростом энтропии, которая вплоть до достижения температуры плавления кристаллического вещества (Тпл) изменяется по плавной кривой ОА (см. рис. 2.6). В точке плавления нарушается дальний порядок во взаимном расположении частиц, и энтропия скачкообразно возрастает на ∆S (отрезок АВ). Повышение температуры выше точки плавления вещества вызывает последовательное увеличение энтропии жидкости, которое происходит по плавной кривой ВС вплоть до достижения температуры кипения (Ткип). В этой точке жидкость полностью превращается в пар, и энтропия скачком возрастает на величину ∆Sпар, соответствующую отрезку CD. Далее энтропия газа изменяется по плавной кривой DE, и новое скачкообразное возрастание энтропии может произойти только в результате химических изменений газа (термической диссоциации, ионизации и т.п.), приводящих к увеличению числа частиц и росту беспорядка в системе.
Энтропия 1 моль вещества в стандартном состоянии называется стандартной энтропией (S°, Дж/(моль∙К). Изменение стандартной энтропии в химической реакции, аналогично изменению энтальпии, можно определить по уравнению
∆rS° = ∑ νj S°прод - ∑ νi S°реаг.
Пример 2.3. Рассчитаем изменение энтропии при получении сульфата цинка путем обжига сульфида цинка (сфалерита).
ZnS(k) + 2O2(г) = ZnSO4(k)
S° 298, Дж/(моль-К) 57,7 205,15 110,6
∆rS° = 110,6 – (57,7 + 2∙205,15) = -357,4 Дж/К.
Значения стандартной молярной энтропии различных веществ при 298К сведены в таблицы и имеются в справочной литературе. Стандартная молярная энтропия простого вещества не равна нулю. Стандартная молярная энтропия сложного вещества возрастает при увеличении числа атомов в молекуле.
 2020-09-24
2020-09-24 224
224








