Раствор, содержащий соли слабой многоосновной кислоты, также обладает буферным свойством. В этом случае роль кислоты играет наиболее кислая соль.
Карбонатный буферный раствор – NaHCO3 + Na2CO3.

 Na2CO3 ® CO32– + 2Na+ NaHCO3 ® HCO3– + Na+ HCO3– CO32– + Н+
Na2CO3 ® CO32– + 2Na+ NaHCO3 ® HCO3– + Na+ HCO3– CO32– + Н+
В этом растворе диссоциация гидрокарбонатного иона HCO3– подавлена из-за присутствия в растворе карбонатных ионов CO32–.
Концентрация протонов в растворе определяется константой диссоциации угольной кислоты по второй ступени:
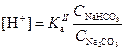
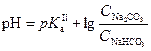
Фосфатный буферный раствор – NaH2PO4 + Na2HPO4
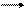
 Na2HPO4 ® HPO42– + 2Na+ NaH2PO4 ® Na+ + H2PO4– H2PO4– HPO42–+ Н+
Na2HPO4 ® HPO42– + 2Na+ NaH2PO4 ® Na+ + H2PO4– H2PO4– HPO42–+ Н+
В этом растворе диссоциация дигидрофосфатного иона H2PO4– подавлена из-за присутствия в растворе гидрофосфатных ионов HPO42–.
Концентрация протонов в растворе определяется константой диссоциации фосфорной кислоты по второй ступени:
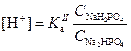
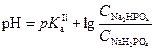
Произведение растворимости
Абсолютно нерастворимых солей не существует. Любая соль характеризуется растворимостью s – молярной концентрацией насыщенного раствора. При наличии насыщенного раствора соли и ее нерастворившегося осадка будет наблюдаться равновесие процесса растворения, которое с учетом полной диссоциации соли выглядит так:

 Ca3(PO4)2 (тв) Ca3(PO4)2 (раствор) ® 3Ca2+ + 2PO43–
Ca3(PO4)2 (тв) Ca3(PO4)2 (раствор) ® 3Ca2+ + 2PO43–
Равновесие между донной фазой и раствором может быть описано с помощью КР:
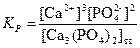
Но поскольку (см. 5.2) концентрация твердой фазы – постоянная величина, то
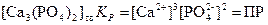 ,
,
где ПР – это произведение растворимости.
ПР = [Ca2+]3[PO43–]2
Концентрация ионов связана с растворимостью s: [Ca2+] = 3s, [PO43–]=2s, следовательно:
ПР = (3s)3(2s)2 = 108s5 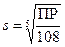
В общем виде, ПР соли состава (M+x)y(A-y)x, где +х и –у заряды катиона M и аниона A, соответственно, можно записать как:
ПР = (y∙s)y(x∙s)x = yy∙xx∙s(x+y) 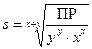
Условие выпадения осадка: произведение концентрации ионов в растворе должно быть больше произведения растворимости – 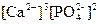 > ПР.
> ПР.
Задачи к разделу
 2020-09-24
2020-09-24 249
249








