Важным источником энергии в живой природе являются триглицериды жирных кислот, при биологическом окислении которых генерируется около 9 ккал/г (в среднем человек расходует в сутки около 2800 ккал). Как отмечалось выше, возможность накопления источника энергии в виде гликогена ограничена, тогда как жиры могут накапливаться многоклеточными организмами в количествах, обеспечивающих, например, зимнюю спячку грызунов и медведей или тысячекилометровые перелеты птиц. Жиры запасаются в специализированных клетках (адипоцитах) и транспортируются жидкими средами организма с помощью транспортных белков альбуминов в гидрофобных «карманах» или же с помощью различных биогенных поверхностно-активных веществ.
В желудочно-кишечном тракте животных жиры эмульгируются желчными кислотами и гидролизуются секретируемыми поджелудочной железой липазами на жирные кислоты, диацилглицерины и моноацилглицерины, которые всасываются стенками тонкого кишечника (плазма крови человека после сытной трапезы похожа на молоко). Отделившиеся от альбуминов жирные кислоты проходят через клеточные мембраны и попадают в цитозоль, где с участием аденозинтрифосфата ацилируют кофермент А по обычной схеме в присутствии ацил-СоА-синтетаз:

В обычных условиях равновесие этой реакции сдвинуто влево, например, такие макроэргические соединения, как тиоэфиры карбоновых кислот, используются клетками для биосинтеза АТФ и ГТФ (см. на стр. 142 превращение сукцинил-СоА), но пирофосфатаза гидролизует пирофосфат на две молекулы фосфорной кислоты и реакция становится необратимой.
Катаболические превращения жирных кислот протекают во внутренней среде (матриксе) митохондрий – клеточных органелл с двумя мембранами. Ацилированные жирными кислотами молекулы кофермента А проходят через внешнюю мембрану в межмембранное пространство с помощью простой диффузии, тогда как для преодоления внутренней мембраны митохондрий подключается дополнительное вещество – «челнок» – карнитин, образующийся из аминокислоты лизина по многостадийной схеме, включающей реакции метилирования концевой аминогруппы, гидроксилирования и укорочения углеродной цепи. В результате генетических нарушений может быть нарушен механизм образования карнитина или транспорт ацилкарнитина в митохондрии. У людей с таким нарушением в обмене веществ происходит ожирение мышечной ткани, сопровождающееся болевыми ощущениями в мышцах. Фермент карнитинацилтрансфераза I на внешней стороне внутренней мембраны митохондрий осуществляет реакцию:
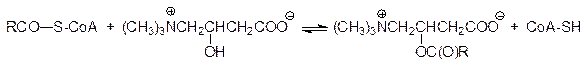
После этого ацилированный карнитин соответствующей транслоказой перемещается в матрикс митохондрий, где другой фермент карнитинацилтрансфераза II переносит ацильный остаток в обращение предыдущей реакции на внутримитохондриальный кофермент А, а карнитин снова выводится в межмембранное пространство митохондрий. Такой усложненный транспорт нужен для того, чтобы разделить кофермент А внутри и вне митохондрий, поскольку иначе живой природе пришлось бы находить возможность определения уровня кофермента А по разные стороны мембраны и выведения из митохондрий только тех его молекул, которые поступили в виде тиоэфиров с жирной кислотой.
Окисление жирных кислот начинается с реакции дегидрирования ацилкофермента А ацил-СоА-дегидрогеназой по схеме:

Затем еноил-СоА-гидратаза превращает тиоэфир транс -изомера a,b‑ненасыщенной кислоты в L -3-гидроксиацил-СоА:

а 3-гидроксиацил-СоА-дегидрогеназа превращает его в 3-кетоацил-СоА:
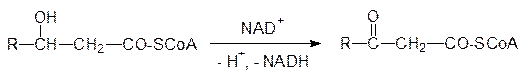
Образовавшееся b-дикарбонильное соединение расщепляется по С–С‑связи коферментом А. Поскольку эта реакция представляет собой тиолиз (разрыв связи сульфгидрильной группой), катализирующий ее фермент называется тиолазой:
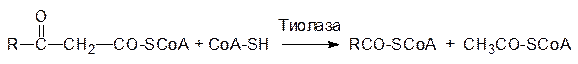
В результате этих превращений молекула жирной кислоты становится короче на два атома углерода, то есть это превращение соответствует b‑окислению. Повторение представленных выше ферментативных реакций на жирной кислоте с четным числом атомов углерода (основные кислотные компоненты жиров) приведет в конце концов к ацетоацетил-СоА, который расщепляется коферментом А в присутствии тиолазы на две молекулы ацетил-СоА, встраивающиеся, как и полученные на предыдущих стадиях, в цикл Кребса.
Если учесть все протекающие биохимические реакции, включая участие ацетильных остатков в цикле Кребса и окислительное фосфорилирование (см. гл. 8.) генерируемого в b-окислении и в цикле Кребса восстановительного потенциала, то катаболизм одной молекулы пальмитиновой кислоты приведет к образованию 106 молекул аденозинтрифосфата (АТФ), при этом суммарный КПД будет равен 33%. Или иначе: при окислении одного моля (256 г) пальмитиновой кислоты образуется 45000 г АТФ.
В живой природе реализуется также механизм a-окисления. В частности, в состав липидов клеток мозга входят a-гидроксизамещенные жирные кислоты, образующиеся при окислении жирных кислот монооксигеназами. При их дегидрировании получаются высшие a-кетокислоты, которые подвергаются окислительному декарбоксилированию кислородом в присутствии ионов Fe2+ и аскорбиновой кислоты, то есть по механизму, который отличается от описанного выше превращения пирувата и кетоглутарата. Образовавшиеся при этом кислоты с нечетным числом атомов углерода в цепи в результате b-окисления превращаются в пропионил-СоА, который карбоксилируется биотинзависящим ферментом в метилмалонил-СоА, изомеризующийся кобаламинзависимым ферментом с образованием участвующего в цикле Кребса сукцинил-СоА (см. стр. 108–109).
Для катаболического превращения ненасыщенных жирных кислот, входящих в состав жиров и липидов мембран, нужны дополнительные ферменты. Дело в том, что последовательное b‑окисление (например олеилкофермента А) приводит к соответствующему тиоэфиру цис -додец-3-еновой кислоты (цис -D3-С12-кислоты), тогда как субстратом еноил-СоА-гидратазы являются соответствующие эфиры транс -D2-ненасыщенных кислот. Далее следует очередь первого дополнительного фермента – енолил-СоА-изомеразы, катализирующей превращение по схеме:
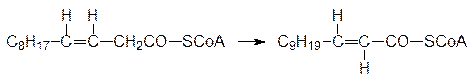
Образовавшийся тиоэфир транс -D2-С12-кислоты представляет собой обычный субстрат гидратазы. Если же катаболическому превращению подвергаются полиненасыщенные кислоты, то b‑окисление может привести к тиоэфирам цис -2-еновых кислот, которые гидратируются еноил-СоА-гидратазой. Продуктом реакции становится тиоэфир D -изомера 3‑гидроксизамещенной кислоты, и для перевода его в субстрат 3-гидроксиацил-СоА-дегидрогеназы служит 3-гидроксиацил-СоА-эпимераза. Так, например, катаболизм линоленовой кислоты в результате представленных выше превращений завершается образованием тиоэфира цис -D2-С12-кислоты, из которой L ‑3‑гидроксидеканоилкофермент А образуется по схеме, асимметрия в которой представлена условно:
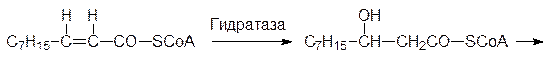

 2020-10-10
2020-10-10 177
177








