37. Назовите по заместительной номенклатуре следующие соединения:
а) HOCH2CH(OH)COOH б)(CH3)2 CH(OH)COOH
38. Какие галогенозамещенные кислоты следует взять для получения яблочной (2-гидроксибутановой),миндальной(2-гидроксифенилуксусной) кислот.
39. Напишите схемы реакций образования гидротартрата и тартрата калия.
40. В чём проявляется оптическая активность? Как называются стереоизомеры, обладающие оптической активностью? Что такое энантиомеры, диастереомеры? На примере винной кислоты укажите пару энантиомеров и пару диастереомеров:

41. Приведите проекционные формулы Фишера а)винной (2,3-дигидроксибутандиовой) б) яблочной (2-гидроксибутановой) кислот.
42. Какой структурный фрагмент в молекуле винной кислоты может образовывать комплексную соль меди (II)?
43. Какой химический процесс происходит при нагревании молочной кислоты с концентрированной серной кислотой? Напишите схему реакции. 44. Напишите схемы реакций кислотного и щелочного гидролиза γ-бутиролактама.
IV.Фенолокислоты
Общая характеристика.
Из ароматических гидроксикислот наибольшее значение имеют фенолокислоты, у которых гидроксильные группы непосредственно связаны с бензольным кольцом (фенольные гидроксильные группы). Изомерия фенолокислот обусловлена взаимным расположением –ОН и –СООН групп.
По систематической номенклатуре при формировании названия фенолокислот за родоначальную структуру принята бензойная кислота; наличие –ОН группы отражается префиксом гидрокси- (окси-). Для многих фенолокислот употребляются тривиальные названия – салициловая, галловая и др.
Способы получения
Фенолокислоты чаще всего получают прямым карбоксилированием фенолов, т.е. непосредственным введением –СООН группы. При взаимодействии сухого феноксида натрия с СО2, который при обработке минеральной кислотой превращается в салициловую к-ту:
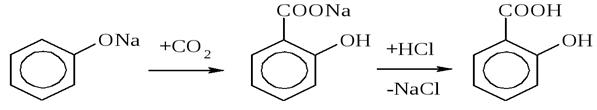
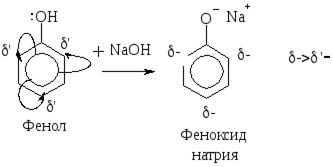
Реакция протекает по механизму SЕ. Поскольку СО2 является слабым электрофилом, непосредственно в реакцию с фенолом он не ступает. Для активации бензольного кольца фенол превращают в феноксид натрия. Отрицательно заряженный атом кислорода феноксид-иона проявляет значительно более сильные электронодонорные свойства, чем неионизированная –ОН группа. Поэтому в феноксид-ионе бензольное кольцо обладает большой активностью в реакциях электрофильного замещения.
Химические свойства
Фенолокислоты являются сильными кислотами. Сила салициловой кислоты кислоты возрастает за счет образования внутримолекулярной Н–связи

Салициловая кислота обладает более кислотными свойствами, чем ее мета- и пара-изомеры.
 2020-10-11
2020-10-11 238
238








