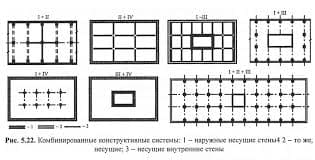
| Процесс | Работа | Теплота | Уравнение состояния газа |
| Изотермный |  | 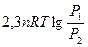 | 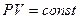 |
| Изохорный | 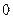 | 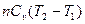 | 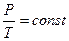 |
| Изобарный | 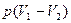 | 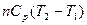 * * | 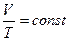 |
| Адиабатный |  | 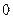 | 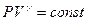 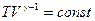 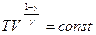 |
Примечание: * -  Дж/моль· К.
Дж/моль· К.
Задача: СО2 в количестве 100 г находится при 0 °С и давлении 1,013· 105 Па. Определить Q, А, ∆U, ∆Н:
а) при изотермном расширении до объема 0,2 м3;
б) при изобарном расширении до того же объема;
в) при изохорном нагревании до достижения давления 2,026 ·105 Па;
г) при адиабатном сжатии до 2,026· 105 Па.
Принять, что СО2 подчиняется законам идеальных газов, а истинная мольная теплоемкость СО2 при постоянном давлении постоянна и равна 37,1 Дж/моль·К.
Решение:
а) Для изотермного расширения 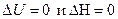 :
: 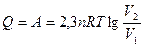 .
.
Число молей СО2 в 100 г составляет: 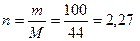 моль.
моль.
Первоначальный объем определяем по уравнению
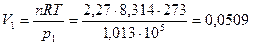 м3.
м3.
Количество теплоты равно
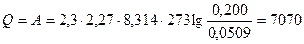 Дж.
Дж.
б) Для изобарного процесса  ,
,
так как  ;
; 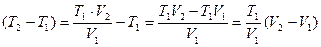 .
.
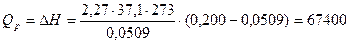 Дж.
Дж.
Работа расширения газа в изобарном процессе
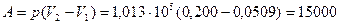 Дж.
Дж.
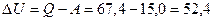 кДж.
кДж.
в) Для изохорного процесса: 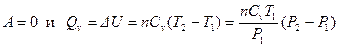 .
.
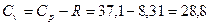 Дж/моль·К.
Дж/моль·К.
Отсюда 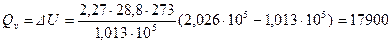 Дж.
Дж.
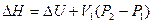 .
.
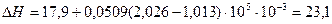 кДж.
кДж.
г) Для адиабатного сжатия
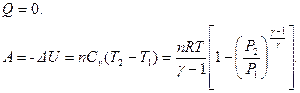
Коэффициент 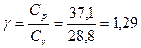 .
.
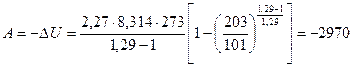 Дж.
Дж.
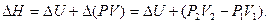
Выражая конечный объем V2 из уравнения адиабаты 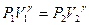 , получим
, получим
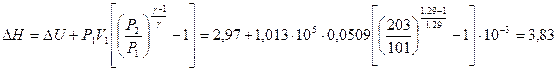 кДж.
кДж.
 2014-02-04
2014-02-04 1501
1501