Ароматические амины – бесцветные жидкости и твердые вещества. Вследствие окисления жидкие ароматические амины часто бывают окрашены в желтый цвет. Малорастворимы в воде.
Анилин – бесцветная маслянистая жидкость, из-за долгого хранения темнеет, так как окисляется, плохо растворим в воде. Температура кипения – 182 оС, температура плавления – 6 оС, немного тяжелее воды, является ядом аккумулирующего действия.
1. Анилин легко окисляется различными окислителями, поэтому темнеет при хранении. При действии хлорной извести (CaOCl2) на водный раствор анилина, появляется интенсивное фиолетовое окрашивание. Это качественная реакция на анилин.
2. Горение
4C6H5─NH2 + 31O2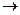 24CO2 ↑+ 2N2↑ + 14H2O
24CO2 ↑+ 2N2↑ + 14H2O
3. Основные свойства выражены слабее, чем у аммиака и алифатических аминов, из-за влияния ароматического ядра на аминогруппу. С минеральными кислотами образует соли
C6H5─NH2 + HCℓ 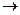 [C6H5─ NH3]
[C6H5─ NH3]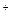 Cℓ
Cℓ → (C6H5─ NH2•HCℓ)
→ (C6H5─ NH2•HCℓ)
хлорид фениламмония солянокислый анилин
Соли анилина хорошо растворимы в воде, но не растворимы в неполярных органическихрастворителях. Действием щелочи на соли анилина можно выделить его в чистом виде
[C6H5─ NH3] Cℓ + NaOH 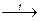 C6H5─NH2 + NaCℓ + H2O
C6H5─NH2 + NaCℓ + H2O
4. Реакция ацетилирования
H O
C6H5─NH2 + (CH3СO)2O 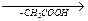 C6H5 –
C6H5 –  –
– 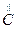 – CH3
– CH3
ацетанилид
5. Реакции электрофильного замещения:
а) галогенирование (идет очень легко). Реакция с бромом – качественная реакция на анилин
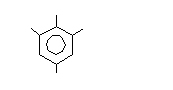
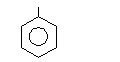 NH
NH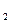 NH
NH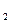
Br Br
+ 3 Br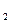
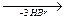
Br
2,4,6-триброманилин
б) нитрование. С концентрированной азотной кислотой идет со взрывом с образованием n-нитроанилина;
в) при сульфировании анилина образуется сульфаниловая кислота, амиды которой являются лекарственными веществами;
6. Реакции диазотирования. С азотистой кислотой анилин образует диазосоединения – соли диазония, которые широко применяются в производстве красителей.
C6H5─NH2 + NaNO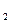 + 2HCℓ
+ 2HCℓ 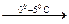 [C6H5N
[C6H5N N]
N]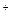 Cℓ
Cℓ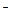 + NaCℓ + 2H2O
+ NaCℓ + 2H2O
хлористый фенилдиазоний
 2014-02-02
2014-02-02 1941
1941








