Катионы шестой аналитической группы катионов
1. Общая характеристика группы.
2. Частные реакции катионов второй аналитической группы.
3) Реакции на катион ртути (II).
К шестой аналитической группе катионов относятся катионы Cu2+, Hg2+, Co2+, Ni2+. Cd 2+ Хлориды, сульфаты и нитраты этих катионов хорошо растворимы в воде. Растворы солей меди (II) окрашены в голубой цвет, кобальта (II) — в розовый, а никеля (II) — в зеленый.
Гидроксиды катионов этой группы являются труднорастворимыми слабыми электролитами, гидроксиды Сu(ОН)2 и Hg(OH)2 неустойчивы и разлагаются на соответствующий оксид и воду, Сu(ОН)2 при нагревании, a Hg(OH)2 при обычной температуре.
Соли катионов шестой аналитической группы подвергаются гидролизу в водных растворах.
Для катионов этой группы характерны реакции комплексообразования. Растворы аммиака осаждают Сu, Hg, Со, Ni, Cd в виде гидрооксидов. При избытке аммиака они растворяются, образуют комплексные соединения:
[Сu (NH3) 4]2+, [Hg (NH3) 4J2+, [Co (NH3) б]2+, [Ni (NH3) 6 ]2+
Медь, ртуть и кобальт имеют переменную степень окисления, поэтому для них характерны окислительно-восстановительные реакции. Некоторые из этих реакций используются для открытия отдельных ионов. Например, ион Hg2+ открывают восстановлением его до Hg(I) и затем до свободной ртути действием SnС12.
Медь принадлежит к числу микроэлементов, очень малые количества которых необходимы для нормальной жизнедеятельности живых организмов. Удобрения, содержащие медь, способствуют росту растений на некоторых малоплодородных почвах, повышают их устойчивость против засухи и холода. В человеческом организме медь обнаружена в составе эритроцитов. Она оказывает заметное влияние на повышение сопротивляемости организма к вредному воздействию некоторых факторов внешней среды.
Частные реакции катионов шестой аналитической группы
Реакции катиона ртути (II) Hg2+
1. Гидроксиды щелочных металлов NaOH и КОН осаждают из растворов солей ртути (II) желтый осадок оксида ртути:
Hg(NO3)2+ 2КОН → HgO↓+ Н2О + 2KNO3
Hg2+ + 2ОН- → HgO↓+ Н2О.
Осадок легко растворим в кислотах. Реакция является фармакопейной.
2. Иодид калия KI с солями ртути (II) дает красный осадок иодида ртути (II):
Hg (NО3) 2 + 2KI → HgI2↓+ 2KNO3
Hg2+ + 2I - → HgI2↓
Осадок растворяется в избытке реактива с образованием бесцветной комплексной соли:
HgI2 + 2I- → [HgI2]2-
Реакция часто используется для обнаружения ионов Hg2+, хотя ионы Сu2+ мешают определению. Реакция является фармакопейной.
3. Хлорид олова (II) SnCl2 восстанавливает соли ртути (II) до нерастворимого хлорида ртути (I) белого цвета:
2HgCl2+ SnCl2 → Hg2Cl2 ↓+ SnCl4
2Hg2++ Sn2+ + 2Сl-→ Hg2Cl2↓ + Sn4+
Если реактив брать в избытке, то происходит дальнейшее восстановление ртути до металлической:
Hg2Cl2 + SnCl2 → 2Hg↓+ SnCl4
Hg2Cl2 + Sn2+ → 2Hg↓+ Sn4+ + 2Сl-
Этой реакцией пользуются для обнаружения иона ртути (II).
4. Реакция с сульфид - ионом. Реакция является фармакопейной. Катионы Hg2+ осаждаются из водных растворов сульфид – ионом в виде черно- коричневого осадка. Реакция протекает в несколько стадий. Вначале образуется белый осадок, постепенно изменяющий окраску через желто- красную и бурую на черно- коричневую при избытке сульфид – ионов.
HgCl2 +2H2S → 2HgS? HgCl2↓+ 4HCl
2HgS? HgCl2+2H2S → 3HgS+ 2HCl
Сульфид ртути (II) не растворяется в разбавленной азотной кислоте, но растворим в царской водке.
Реакции катиона меди (II) Сu2+
1. Гидроксиды щелочных металлов NaOH и КОН из растворов солей меди (II) выделяют на холоду голубой осадок гидроксида меди (II):
CuSО4 + 2КОН → Сu(ОН)2↓ + K2SO4
Cu2+ + 2ОН-→ Сu(ОН)2↓
При кипячении смеси раствора с осадком гидроксид меди (II) разлагается, теряя воду:
Сu(ОН)2 → СuО + Н2О
Осадок растворим в концентрированном растворе аммиака:
Сu(ОН) 2 + 4NH3 → [Сu(NH3) 4](ОН) 2.
2. Водный раствор аммиака, взятый в избытке, образует с солями меди (II) комплексное соединение меди (II) ярко - синего цвета:
CuSО4+ 4NH3 → [Сu(NH3)4]SO4
Cu2++ 4NH3 → [Сu(NH3) 4] 2+
Реакция является наиболее характерной для иона Сu2+ и чаще всего применяется для его обнаружения. Проведению реакции мешают ионы Ni2+ и Со2+.
Реакция фармакопейная.
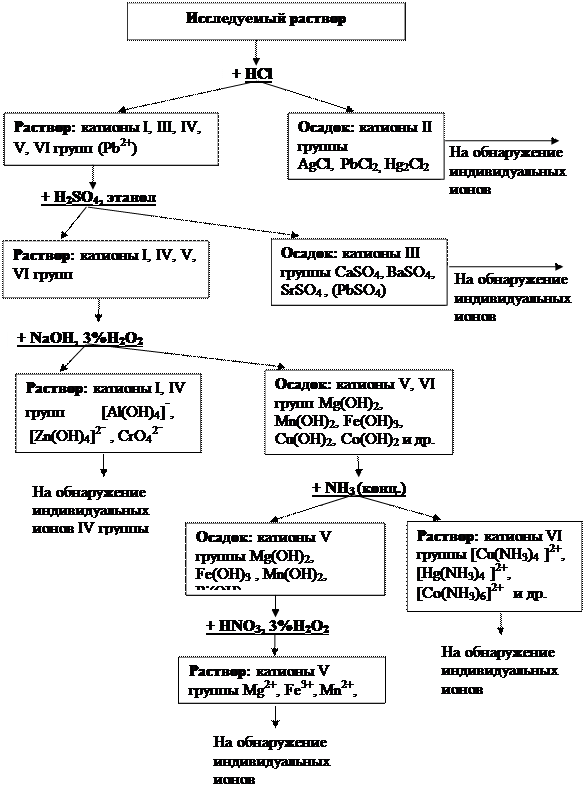
Схема анализа катионов I-VI аналитических групп представлена на рисунке 6
|
3. Гексацианоферрат (II) калия. K4Fe(CN)6] осаждает из нейтральных или слабокислых растворов солей меди(II) красно – бурый осадок
2CuCl2 + K4[Fe(CN)6] → Cu2[Fe(CN)6]↓ + 2К2SO4
2Cu2+ + [Fe(CN)6]4- → Cu2[(CN)6]↓
осадок не растворяется в разбавленных кислотах, но растворяется в 25% растворе аммиака.
Cu2[Fe(CN)6] + 12NH3+ 4Н2О→ (NH4)4[Fe(CN)6]+ 2[Сu(NH3)4](OH)4
4. Иодид калия или натрия окисляется солями меди (II) до свободного иода:
2СuSO4 + 4KI → 2CuI ↓ + 2К2SO4+ I2.
5. Реакция восстановления меди (II) до металлической меди. Реакция фармакопейная. Металлы, расположенные в ряду напряжений металлов леве меди, восстанавливают катион Cu2+ до металлической меди. Чаще для этой цели используют металлический алюминий, цинк, железо.
Cu2++ Zn → Cu + Zn2+
Cu2++ Fe → Cu + Fe 2+
Схема систематического анализа катионов всех шести аналитических групп представлена на рисунке 6.
Тема: «Анионы»
1. Общая характеристика анионов.
3. Частные реакции на анионы первой аналитической группы.
4. Частные реакции на анионы второй аналитической группы.
5. Частные реакции на анионы третьей аналитической группы.
Анионы образуются в основном p-элементами и некоторыми d- элементами (Cr, Mn). Высокой способностью к образованию анионов обладают p-элементы, расположенные в верхнем правом углу Периодической системы Д. И. Менделеева. Они имеют переменную степень окисления и способны к образованию кислот, причем сила кислот возрастает с увеличением степени окисления.
Классификация анионов основывается на различной растворимости солей бария и серебра соответствующих кислот, классификация анионов представлена в таблице 2
Первая группа анионов: фосфат-ион РО43- сульфат-ион SO42-, сульфит-ион SO32-, карбонат-ион СО32-, тиосульфат-ион S2O32-, метаборат-ион ВО2-(или тетраборат-ион В4О72-) и оксалат-ион С2О42-. Перечисленные ионы образуют с ионами бария Ва2+ труднорастворимые в воде соли. Групповым реагентом является ВаСl2 в нейтральной или слабощелочной среде.
Вторая группа анионов: хлорид-ион С1-, бромид-ион Вг-, иодид-ион I-, сульфид-ион S2-. Анионы второй группы образуют с ионами Ag+ труднорастворимые в воде и нерастворимые в разбавленной азотной кислоте соли. Групповым реагентом является AgNO3 в присутствии разбавленной азотной кислоты.
Третья группа анионов: нитрат-ион NO3-, нитрит-ион NO2- и ацетат-ион СН3СОО-. Серебряные и бариевые соли этих анионов хорошо растворимы в воде. Группового реагента нет.
Таблица 2
 2014-02-02
2014-02-02 19592
19592
