Электрический пробой мембран может играть какую бы то ни было роль в живой клетке, только если будет доказано, что пробой может происходить под влиянием собственного мембранного потенциала, т.е. разности потенциалов на мембране, которую сама мембрана генерирует в результате диффузии ионов. Опыт, который показывает, что такое бывает, приведен на рис. 7.
К раствору, омывающему БЛМ, добавляли переносчик протонов через мембрану (протонофор) ClCCP, а затем с одной стороны мембраны вводили немного кислоты, чтобы создать на мембране разность pH (DpH). На мембране возникал ионный диффузионный потенциал, величина которого при небольших DpH совпадала с теоретической величиной, рассчитанной по известному уравнению Нернста:
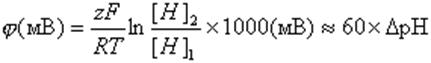 (6)
(6)
Так при DpH = 1,2 теоретический потенциал должен быть 72 мВ, что близко к опытным данным (см. рис. 7, снизу). Но при DpH = 3,2 теоретический потенциал 192 мВ не достигается. Когда потенциал немного не доходит до 140 мВ мембрану пробивает электрическим полем и измеряемый прибором потенциал падает. При этом мембрана не разрушается механически, по крайней мере, некоторое время. Если осуществить "короткое замыкание" водных растворов по сторонам мембраны с помощью солевого мостика, потенциал сбрасывается и мембрана "самозалечивается" (см. рис. 8). После удаления солевого мостика повторяется та же картина: быстро нарастает потенциал, который по достижении потенциала пробоя (около 140 мВ) падает и т. д. Опыт можно проделать два-три раза, пока мембрана, наконец, не разрушится. Таким образом, мембрану может "пробивать" электрический потенциал, который она же и создает.
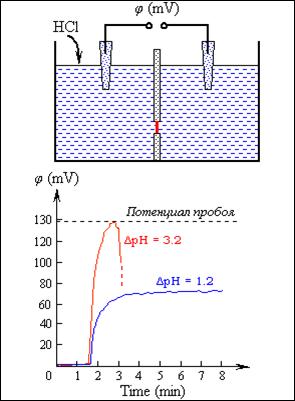 Рис.7. Самопробой БЛМ протонным диффузионным потенциалом
Рис.7. Самопробой БЛМ протонным диффузионным потенциалом
Измерение потенциала генерируемого мембраной в результате диффузии ионов в присутствии переносчика протонов ClCCP (сверху). Запись измерения потенциала (снизу). После добавления ClCCP с одной стороны мембраны добавляли кислоту для создания разности pH (DpH).
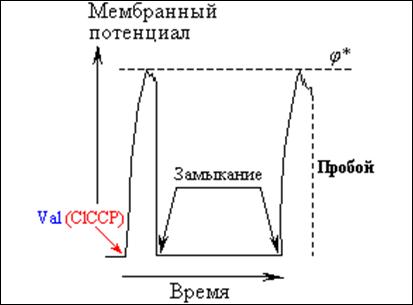 Рис.8. Электрический пробой мембран собственным мембранным потенциалом.
Рис.8. Электрический пробой мембран собственным мембранным потенциалом.
Источником электродвижущей силы в данном случае служит сама мембрана, по сторонам которой созданы разные концентрации ионов: K+ (или H+). Мембранный потенциал появлялся в ответ на введение ионофора: валиномицина (val) – переносчик ионов калия (или ClCCP – переносчик протонов). Как только потенциал достигал критического значения, наступал электрический пробой и измеряемый потенциал начинал падать. В этот момент производилось "короткое замыкание" растворов по сторонам мембраны с помощью солевого мостика. После удаления мостика потенциал вновь развивался и вторично наступал электрический пробой мембраны (при потенциале пробоя j*). Однако во второй раз короткое замыкание не осуществлялось, и наступал механический разрыв мембраны (пунктир
Потенциал пробоя фосфолипидных везикул (липосом)
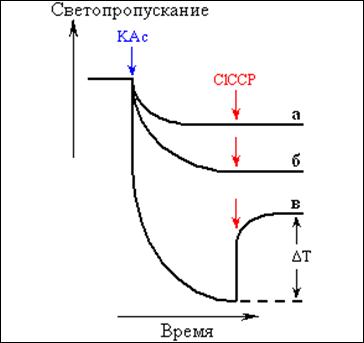
Для создания потенциала на мембранах фосфолипидных везикул к суспензии липосом в незабуференном растворе сахарозы добавляли ацетат калия. Уксусная кислота в недиссоциированной форме проникает внутрь липосом, создавая на мембране разность концентраций ионов водорода (DpH). Эта разность концентраций препятствует дальнейшему вхождению ацетата, и липосомы сжимаются под влияние осмотического давления K+ и Ac– снаружи. Судить о таком сморщивании липосом можно по возрастанию светорассеяния (и уменьшению светопропускания) суспензии, как это видно на рис. 9. О наступлении пробоя можно судить по резкому скачку светопропускания суспензии (DT на рис. 9), который связан с входом ацетата калия в липосому. Если отложить величину этого скачка светопропускания как функцию потенциала на мембране, рассчитанного по уравнению Нернста, то мы увидим отчетливый перелом на кривой, который соответствует потенциалу пробоя (см. рис. 10).
 2014-02-03
2014-02-03 716
716








