Рис.12. Электрический пробой мембран митохондрий
При добавлении к митохондриям субстратов появляется мембранный потенциал (Dj). При добавлении ацетата уксусная кислота проникает в матрикс, уменьшая DpH на мембране и тем самым увеличивая Dj (левая кривая). Этот потенциал стабилен. Если добавить больше ацетата, Dj вырастет сильнее, но он не держится (правая кривая).Величина tga на правой кривой характеризует утечку ионов через мембрану, пробитую слишком высоким потенциалом. См также рис. 13.
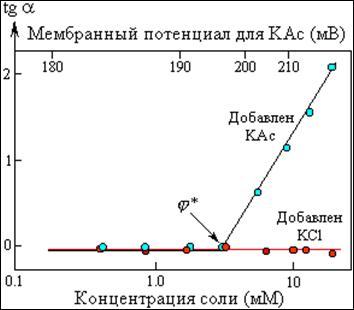
Рис.13. Зависимость скорости падения мембранного потенциала (tga на рис. 12) от концентрации добавленного ацетата (нижняя ось) и мембранного потенциала (верхняя ось)
Точка перелома на кривой с KAc соответствует началу пробоя мембраны и может рассматриваться как потенциал пробоя j *.
На рисунке также видно, что добавление KCl вместо KAc не приводит к пробою мембраны.
На всех исследованных объектах (БЛМ, липосомы, эритроциты и митохондрии) было показано, что перекисное окисление липидов приводит к снижению потенциала пробоя, т.е. уменьшению электрической прочности (стабильности) липидного слоя мембран. Некоторые экспериментальные данные, демонстрирующие этот вывод, приведены на рисунках 14 (a), 15 и 16.
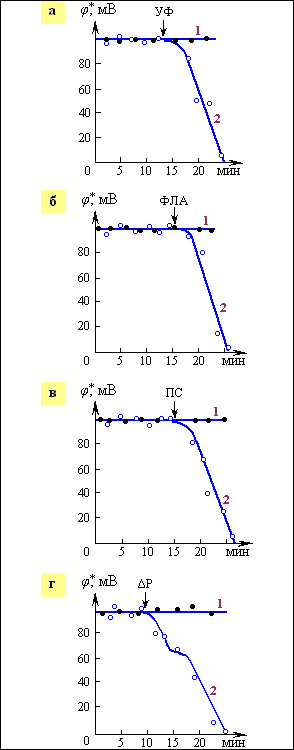
Рис.14. Снижение электрической прочности БЛМ при действии основных четырех факторов нарушения барьерной функции мембран в патологии:
перекисного окисления (ультрафиолетового излучения) – УФ (а, кривая 2), фосфолипазы А2 – ФЛА2 (0,2 мкг/мл) (б, кривая 2), протаминсульфата – ПС (0,025 мг/мл) (в, кривая 2), при растяжении мембраны за счет гидростатического давления DР (г, кривая 2). Кривые 1 – контроль (без воздействия фактора).
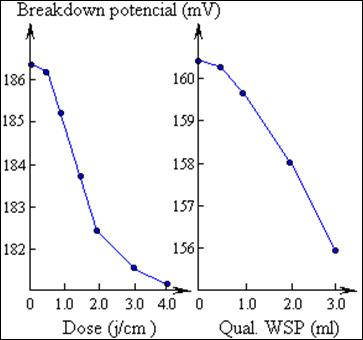
Рис.15. Снижение электрической прочности мембран липосом при УФ облучении (слева) и при добавлении водорастворимых продуктов перекисного окисления липидов (WSP – water-soluble products) (справа)
 Рис.16. Электрический пробой мембран эритроцитов хлорным диффузионным потенциалом
Рис.16. Электрический пробой мембран эритроцитов хлорным диффузионным потенциалом
[Cl]i и [C1]o, – концентрации иона хлорида в клетке и окружающей изотонической среде, соответственно; jm [Сl-] – мембранный потенциал, рассчитанный по уравнению Нернста на основе отношения (Сl-)i/(Cl-)o; jm (H+) – мембранный потенциал, рассчитанный по величине DрН, возникающей в среде после введения эритроцитов. Перелом на кривых свидетельствует о возрастании катионной проницаемости мембран. 1 – исходные эритроциты; 2 – эритроциты после перекисного окисления, вызванного УФ – облучением. Видно, что перекисное окисление липидов снижает потенциал пробоя от j*1 = 110 до j*2= 93 mV.
 2014-02-03
2014-02-03 775
775








