Первый закон термодинамики – закон сохранения энергии.
В качестве функции состояния наиболее показательна внутренняя энергия системы. Являясь суммой кинетической и потенциальной энергии всех атомов и молекул данной системы, она зависит от термодинамических параметров.
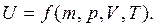
Ее производная 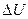 не зависит от пути перехода и является отражением
не зависит от пути перехода и является отражением
I-го закона ТД:
 ,
,
где 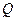 и
и 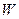 – сообщенное тепло и совершаемая работа, над системой (+), а (-) - самой системой, соответственно.
– сообщенное тепло и совершаемая работа, над системой (+), а (-) - самой системой, соответственно.
В дифференциальной форме I-ый закон ТД выглядит так:
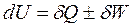 ,
,
где 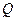 и
и 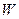 – сообщенное тепло и совершаемая работа, соответственно, не являются функциями состояния, так как это функции процесса, которые не могут быть выражены разностью начального и конечного значения и поэтому не имеют полного дифференциала.
– сообщенное тепло и совершаемая работа, соответственно, не являются функциями состояния, так как это функции процесса, которые не могут быть выражены разностью начального и конечного значения и поэтому не имеют полного дифференциала.
Следствием I-го закона термодинамики является закон Гесса, утверждающий, что тепловой эффект реакции не зависит от пути реакции, а только от начального и конечного состояния:
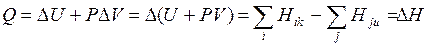 ,
,
где H-энтальпия, а ΔH – разница между энтальпией продуктов реакции (∑Hik) и исходными продуктами (∑Hju), РΔV- работа по изменению объёма.
Доказательства применимости I–го закона ТД к живым системам были приведены с помощью методов прямой и непрямой калориметрии.
Прямая калориметрия связана с непосредственным определением количества энергии в системе при полном сжигании ее в замкнутом пространстве (калориметрическая бомба).
Непрямая калориметрия основана на знании тепловых эквивалентов используемых с пищей веществ. В1904 г. Этуотер сконструировал дыхательный калориметр, измеряющий поток теплоты между его стенками, и поместил туда человека, измеряя количество калорий, выделяемых и потребляемых им с пищей в течение суток. В итоге измерений при минимальной работе, совершаемой человеком, оказалось, что эти величины (7784,1 кДж – потреблено с пищей и 7771 кДж – выделено) друг от друга отличались незначительно.
Табл.1 Значение дыхательных коэффициентов d и энергетических эквивалентов Q (энергия на 1 л О2) при окисление органических веществ
| Наименование вещества | d | Q, кДж/л |
| Углеводы | 21,0 | |
| Белки | 0,8 | 18,8 |
| Жиры | 0,71 | 19,6 |
Оба метода убедительно подтвердили применимость I-го закона ТД к биологическим системам.
 2014-02-03
2014-02-03 1202
1202
