Прямые методы, использующие графеновые нанотехнологии для быстрого обнаружения вирусов, в прошлом были мало исследованы, и в последовательных обзорах литературы не сообщалось о критическом обсуждении [ 96, 97 ].
Это отношение не изменилось даже во время чрезвычайной ситуации SARS – CoV-1, которая стала причиной инфекции тяжелого острого респираторного синдрома (SARS) в 2003 году в Азии, вызвавшей около 8000 случаев заболевания и 774 случая смерти, также во время ближневосточного респираторного дистресс-синдрома (MERS) в 2013 году., от которого пострадала Саудовская Аравия, в результате чего погибло около 858 человек [ 12, 98, 99, 100 ]. Достижения в области нанотехнологий начали играть важную роль в обнаружении вирусов, в повышении предела обнаружения и упрощении работы вирусной диагностики [ 78 ].
Графеновые полевые транзисторы с копланарным затвором (GFET) [ 71 ] были предложены для обнаружения вирусов ВИЧ-1 (вирус иммунодефицита человека 1) и MLV (вирус лейкемии мышей) с использованием антител к вирусу везикулярного стоматита Индианы (VSV) в качестве элемент биопознания. Антитела VSV иммобилизованы на слое G с помощью сукцинимидилового эфира 1-пиренбутановой кислоты (PASE). PASE связывает G за счет π-π взаимодействий, закрепляя первичные аминогруппы антитела за счет противоположной сукцинимидильной группы. Образование комплекса вирус-антитело приводит к понижению напряжения точки Дирака независимо от типов обнаруженных вирусов. Предлагаемая платформа работает в широком диапазоне концентраций (от 47,8 мкМ до 10,55 нМ), но отсутствие вирусной специфичности является основным ограничением этой стратегии.
Недавно был описан датчик поверхностного плазмонного резонанса (SPR) на основе функционализированного полиамидоамином rGO (композит с моноклональными антителами, иммобилизованными на самоорганизующемся дитиобис (сукцинимидил ундеканоат, DSU) для обнаружения / количественного определения вируса денге (DENV)) [ 97 ].
Специфичность и чувствительность сенсора были достигнуты за счет закрепления стабильного элемента биораспознавания (антител (IgM) против белков оболочки типа 2 денге) на золотой поверхности сенсора. Специфическое связывание антитела с Е-белком DENV 2 позволяет значительно изменить угол минимума отражательной способности, который коррелирует с обнаружением вируса Денге. Предлагаемый датчик показал чувствительный и селективный ответ на E-белки DENV 2 по сравнению с E-белками DENV 1 и E-белками ZIKV (вируса Зика). Хотя в описанный выше сенсор [ 97 ] не были интегрированы материалы G, критерии, использованные для его изготовления, были включены в этот обзор, так как эта стратегия может быть распространена на другие вирусы, а характеристики благородного металла SPR могут быть улучшены в наличие G [ 76 ].
В отличие от прошлого, нынешняя чрезвычайная санитарная пандемия, вызванная новым типом коронавируса (SARS – CoV-2), характеризуется глобальными усилиями по выявлению биомаркеров, которые предсказывают тяжесть заболевания пациентов с COVID-19, и разработке диагностических инструментов для быстрого выявления инфекции SARS – CoV-2 [ 101 ].
В настоящее время тестирование на нуклеиновые кислоты на образцах респираторных органов является эталонным золотым стандартом для диагностики пациентов, инфицированных COVID-19 [ 102 ]. Тест требует ряда лабораторных процедур: (а) выделение вирусной РНК; (b) добавление к мастер-смеси, содержащей воду, свободную от нуклеаз, обратные праймеры, зонд гасителя флуорофора и реакционную смесь (т.е. полимеразу, обратную транскриптазу, магний, нуклеотиды и добавки); (c) загрузка экстрагированной РНК / мастер-смеси в термоциклер для ПЦР; (d) несколько циклов при установленной температуре. Во время циклов ОТ-ПЦР расщепление зонда гасителя флуорофора генерирует флуоресцентный сигнал, обнаруживаемый и записываемый в режиме реального времени [ 101 ].
ОТ-ПЦР использует респираторные образцы для генетического обнаружения SARS – CoV-2; по некоторым данным, у 20–34% пациентов с COVID-19 тест показал отрицательный результат, несмотря на то, что они были инфицированы. Эта разница в чувствительности может быть в основном связана с низкой вирусной нагрузкой (т. Е. У пациентов, прошедших тестирование на ранней стадии вирусного заболевания) [ 102 ]. Другие проблемы RT-PCR включают трудоемкий и дорогостоящий анализ и техническую экспертизу при выполнении текста.
Для устранения этих недостатков быстро появляются другие технологии, такие как технологии в местах оказания медицинской помощи и серологические иммуноанализы [ 78 ].
Аналитические методы оценки предшествующей инфекции и иммунитета к SARS – CoV-2 путем идентификации антител важны для эпидемиологических исследований, хотя чувствительность и специфичность тестов, доступных в настоящее время на рынке, остаются неопределенными. Перекрестная реактивность антител к белкам коронавируса, не относящимся к SARS-CoV-2, является основной проблемой этих серологических тестов [ 101, 102 ]. Разработка теста на обнаружение антигена [ 102 ] мог бы воспользоваться прогрессом в производстве моноклональных антител против нуклеокапсидного белка SARS – CoV-2. Глобальные усилия по увеличению возможностей тестирования SARS – CoV-2 используют преимущества самых последних достижений в химии, молекулярной биологии, технологии генома и нанотехнологиях. В этом направлении ведется несколько проектов, некоторые результаты уже представлены в литературе [ 95, 103 ].
Обнаружение SARS-CoV-2 в респираторных образцах было достигнуто с помощью биосенсора LSPR, сочетающего фототермический эффект и плазмонную сенсорную трансдукцию вирусной нуклеиновой кислоты SARS-CoV-2 [ 103 ].
Seo et al. Сообщили о биосенсорном устройстве на основе полевого транзистора (FET) для обнаружения спайкового белка (S) SARS – CoV-2 в клинических образцах. [ 104 ]. Антитела против белка S были закреплены на листе графена (внешнее покрытие FET) сукцинимидиловым эфиром 1-пиренбутановой кислоты (PBASE, рис. 3).
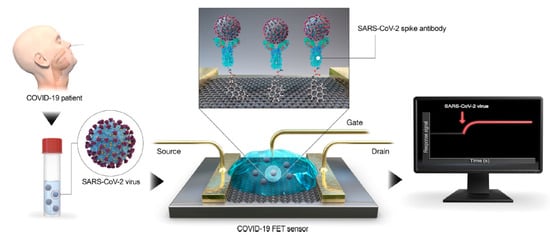
Рис. 3. Датчик на полевом транзисторе (FET) на коронавирусную болезнь 2019 (COVID-19). Графен выбран в качестве чувствительного материала и украшен спайк-антителом SARS – CoV-2 с использованием сукцинимидилового эфира 1-пиренбутановой кислоты (PBASE) в качестве взаимодействующей молекулы и линкера зонда. Перепечатано с разрешения из ссылки [ 104 ], Copyright © 2020, Американское химическое общество.
Работоспособность датчика определяется с использованием антигенного белка, культивированного вируса и образцов носоглоточного мазка от пациентов с COVID-19. Устройство могло обнаруживать белок S в концентрациях 1 фг / мл в PBS и 100 фг / мл в клинической транспортной среде, а также отличать антигенный белок SARS – CoV-2 от белков MERS-CoV. Успешное изготовление FET-датчика COVID-19 на основе интеграции спайкового антитела SARS-CoV-2 с графеном предполагает ключевую роль G для диагностической области [ 80 ]. В частности, функционализация G различными функциональными молекулами [ 14, 17, 105, 106 ] может быть ключевым элементом для адаптации его свойств и получения передовых диагностических инструментов для диагностики SARS – CoV-2. Между тем, для доработки этой рукописи в литературе сообщается о некоторых работах, посвященных датчикам для диагностики COVID-19 на основе графена [ 107 ], и, хотя, несомненно, необходимы дальнейшие исследования, ведущая роль G в мировой борьбе с COVID-19 явно выходит [ 108 ].
Таким образом, биомолекулы, которые до сих пор использовались для нацеливания на SARS-CoV-2, включают вирусную РНК, вирусные шиповые белки и специфические иммуноглобулины, продуцируемые иммунной системой хозяина. Сообщество биосенсоров активно работает над улучшением портативности, времени и стоимости обнаружения SARS – CoV-2 на основе ПЦР, а также над созданием производимых микрожидкостных устройств на основе ПЦР. Недавно была разработана технология редактирования генов (CRISPR / Cas) для решения проблем, связанных с системами на основе ПЦР. В технологии CRISPR были предложены два различных режима обнаружения: на основе связывания или расщепления [ 109 ]. Сенсор разработан путем иммобилизации на полевом транзисторе на основе графена (GFET) Cas9 с sgRNA, специфичной для целевой последовательности SARS COV-2; электрический сигнал, возникающий при связывании нуклеиновой кислоты-мишени комплексом Cas9-sgRNA, записывается с помощью простого портативного устройства без амплификации.
 2022-01-07
2022-01-07 148
148








