При анализе образцов, содержащих достаточно большое число видов разнообразных катионов, их взаимное мешающее действие не позволяет ис-пользовать дробный метод анализа. В этом случае используют систематиче-ский анализ, чтобы предварительно разделить эти ионы на более мелкие груп-пы с помощью подходящих групповых регентов, а затем определять отдель-ные виды катионов внутри каждой группы.
Аналитическая классификация катионов на группы проводится не по всей совокупности химических свойств элементов, а по небольшому числу выбранных свойств конкретных ионов, которые определяют конкретную спе-цифику их качественного анализа.
В каждом отдельном случае, исходя из определенных частных сообра-жений, выбирают свойства катионов для распределения их на группы. В ре-зультате созданы разные классификации катионов и, как следствие этого, разные схемы анализа: кислотно-основная, сероводородная, аммиачно-фос-фатная, тиоацетамидная и др. Каждая из этих схем анализа обладает опреде-ленными достоинствами и недостатками, но в конечном итоге при тщатель-ном выполнении все они дают правильные результаты.
| Аналитическая классификация катионов | Таблица 3 | |||
| Гру | Катионы | Группо- | Примечание | |
| ппы | вой реа- | |||
| гент | ||||
| Na+, K+, NH 4+ | Эти катионы в большинстве случаев образуют хорошо | |||
| I | - | растворимые соли и группового реагента не имеют. | ||
| Ag +, Hg 22+, | Эти катионы образуют малорастворимые хлориды. | |||
| II | Pb 2+ | HCl | Наибольшее значение произведения растворимости у | |
| PbCl2 (1,6 · 10-5), поэтому часть ионов Pb2+ остается в | ||||
| растворе и в ходе систематического анализа попадает в | ||||
| III группу. | ||||
| III | Ca 2+, Sr 2+, Ba 2+, | H2SO4 | Эти катионы образуют малорастворимые сульфаты. | |
| Pb 2+ | Наибольшей растворимостью обладает CaSO4 (ПР = 2,5 | |||
| · 10-5). Для снижения растворимости следует добавлять | ||||
| равный объем этилового спирта. | ||||
| IV | Al 3+, Cr 3+, Zn 2+, | NaOH | Эти катионы образуют амфотерные гидроксиды или | |
| As 3+, As 5+, Sn 2+, | растворимые соли кислородсодержащих кислот и | |||
| Sn 4+ | поэтому хорошо растворяются в избытке щелочей. | |||
| V | Bi 3+, Fe 3+, Fe 2+, | NaOH | Эти катионы образуют малорастворимые гидроксиды | |
| Mg 2+, Mn 2+, | или кислородсодержащие кислоты. | |||
| Sb 3+, Sb 5+ | ||||
| VI | Cd 2+, Co 2+, Cu 2+, | NH4OH | Эти катионы образуют прочные растворимые в воде | |
| Ni 2+, Hg 2+ | аммиакаты, в результате образования которых не- | |||
| растворимые гидроксиды легко переходят в раствор. | ||||





В основу кислотно-основной схемы анализа положено разное отноше-ние катионов к действию на них разных кислот и оснований, в частности,
HCl, H2SO4, NaOH, NH4OH. В соответствии с их действием выделены шесть групп катионов.
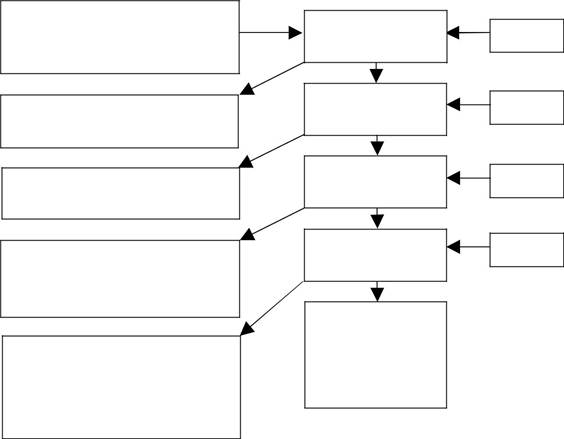
Предварительные испытания на катионы I группы:
Na +, K +,
Осадок хлоридов II группы:
AgCl, Hg 2 Cl 2, PbCl 2
Осадок сульфатов III группы:
CaSO 4, SrSO 4, BaSO 4, PbSO 4
Раствор соединений IV группы:
Раствор аммиакатов катионов VI группы:,
Раствор катионов I – VI группы
Раствор катионов III – VI группы
Раствор катионов IV – VI группы
Раствор катионов V – VI группы
Осадок катионов V группы:
Mg (OH)2,
Mn (OH)2, HSbO 2,
HSbO 3
HCl
H2SO4
NaOH
NH4OH
Рис. 2. Схема разделения катионов на аналитические группы.
В соответствии с кислотно-основной классификацией систематический ход качественного анализа смеси катионов можно представить схемой (рис.2), приведенной выше.
 2021-09-15
2021-09-15 283
283








